IDS159 - Installation d'un système de repositionnement surfacique (non irradiant) dans un service de Radiothérapie
Catégories
Les projets ou stages publiés auxquels vous accédez sont des rapports d'étudiants et doivent être pris comme tels. Il peuvent donc comporter des imperfections ou des imprécisions que tout lecteur doit admettre et donc supporter. Il ont été réalisés pendant les périodes de formation et constituent avant-tout des travaux de compilation bibliographique, d'initiation et d'analyse sur des thématiques associées aux concepts, méthodes, outils et expériences sur les démarches qualité dans les organisations ou sur les technologies en santé.
Si, malgré nos précautions, vous avez des raisons de contester ce droit de diffusion libre, merci de nous en faire part (master@utc.fr), nous nous efforcerons d'y apporter une réponse rapide. L'objectif de la présentation des travaux sur le web est de permettre l'accès à l'information et d'augmenter ainsi la qualité des échanges professionnels.
Nous ne faisons aucun usage commercial des travaux de projet ou de stage publiés, par conséquent les citations des informations et l'emploi des outils mis à disposition sont totalement libres. Dans ce cas, nous vous demandons de respecter les règles d'éthique en citant explicitement et complètement vos sources bibliographiques.
Bonne lecture...
Auteur

Contact
Jordy RAMOS : jordyramos.ids@gmail.com
Citation
A rappeler pour tout usage : J. RAMOS, "INSTALLATION D’UN SYSTEME DE REPOSITIONNEMENT SURFACIQUE (NON IRRADIANT) DANS UN SERVICE DE RADIOTHERAPIE", Université de Technologie de Compiègne (France), Master Ingénierie de la Santé, rapport de stage, https://travaux.master.utc.fr/, réf IDS159, février - juillet 2022, https://travaux.master.utc.fr/formations-master/ingenierie-de-la-sante/ids159/
Résumé
La radiothérapie est un domaine complexe du fait de sa technicité et de son développement rapide. En effet, le médecin doit s’entourer d’une équipe technique importante pour un traitement de qualité pour les patients.
De par la technicité et la précision attendue pour le traitement, il est essentiel d’avoir une position de traitement des plus proches de celle acquise au scanner. En effet, la délinéation et la planification dosimétrique impose une importante rectitude de la position du patient à chaque séance. Pour cela, les MERM définissent les contentions les plus adaptées à la morphologie de chaque patient dès la scanner de référence dosimétrique. Cependant, les outils mis à dispositions (contentions, lasers, points de tatouage) ne permettent pas toujours une position des plus reproductibles.
Pour cette raison, le CORT37 a décidé d’acquérir un système permettant le repositionnement des patients via un système de reconnaissance surfacique. Des réunions et des démonstrations ont été réalisées pour choisir le système le plus adapté aux besoins des utilisateurs et à l’optimisation du traitement des patients. Le CORT37 a ainsi choisi d’acquérir le système de VisionRT mais également de renouveler son parc de contentions.
La décision de l’implantation de ce système au CORT37 a demandé un travail conséquent pour le bon déroulement de sa mise en place et la formation de la totalité des utilisateurs. Un groupe de travail composé de MERM, d’un physicien, d’un médecin et d’un stagiaire ingénieur biomédical a été constitué pour réfléchir à la mise en place du système. Plusieurs réunions ont été réalisées pour gérer au mieux l’installation et prévoir en amont les problématiques qu’il est possible de rencontrer. Pour l’installation, une organisation au traitement a été nécessaire tel que la mise à disposition de l’accélérateur pendant 3 jours.
Les MERM référents ont formé la totalité des MERM. Les physiciens ont été formés sur l’utilisation du système et la gestion des pannes. Un suivi régulier est prévu pour éviter toutes dérives.
Une étude sur le temps de prise en charge des patients et la précision du système a été réalisée avec pour résultat, un gain de temps sur la mise en place du patient et un positionnement plus précis dans certains cas. Le système permet également un suivi morphologique à chaque séance.
La plupart des incidents avaient été réfléchi en amont permettant de les éviter ou d’intervenir très rapidement. L’installation s’est bien déroulé malgré quelques problèmes techniques rencontrés (installation sur la mauvaise partition du serveur, intervention pour l’installation plus courte que prévu impactant les traitements…). La mise en place d’un second système le mois suivant a permis de mettre à profit ces retours. Ce second système a pour but la mise en place d’une nouvelle technique, le DIBH.
Abstract
The radiotherapy is a complex field due to its technical nature and rapid development. Indeed, the physician must be surrounded by a large technical team to provide quality treatment for patients.
Because of the technical nature and the precision expected for the treatment, it is essential to have a treatment position as close as possible to that acquired on the scanner. Indeed, delineation and dosimetric planning require a high degree of accuracy in the patient's position at each session. To achieve this, the MERMs define the most suitable restraints for the morphology of each patient from the dosimetric reference scan. However, the tools available (restraints, lasers, tattoo points) do not always allow for the most reproducible position.
For this reason, CORT37 decided to acquire a system allowing the repositioning of patients via a surface recognition system. Meetings and demonstrations were held to choose the system best suited to the needs of users and to optimise patient treatment. CORT37 thus chose to acquire VisionRT system but also to renew its fleet of restraints.
The decision to implement this system at CORT37 required a great deal of work to ensure that it was properly set up and that all users were trained. A working group composed of MERMs, a physicist, a doctor and a trainee biomedical engineer was set up to think about the implementation of the system. Several meetings were held to manage the installation as well as possible and to anticipate any problems that might be encountered. For the installation, a treatment organisation was necessary, such as making the accelerator available for three days.
The referring radiographers trained all the radiographers. The physicists were trained on the use of the system and the management of breakdowns. Regular monitoring is planned to avoid any drift.
A study on the time taken to treat patients and the accuracy of the system has been carried out, resulting in a time saving on patient positioning and more accurate positioning in certain cases. The system also allows morphological monitoring at each session.
Most of the incidents had been thought out beforehand, allowing them to be avoided or to be dealt with very quickly. The installation went well despite some technical problems encountered (installation on the wrong server partition, intervention for the installation shorter than expected impacting the treatments...). The implementation of a second system the following month made it possible to take advantage of this feedback. The purpose of this second system is to implement a new technique, the DIBH.
Téléchargement

Mémoire complet
INSTALLATION D’UN SYSTEME DE REPOSITIONNEMENT SURFACIQUE (NON IRRADIANT) DANS UN SERVICE DE RADIOTHERAPIE
Remerciements
Je tiens à remercier toutes les personnes qui ont contribué au succès de mon stage et qui m’ont aidée lors de la rédaction de ce rapport.
Je voudrais dans un premier temps remercier, mon suiveur UTC Pol-Manoel FELAN, professeur à l’université de Compiègne, pour sa patience, sa disponibilité et surtout ses judicieux conseils, qui ont contribué à alimenter ma réflexion.
Je remercie également toute l’équipe pédagogique de l’UTC et les intervenants professionnels responsables de ma formation, pour avoir assuré la partie théorique de celle-ci.
Je tiens à témoigner toute ma reconnaissance aux personnes suivantes, pour leur aide dans la réalisation de ce rapport :
Monsieur Antoine LE BORGNE qui m’a beaucoup appris sur les défis à relever dans le monde médical. Il a partagé ses connaissances et expériences dans ce milieu, tout en m’accordant sa confiance et une large indépendance dans l’exécution de mes missions. Et pour avoir relu et corrigé mon mémoire. Ses conseils de rédaction ont été très précieux.
Je remercie également les médecins du CORT37 pour leur confiance et l’intérêt qu’ils ont portés à mon stage. Ainsi que toute l’équipe du CORT37 qui a su me soutenir dans ce projet.
Liste des abréviations
- ADN : Acide DésoxyriboNucléique
- ASN : Autorité de Sureté Nucléaire
- Adresse IP : Internet Protocol
- CBCT : Cone Beam Computerized Tomography
- CIRS : Fantome de test pour radiothérapie
- Clinac : Accélerateur linéaire de particule Varian
- CORT 37 : Centre d’Oncologie et de RadioThérapie 37
- CQ : Contrôle Qualité
- CQE : Contrôle Qualité Externe
- CRP : Conseiller en RadioProtection
- CTV : Clinical Target Volume
- DIBH : Deep-Inspirtation Breath-Hold
- DICOM : Digital Imaging and Communications in Medicine
- DM : Dispositif médical
- ESTRO : European Society for Therapeutic Radiology
- FFF : Flattening Filter Free
- GMAO : Gestion de Maintenance Assisté par Ordinateur
- GTV : Gross Tumor Volume
- IA : Intelligence Artificielle
- IGRT : Imaged Guided Radiation Therapy
- IPA : Infirmière de Pratique Avancée
- IRM : Imagerie par Résonance Magnétique
- ITV : Internal Target Volume
- kV : kiloVolt
- LAT D : Latéral Droit
- LED : Light-Emitting Diode
- MERM : Manipulateur en ElectroRadiologie Médicale
- MV : MegaVolt
- OAR : Organe à Risque
- ORL : Oto-Rhino-Laryngologie
- PC : Personal Computer
- POST : Postérieur
- PSLV : Pole Santé Léonard de Vinci
- PTV : Planning Target Volume
- RCMI : Radiothérapie Conformationelle avec Modulation d’Intensité
- RH : Ressources Humaines
- ROC 37 : société de Recherche Oncologique Clinique 37
- SGRT : Surface Guided RadioTherapy
- SFPM : Société Francaise de Physique Médicale
- SFRO : Société Francaise de Radiothérapie Oncologie
- STAFF : Réunion du personnel médical ou des médecins
- TDM : TomoDensitoMétrie
- TEP : Tomographie par Effet Positons
- TPS : Système de planification de traitement
- UH : Unité Hounsfield
- VMAT : Irradiation avec modulation d’intensité Volumétrique par ArcThérapie
Liste des figures
- Figure 1 : Plan d'accès au PSLV. 8
- Figure 2 : Plan d'accès aux différents services du PSLV. 9
- Figure 3 : Photo de Flemming(à gauche) et du CORT37(à droite) 9
- Figure 4 : Organisation du service de radiothérapie. 10
- Figure 5 : Plan du rez de jardin(à gauche) et du rez de chaussé(à gauche) 11
- Figure 6 : Zonage des bunkers en radiothérapie. 12
- Figure 7 : Schéma d'un accélérateur de particules de la marque Varian. 13
- Figure 8 : Photo du Scanner GE du CORT37. 14
- Figure 9 : Photo de l'appareil de curiethérapie. 15
- Figure 10:Contrôle des temps d'arrêt à différentes distances. 15
- Figure 11 : Photo d’un Truebeam(à gauche) et image d’un Halcyon (à droite)(d'après le site web Varian.com) 16
- Figure 12 : Parcours du patient en radiothérapie. 17
- Figure 13 : Points de tatouage et laser. Des outils utiles en radiothérapie au positionnement du patient 18
- Figure 14 : Délinéation des volumes cibles et des OAR par le médecin. 18
- Figure 15 : Traitement de stéréotaxie. 19
- Figure 16 : Les différentes étapes du dossier patient en radiothérapie. 20
- Figure 17 : Schéma de l'effet radio biologique des rayons X sur les cellules. 21
- Figure 18 : Schéma des volumes cibles en radiothérapie. 22
- Figure 19 : Technique de traitement en radiothérapie. 23
- Figure 20 : Contentions testées au CORT37. 24
- Figure 21 : Spiromètre de la marque Dyn'R. 25
- Figure 22 : Caméra de la marque VisionRT. 25
- Figure 23 : Système surfacique de la marqueC-RAD. 26
- Figure 24 : système surfacique de la marque Varian. 26
- Figure 25 : Système surfacique de la marque Brainlab. 27
- Figure 26 : Pupitre après installation du système AlignRT. 29
- Figure 27 : Salle de traitement avant(à gauche) et après(à doite) installation du système AlignRT. 30
- Figure 28 : Etalonnage du système AlignRT. 30
- Figure 29 : Diagramme d'Ishikawa pour la bonne réalisation du projet 31
- Figure 30 : Planning de formation. 32
- Figure 31 : CQ quotidien d'AlignRT. 34
- Figure 32 : Imagerie de positionnement illustrant la différence entre le positionnement sans(à gauche) et avec(à droite) AlignRT. 35
- Figure 33 : Temps de traitement sans(image supérieure) et avec(image inférieure) AlignRT. 36
- Figure 34 : Pupitre de traitement du Clinac 1 avant et après installation de AlignRT. 39
- Figure 35 : Image de scanner d'une application de curiethérapie. 42
- Figure 36 : Photo et image scanner du CIRS. 44
- Figure 37 : Cycle d'amélioration continu pour la mise en place d'une GMAO.. 46
Liste des tableaux
- Tableau 1 : Résultats des décalages après réalisation de l'imagerie irradiante pour 20 patientes. 36
- Tableau 2 : bilan personnel 48
Introduction
La radiothérapie est un domaine médical en constante évolution. Les domaines de l’imagerie, des techniques de traitements, de l’intégration de l’IA dans les outils informatiques, de nouveaux dispositif permettant des aides aux traitements sont en constante évolution et permettent de délivrer un traitement optimal aux patients [1].
La mise en place du patient est un point important dans le traitement de radiothérapie. Les avancées technologiques permettent de rendre les traitements plus précis pour le traitement de la tumeur et de réduire les complications qui peuvent y être liées. Cependant pour permettre la bonne réalisation des traitements, le positionnement du patient à chaque séance est un défi important. Pour cette raison différentes possibilités s’offre aux services de radiothérapie. L’utilisation des lasers, des contentions personnalisées, des imageurs embarqués ou d’autres techniques liées aux routines des centres étaient possible pour valider le positionnement du patient. Aujourd’hui, de nouvelles technologies voient le jour permettant un repositionnement identique à chaque séance dans le but de délivrer un traitement avec une grande précision.
A travers ce rapport, nous allons voir la mise en place d’un dispositif médical permettant le repositionnement surfacique du patient à chaque séance de radiothérapie. La radiothérapie étant un domaine complexe, avec des évolutions permanentes et une organisation particulière, des procédés sur l’intégration d’un tel système ont dû être mis en place pour une bonne gestion de ce projet.
Les points importants sur la gestion de ce projet seront abordés en expliquant, en amont, l’organisation du service pour en faire ressortir les problématiques rencontrées et les axes d’améliorations pour les projets futurs dans le but d’améliorer en continu les traitements des patients.
Nous commencerons ainsi par une présentation complète du service puis nous aborderons le projet d’installation du système de caméras surfaciques dans son ensemble et enfin quelques missions annexes réalisées durant ce stage.
I. Centre d’Oncologie et de Radiothérapie 37
A travers ce rapport nous verrons l’installations d’un système de repositionnement surfacique au sein du Centre d’Oncologie et RadioThérapie 37 (CORT37) à Chambray-les-Tours. Ce centre de radiothérapie est un service du Pôle Santé Léonard de Vinci.
1. Pôle santé Léonard de Vinci (PSLV)
Le PSLV se trouve à Chambray-lès-Tours au 7 avenue du professeur Alexandre Minkowski (Figure 1). Il est l’un des centres sanitaire principale de la région Centre à caractère privé. Regroupant 125 médecins, une équipe de 600 personnes et une capacité d’accueil de 460 lits dont 60 lits d’hospitalisation de jour.
Figure 1 : Plan d'accès au PSLV
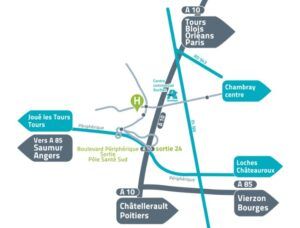
Créé en 2004 l’établissement regroupe donc un grand nombre de professionnels pour la prise en charge de bon nombre de pathologies (Figure 2). En effet le PSLV est le rassemblement des cliniques privées de Tours en un même endroit à travers différents pôles. Il s’y trouve un pôle maternité, un pôle chirurgie, un pôle médecine et soins palliatifs, un pôle cancérologie ainsi que des services d’imagerie lourde, d’imagerie conventionnelle, de médecine nucléaire, des laboratoires d’analyses et des cabinets privés.
Figure 2 : Plan d'accès aux différents services du PSLV
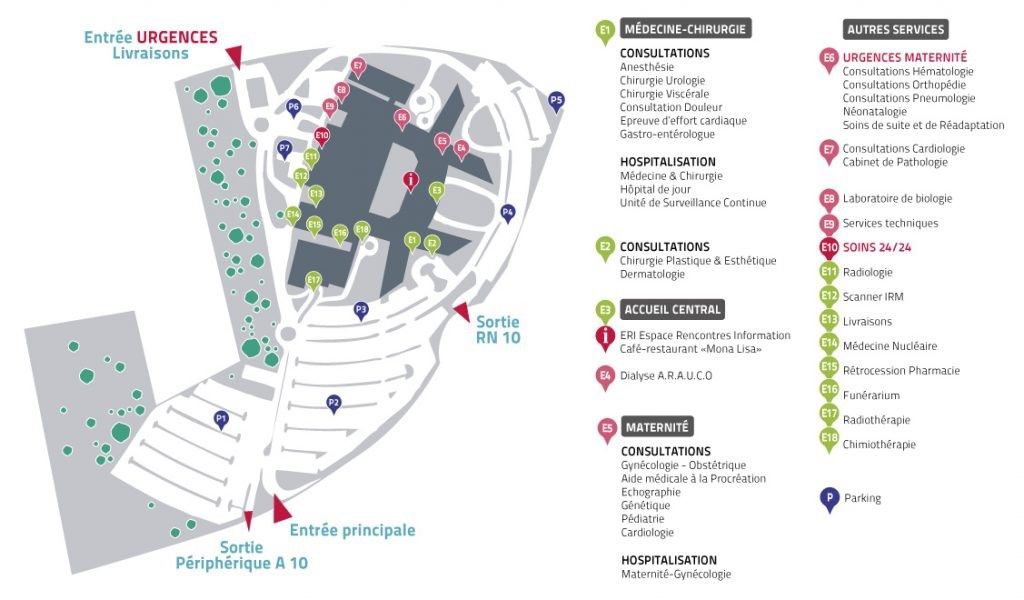
Le PSLV a son équipe technique composée de techniciens de tous horizons. Celle-ci, sous la gérance d’une ingénieure biomédicale, intervient uniquement pour le groupement de service rattaché au PSLV (bloc opératoire, cardiologie, urgences, soins de suite…). Les maintenances et contrôle sont pour la majorité externalisés. Les techniciens interviennent pour les pannes de moindre gravité mais également pour les problèmes autres que ceux liés au dispositifs médicaux. L’ingénieure biomédicale a mis en place un système de GMAO pour le suivi des pannes et des interventions des techniciens. Elle intervient surtout pour toute la gestion d’achat et les programmations d’interventions.
Bien qu’il y soit rattaché géographiquement, le centre de radiothérapie d’Indre-et-Loire (CORT37), ne fait pas partie administrativement du PSLV mais travaille avec les autres pôles afin de garantir le traitement le plus adapté aux patients.
2. Histoire du CORT37 et évolution
Installé depuis 2007 sur le site du pôle santé Tours Sud, le CORT37 (Figure 3) était avant cela situé à la clinique Fleming à Tours (Figure 4). La volonté de changer de site s’est faite avec la construction du PSLV et l’envie des radiothérapeutes de faire évoluer leur service. En changeant de lieu, ils ont pu devenir propriétaires des locaux, doubler leur effectif et mettre en place de nouvelles techniques liées au nouveau parc de dispositifs médicaux (scanner dédié à la dosimétrie, accélérateurs linéaires…) mais aussi grâce à la proximité avec d’autres services (médecine nucléaire, radiologie…).
Figure 3 : Photo du CORT37

Figure 4 : Photo de Flemming

3. Organisation du service
Le service est composé de plusieurs pôles(Figure 5), le pôle comptabilité et RH composé de 4 personnes dont l’une d’elle est la responsable du pôle, le pôle secrétaires divisé en deux, les secrétaires d’accueil et les secrétaires médicales qui sont sous la gérance d’une responsable de pôle, la responsable qualité sous le direction d’un médecin, la responsable communication également sous la direction d’un autre médecin.
Figure 5 : Organisation du service de radiothérapie
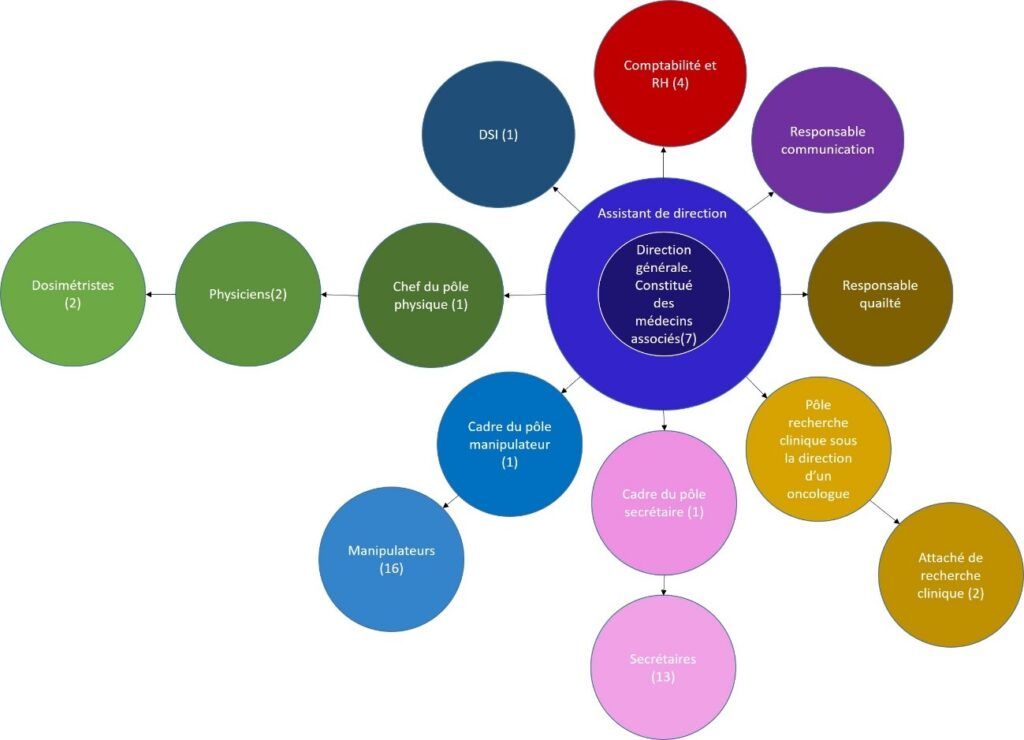
Il y a ensuite le pôle manipulateur de radiothérapie, managé par un cadre de santé, qui s’occupe des scanners de radiothérapie mais également des traitements de radiothérapie et de curiethérapie[2]. Les manipulateurs sont deux par poste pour les traitements, ce qui est réglementaire, pour une surveillance plus accrue.
Il y a également le pôle physique qui gère la partie technique du service. Ce pôle se divise en deux, les physiciens médicaux sont garants de la dose [2] et s’occupent de la partie technique du centre (maintenance, contrôle qualité…) [3] et les techniciens en planification de traitement qui veillent à la bonne planification des traitements et qui sont formés en partie au contrôle qualité des appareils[4]. Les maintenances étant externalisées, un suivi est réalisé mais personne n’est formé pour l’intervention des dispositifs médicaux.
Le pôle informatique est un pôle essentiel au bon fonctionnement du service. Le précédent informaticien étant parti au moment de mon arrivée le nouvel informaticien met en place de nouveaux protocoles pour la gestion des données.
Il y a également un pôle recherche qui est sous la gérance d’un oncologue et qui est composé d’une attachée de recherche clinique qui sera rejoint dans quelques mois par une collaboratrice. Ce pôle ne fait pas partie du CORT37 mais le ROC37 en est une sous entité.
Le CORT37 est certifié ISO 9001 : 2015 [5]. Pour le moment seul la partie radiothérapie est certifiée, c’est-à-dire que le centre n’est pas ISO 9001 pour la curiethérapie, ni pour la chimiothérapie, de même pour le ROC37. La qualiticienne souhaite faire certifier le ROC37 en juin 2023, au moment du premier suivi. Pour le moment seul le paragraphe 8.3 apportant des informations sur la recherche clinique n’est pas validé et avec le changement de qualiticienne, le temps pour travailler sur cette partie était trop court. La chimiothérapie et la curiethérapie seront quant à eux certifiés au deuxième suivi. L’objectif de la politique qualité au CORT37 est de continuer à avoir un système qualité efficace et de le rendre plus efficient grâce à de nouveaux outils, des plans d’actions managés et en allégeant le système documentaire[6].
Chaque pôle est sous la responsabilité d’un binôme de médecins, ce qui permet un échange permanent entre les différents pôles et la direction. De plus, des réunions techniques sont réalisées régulièrement pour avancer sur les différents projets et discuter des possibles difficultés qui peuvent être rencontrés quotidiennement. De par la complexité technique du parc d’équipement, ces réunions techniques permettent à la direction d’avoir les informations nécessaires sur le bon fonctionnement du parc de dispositif médicaux.
De par le fait d’avoir plusieurs intervenants en fonction des actions à mener, il est essentiel de centraliser les informations. Ceci peut rapidement devenir compliqué lorsqu’une personne est absente. Pour cette raison une réflexion sur la mise en place d’une GMAO est en cours et sera développer dans la partie III-2 du rapport.
4. Locaux et radioprotection
a. Les locaux
Figure 7 : Plan du rez de chaussé
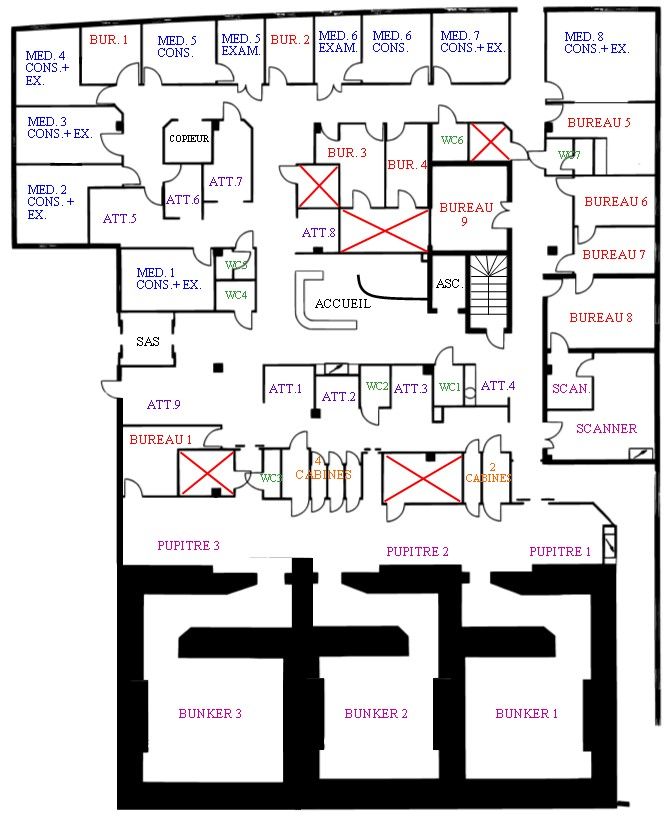
Figure 7 : Plan du rez de jardin
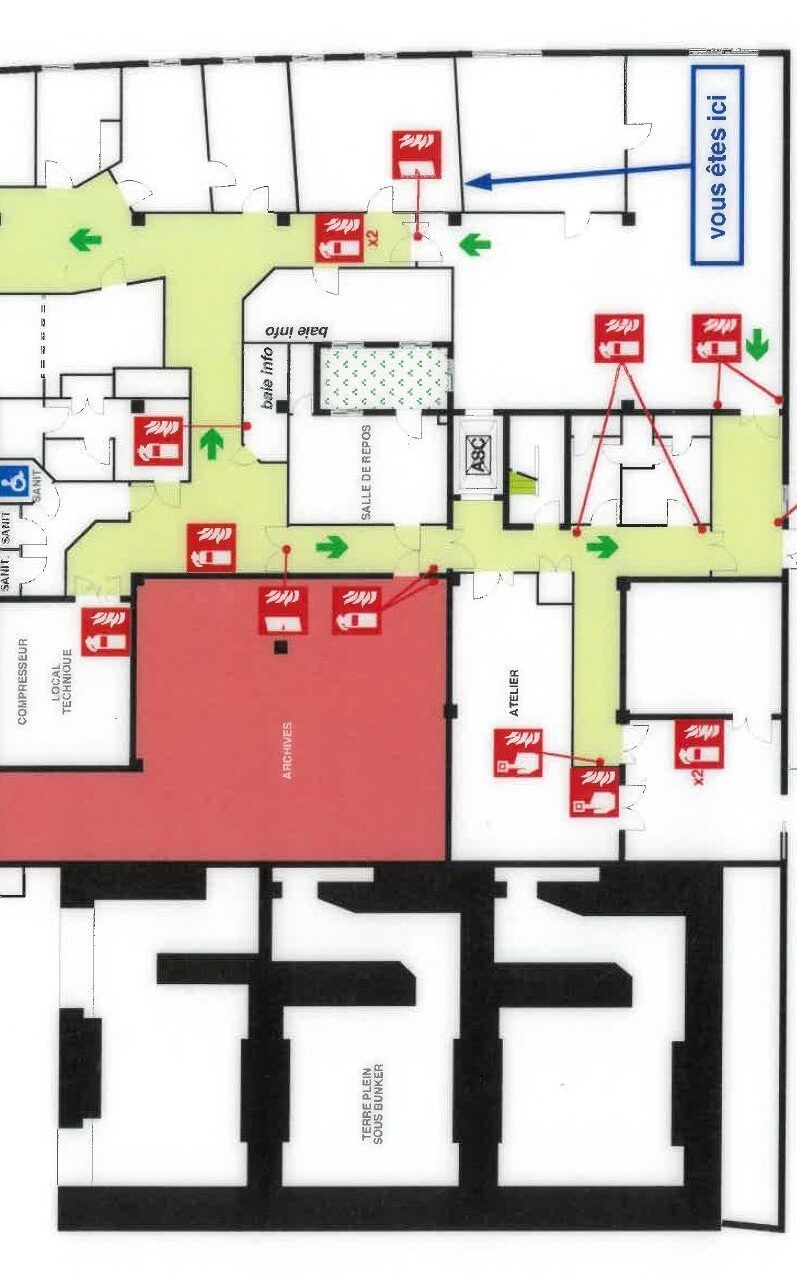
Pour accueillir les patients et offrir un cadre de travail optimal à ses salariés, le CORT37 est construit sur deux étages (Figure 7). Un rez-de-jardin constitué de salles de réunions, d’archives et de bureaux pour le personnel administratif. Le rez-de-chaussée est lui constitué de 3 bunkers, des bureaux de consultations des médecins et de l’infirmière en pratique avancée, des bureaux des physiciens, de la salle de scanner, de deux salles de dosimétrie, d’un local technique pour les pièces des machines ainsi que pour l’entreposage des fantômes utiles au contrôle qualité.
b. Les bunkers
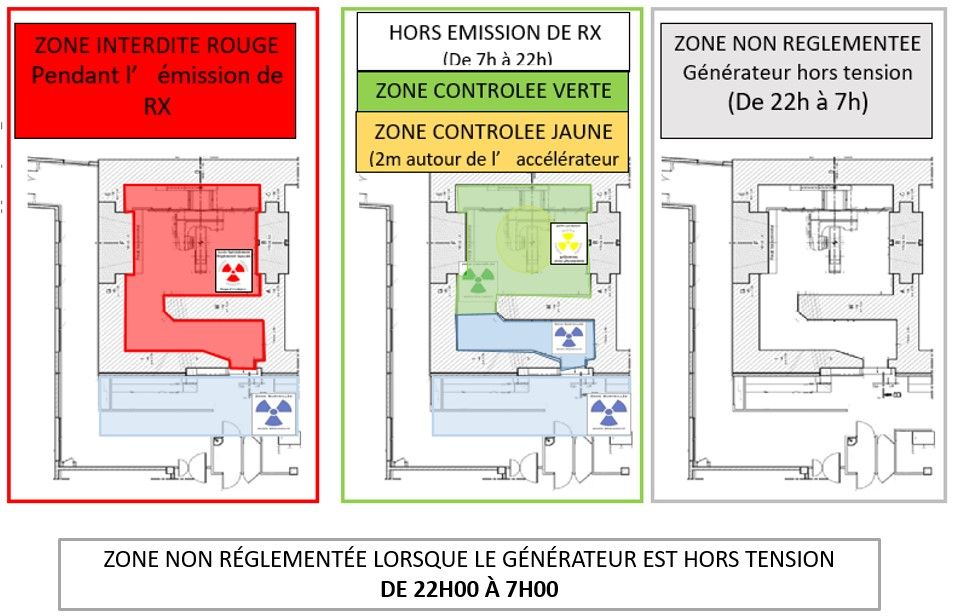
Les bunkers accueillent les accélérateurs de particules dédiés aux traitements de radiothérapie ainsi que le projecteur de source radioactive dédié à la curiethérapie. Il est essentiel, pour limiter les risques d’exposition du personnel soignant et du public, que les machines de radiothérapie soient installées dans des bunkers garantissant des exigences liées aux expositions. En effet les bunkers ont un rôle de protection des personnes à l’extérieur de celui-ci contre les rayonnements émis. Ce sont les conseiller en radioprotection (CRP) qui ont réalisés des calculs avant la construction des bunkers afin de savoir quelle épaisseur de mur est nécessaire, le type de porte, les matériaux utilisés et la dimension de la chicane. Tous ces facteurs vont permettre de délimiter les zones réglementées(Figure 8)[7].
Figure 8 : Zonage des bunkers en radiothérapie
5. Les dispositifs de traitement disponibles au CORT37
Lorsque le bunker est fini de construire et répond aux exigences en rigueur, la machine est livrée et installée. Les techniciens de la société du constructeur Varian ont monté et réglé l’appareil. C’est ensuite l’équipe de physique du centre qui s’est assuré que l’installation du dispositif répondait au cahier des charges, il s’agit de l’acceptance. Puis ils vont réaliser le commisioning de la machine, qui dure plusieurs semaines, étape consistant en une série d’étalonnages et de mesures de l’accélérateur. Les mesures validées sont ensuite transférées dans le Treatment Planning System (TPS) pour la modélisation des caractéristiques dosimétrique de l’accélérateur. Au CORT37, il a été fait le choix d’avoir les mêmes réglages sur les 3 machines pour réaliser des traitements identiques sur chaque machine. Cela va permettre de traiter un patient sur une autre machine lorsque celle-ci est en panne et facilite grandement l’organisation de prise en charge des patients.
a. Accélérateurs de particules
Pour délivrer les traitements le CORT37 est équipé de 3 accélérateurs linéaire dont un Clinac® 2100C sans l’option RapidArc® et sans CBCT, d’un Clinac® 2100C avec les options RapidArc®, d’un CBCT et d’un Truebeam® avec les options citées ci-dessus, ainsi que d’une table 6D, et enfin d’un système de suivi respiratoire impliquant la possibilité de faire des traitements de stéréotaxie mobile.
Le principe de ces accélérateurs est le suivant :
Un faisceau d’électrons haute énergie est créé en appliquant un courant à un filament de tungstène qui sont ensuite soumis à un champ magnétique, créé par un Klystron, pour les accélérer et les focaliser à travers la section accélératrice. Le faisceau est ensuite harmonisé à travers la tête de déviation qui va permettre le tri des électrons de différentes énergies mais également de focaliser davantage le faisceau. Il est ensuite possible d’obtenir des photons. Pour cela une cible métallique vient se placer à la sortie de la tête de déviation. Les électrons vont alors interagir avec cette cible et permettre l’obtention de photons par l’effet de Bremsstrahlung. Le faisceau passe ensuite par un collimateur primaire permettant de le former. Deux chambres d’ionisation vont permettre le contrôle de l’homogénéité et de la dose de ce faisceau. Des cônes égalisateurs sont ensuite présent de manière à redresser le faisceau et que l’énergie soit la même sur la quasi-totalité du champ formé. La forme du champ final est rendue possible par le collimateur composé de 4 mâchoires et d’un collimateur multi-lames composés de 120 lames indépendantes (Figure 9)[1].
Figure 9 : Schéma d'un accélérateur de particules de la marque Varian

Des options liées à l’accélérateur sont également présentes comme l’imageur portale qui va permettre d’avoir une validation du positionnement et de la dose, un imageur embarqué kV qui va permettre un contrôle du positionnement mais aussi un recalage entre le scanner de dosimétrie et l’imagerie du jour, la table 6D qui va permettre un repositionnement plus précis du patient. Nous retrouvons également des lasers modélisant l’isocentre de la machine dans chaque bunker. En plus de ces options le même matériel de contention se trouve dans chaque salle de traitement. Elles vont permettre de repositionner les patients à l’identique à chaque séance.
Le centre réalise environ 1100 traitements de radiothérapie externe. Chaque traitement varie en fonction de la localisation, ce qui entraine un nombre plus ou moins élevée de séance pour le patient.
Le nombre de paramètres pouvant influer sur le bon traitement des patients, étant important cela nécessite des obligations de maintenance et contrôles. Les accélérateurs linéaires sont donc soumis à des obligations de maintenance répondant aux recommandations du constructeur, ici Varian. Les contrôles qualité sont eux sous la responsabilité des physiciens médicaux. Ils ont une obligation nationale pour garantir le bon fonctionnement, la performance de la machine mais également la qualité de la dose délivrée par ces dispositifs [8].
b. Le scanner
Pour permettre le traitement du patient, il faut au préalable une imagerie scanner. Pour cela le centre est équipé d’un scanner GE medicals systems, OPTIMA CT 580 ( Figure 10).
Les imageries scanner réalisées auront un intérêt majeur dans le traitement du patient, puisqu’elles permettront d’avoir une référence sur le positionnement du patient pour chaque séance. Nous verrons dans la suite de ce rapport, l’importance de l’imagerie pour le bon déroulement du traitement du patient.
Figure 10 : Photo du Scanner GE du CORT37
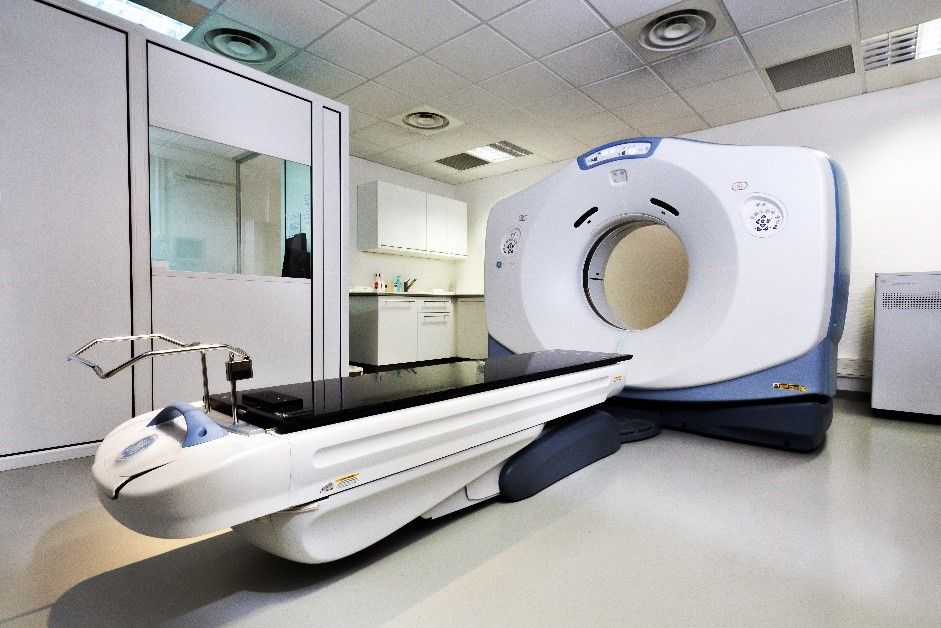
Le scanner est lui aussi soumis à des contrôles réglementaires pour assurer son bon fonctionnement et la qualité de l’imagerie. Des CQ pour les artefacts, le nombre d’unités Hounsfield (UH), le bruit et l’homogénéité de l’image sont réalisés en interne par un physicien en quadrimestriel et des CQE sont réalisés en annuel suivant la décision du ministère de la santé, de la jeunesse et des sports du 22 novembre 2007 fixant les modalités du contrôle qualité des scanographes.
c. La curiethérapie
Une autre technique de traitement est également proposée au CORT37, il s’agit de la curiethérapie(Figure 11).
Figure 11 : Photo de l'appareil de curiethérapie

Le principe de cet appareil de traitement est d’utiliser un applicateur qui viendra au contact de la tumeur pour délivrer une forte dose a celle-ci via une source radioactive mobile qui se déplacera à travers différents canaux. Il sera abordé dans la partie III-1, l’application de la curiethérapie et comment il est possible d’améliorer la pratique liée à la pose des applicateurs.
Pour cet équipement des CQ sont également effectué et cela avant chaque séance de manière à vérifier que la source est encore présente, qu’elle passe bien dans les canaux sans blocage (via le contrôle avec une source fictive) et qu’elle s’arrête bien au bon endroit(Figure 12). Il n’y a pas d’obligations réglementaire, l’ASN préconise de suivre les recommandations du fabricant. Tous les an un contrôle de la mesure l’activité de la source est réalisé, et tous les 6 mois le contrôle de l’intégrité des guides, des applicateurs…
Figure 12 :Contrôle des temps d'arrêt à différentes distances

Le CORT37 réalise une vingtaine de traitement par an de curiethérapie. Ce chiffre varie en fonction des patients adressés et de la possibilité ou non de réaliser une curiethérapie plutôt qu’un traitement de radiothérapie externe.
6. Développement du centre
Dans un souci de modernisation du parc d’équipement, le CORT37 a acheté un nouveau Truebeam (Figure 13) pour remplacer le Clinac1 dans le but de pouvoir traiter la majorité des patients en RapidArc. Une autre machine est commandée, un Halcyon(Figure 13) qui permettrait de mettre en place de nouvelles techniques de traitement. De par son design plus proche de celle du scanner, le dispositif parait moins impressionnant pour le patient. De plus avec une seule énergie (6MV FFF) avec un débit de délivrance de la dose plus élevé, son collimateur mutilames composé de 2 rangés superposées de lames, son système d’imagerie embarquée et sa vitesse de rotation, l’Halcyon permet des traitements plus rapide et plus précis [9]. Du fait d’une ergonomie différente l’Halcyon demande certaines adaptations du matériel pour le traitement du patient, nous verrons par la suite une adaptation possible pour le positionnement des patients dans l’anneau.
Figure 13 : Photo d’un Truebeam
Figure 13 : Image d’un Halcyon (d'après le site web Varian.com)
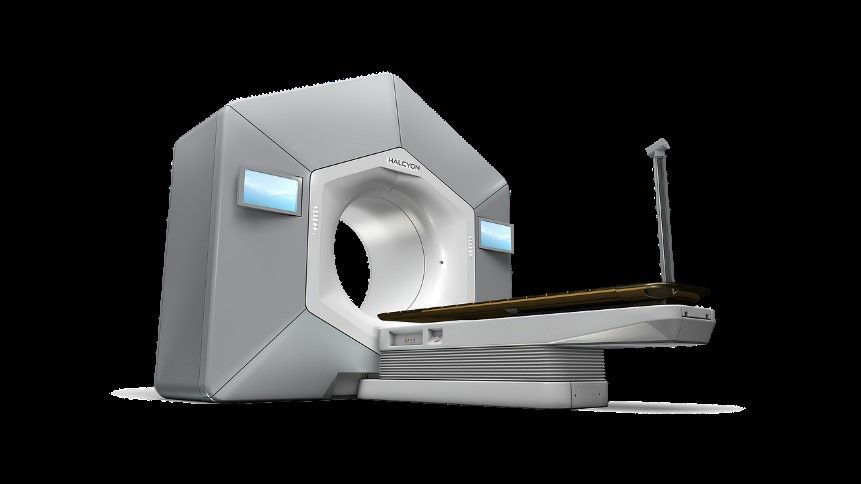
Pour cette raison un projet d’extension à vue le jour il y a maintenant quelques années. Cependant celui-ci est resté un moment en stand-by de par les questions de politiques entre le CORT37 et le PSLV mais aussi la crise COVID et les délais des matières premières. Ces différentes problématiques ont ralenti certains projets comme celui de la mise en place d’un système pour traiter les patientes atteintes d’un cancer du sein en inspiration bloquée.
Le scanner du centre devait également être renouvelé, après discussions avec différents fournisseurs il a été choisi de garder le scanner actuel mais de l’upgrader de façon à pouvoir s’astreindre des artefacts de prothèse et d’avoir des outils de reconstruction permettant d’obtenir une imagerie de meilleure qualité. Ce choix a été fait de manière à avoir de meilleur traitement pour le patient grâce à une résolution plus importante de l’image mais aussi en diminuant la dose délivrée au patient. Une bonne qualité d’image permet une délinéation des volumes cibles plus précis.
Pour la plupart des choix techniques, un groupe de travail est créé, composé des acteurs nécessaires à la réussite du projet. Plusieurs fournisseurs sont alors contactés pour avoir des démonstrations et ainsi pouvoir choisir le dispositif qui conviendrait le mieux. Une fois le choix fait, une réunion avec la direction est organisée pour acter ou non la décision finale.
Ces différents points de développement du CORT37 n’ont pour but que l’amélioration de la prise en charge des patients. En effet, la mise en place de nouveaux matériels va permettre l’intégration de nouvelles techniques favorisant des traitements plus personnalisés et permettant d’améliorer le contrôle local de la maladie tout en diminuant les toxicités. Le CORT37 est donc dans une optique d’amélioration de sa pratique en faveur de l’optimisation de la prise en charge des patients en proposant les solutions les plus adaptées.
7. Parcours du patient
Le parcours de prise en charge du patient au CORT37 se déroule de la façon suivante (Figure 14) :
Figure 14 : Parcours du patient en radiothérapie
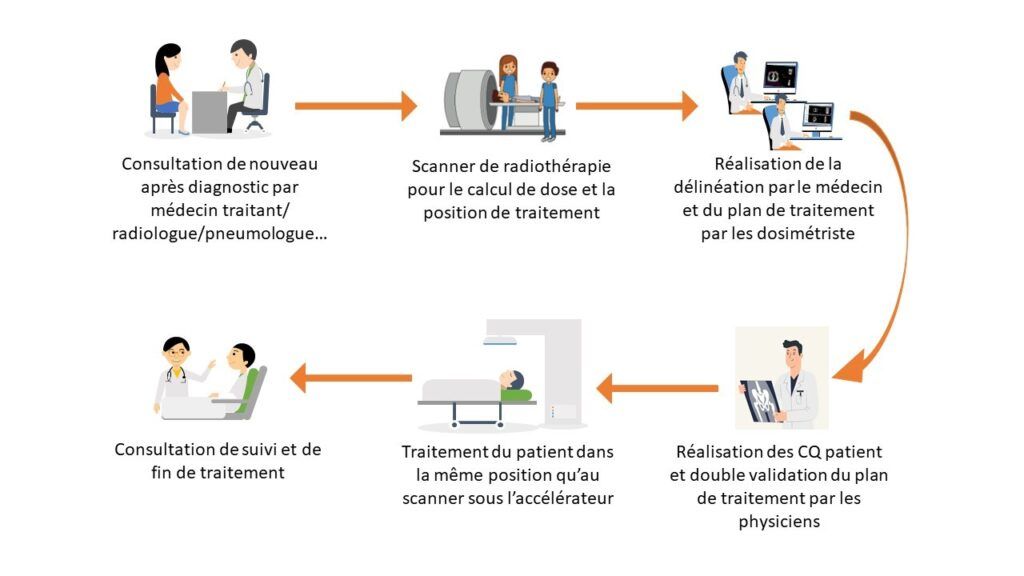
Les patients sont adressés aux radiothérapeutes par leur médecin traitant ou par décision de STAFF (réunion médicale destinée à l'étude des dossiers de patients en cours de prise en charge) une fois un diagnostic établi à partir d’imagerie radiologique, de bilan sanguin… A la suite de cette décision, le patient rencontre le radiothérapeute en consultation. Des informations le concernant sont relevées tels que les antécédents de maladies, les antécédents familiaux, l’âge, l’adresse du domicile, … Il sera fourni au patient des informations sur le déroulement de son traitement ainsi que sur sa maladie. Après la première consultation, le radiothérapeute crée un protocole de traitement contenant les doses prescrites, les antécédents de radiothérapie, la localisation, s’il s’agit d’une chimiothérapie concomitante, la présence d’un défibrillateur ou pacemaker (appareils pouvant être déréglés à cause des neutrons).
Un rendez-vous pour la semaine suivante au scanner de dosimétrie, est donné au patient. Au moment du scanner, les Manipulateur d'Électroradiologie Médicale(MERM) vont donner aux patients des informations sur le régime alimentaire à suivre ainsi que sur les produits d’hygiènes à proscrire le temps de la radiothérapie. A cette étape, les MERM vont utiliser des contentions adaptées à la morphologie du patient pour permettre un repositionnement précis pour les séances de traitement. Des points de tatouages sont réalisés pour modéliser le zéro permettant de positionner le patient sous la machine à l’aide des lasers présent en salle (Figure 15). Cet isocentre correspond à l’intersection entre l’axe des faisceaux et l’axe de rotation de la machine de traitement.
Figure 15 : Points de tatouage et laser. Des outils utiles en radiothérapie au positionnement du patient
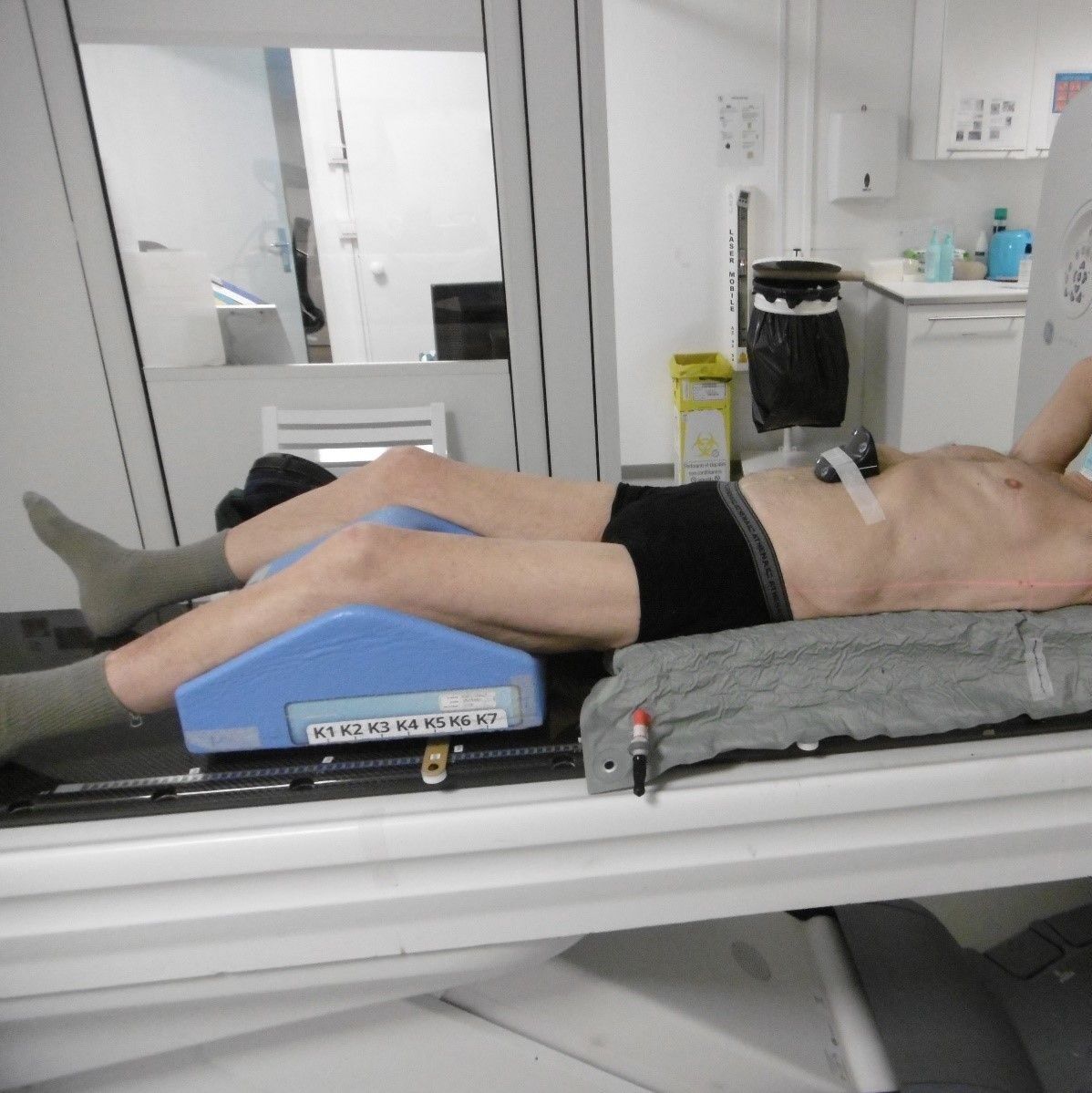
Une fois le scanner acquis avec les constantes optimales, pour une bonne résolution d’image mais aussi l’optimisation de la dose au patient, les images sont envoyées sur le logiciel ARIA de Varian. Le MERM pourra faire les recalages avec l’imagerie diagnostique (IRM, TEP, TDM) sur la zone à traiter [10].
A la suite de ces recalages, le médecin va délinéer les volumes cibles ainsi que les organes à risques (OAR) en regard de la zone à traiter (Figure 16).
Figure 16 : Délinéation des volumes cibles et des OAR par le médecin
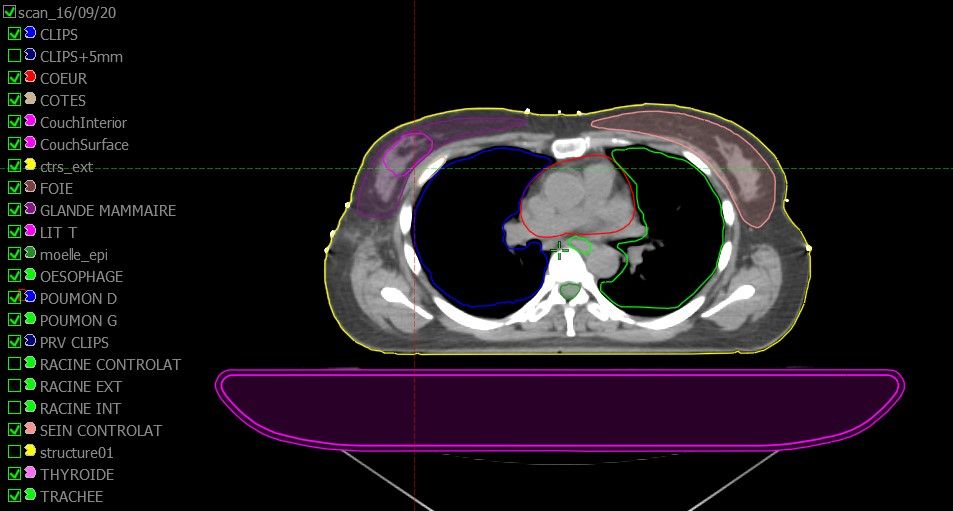
Les techniciens en planification vont alors optimiser la distribution de dose, via le logiciel Eclipse de Varian, sur les volumes cibles. Les volumes cibles recevront la dose prescrite par le radiothérapeute et il faudra optimiser les doses aux OAR sans dépasser les doses inscrites dans les recommandations. Une fois la dosimétrie achevée, le radiothérapeute valide le dossier si celui-ci répond à ses exigences[11] [12].
Lorsque la dosimétrie est validée par le médecin, le physicien médical réalise des contrôles qualité (CQ) patients directement sur l’accélérateur, afin de valider que le plan calculé sur le TPS est proche de ce qui est délivré par la machine selon certains indices de conformité (Figure 16). Le physicien médical est garant de la dose [13]. Si tous les contrôles sont bons et que le plan répond aux exigences, le physicien validera le plan et l’enverra au traitement pour pouvoir traiter le patient [14] .
Environ une semaine après le scanner le patient commencera son traitement par une séance blanche où uniquement des images de contrôles sont réalisées pour valider sa mise en place et constater s’il y a des modifications. Le nombre de séances de traitement varie en fonction de la localisation ; pour le cancer du sein il y 28 séances, pour le cancer de la prostate 37 séances, pour le cancer ORL 33 séances, les métastases sont traitées en 10 à 15 séances suivant l’avis du médecin en normo fractionné ce qui correspond à 2Gy par séance avec une séance par jour sans interruption. Il y a ensuite les traitements en stéréotaxie qui varie en fonction de la localisation entre et 4 et 10 séances avec une séance un jour sur deux. Ce traitement consiste à délivrer de forte dose en peu de séance dans de petit volumes cibles. Il faut donc pour cette technique une grande précision dans la délivrance du traitement (Figure 17).
Figure 17 : Traitement de stéréotaxie
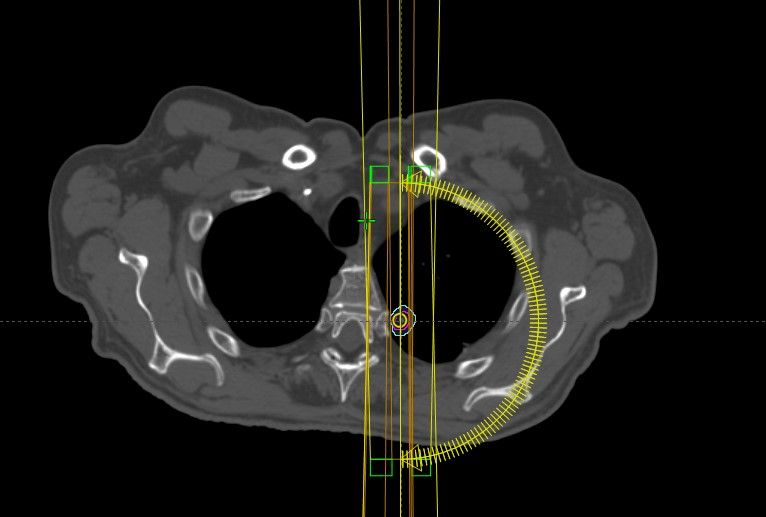
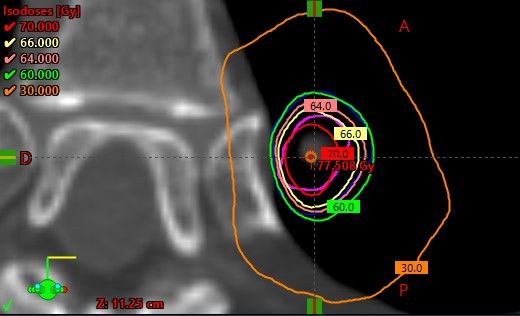
A chaque séance, pour délivrer la dose au bon endroit avec précision, de l’imagerie de positionnement est réalisée(Figure 18) [15].
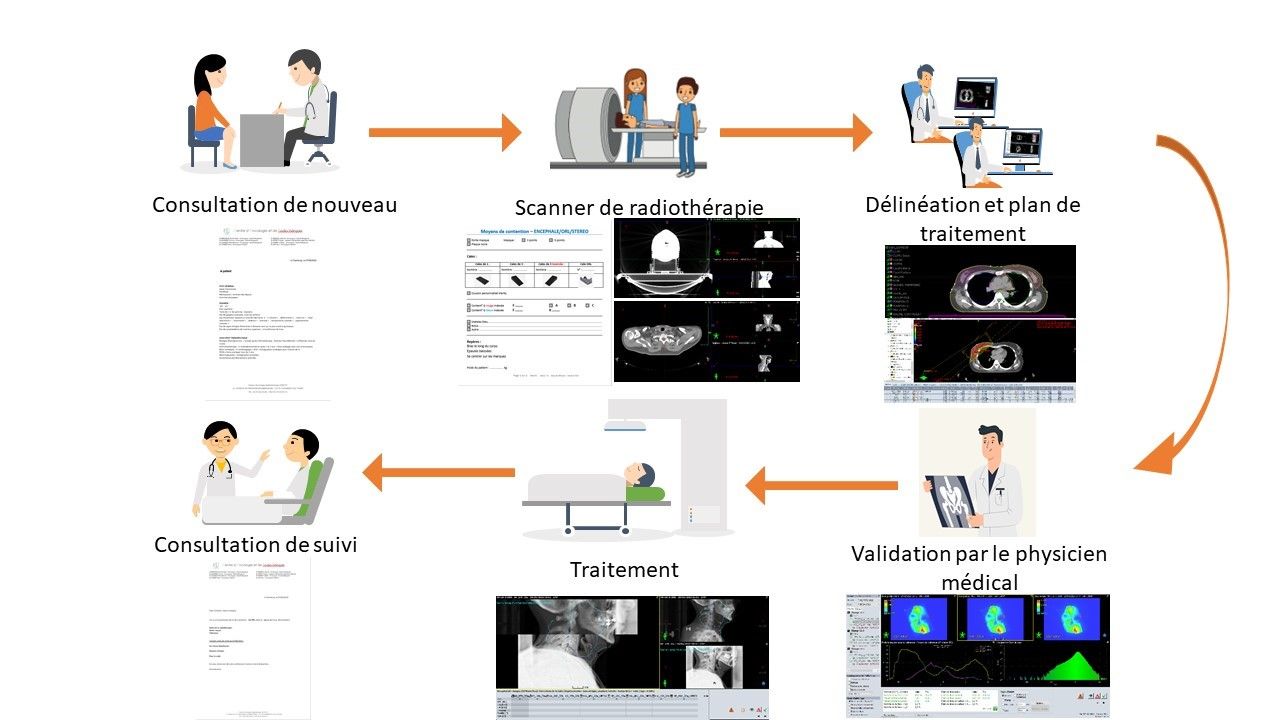
Durant le traitement, les patients voient les radiothérapeute ou l’IPA en consultation de suivi pour suivre l’avancement du traitement et prévoir des adaptations en cas de problème de santé. A la fin du traitement, une consultation de fin de traitement est programmée ainsi que des consultations de suivies à 6mois ou 1 an, afin de suivre l’évolution de la maladie dans le temps.
Figure 18 : Les différentes étapes du dossier patient en radiothérapie
II. Mission principale d’ingénieur biomédical durant le stage : intégration d’un nouveau dispositif médical pour le repositionnement surfacique
1. Contexte et enjeux de la radiothérapie
a. Cycle cellulaire
Les avancées technologiques entrainent des évolutions pour les traitements qui permettent de délivrer des séances de radiothérapie plus précises aux patients avec un contrôle local de la maladie plus important. Ces évolutions s’accompagnent d’un souhait d’améliorer les traitements en augmentant les doses aux volumes cibles tout en diminuant les doses aux OAR. Pour bien comprendre l’intérêt d’augmenter les doses il est important de comprendre le fonctionnement des rayons ionisants sur les cellules (Figure 19).
Figure 19 : Schéma de l'effet radio biologique des rayons X sur les cellules
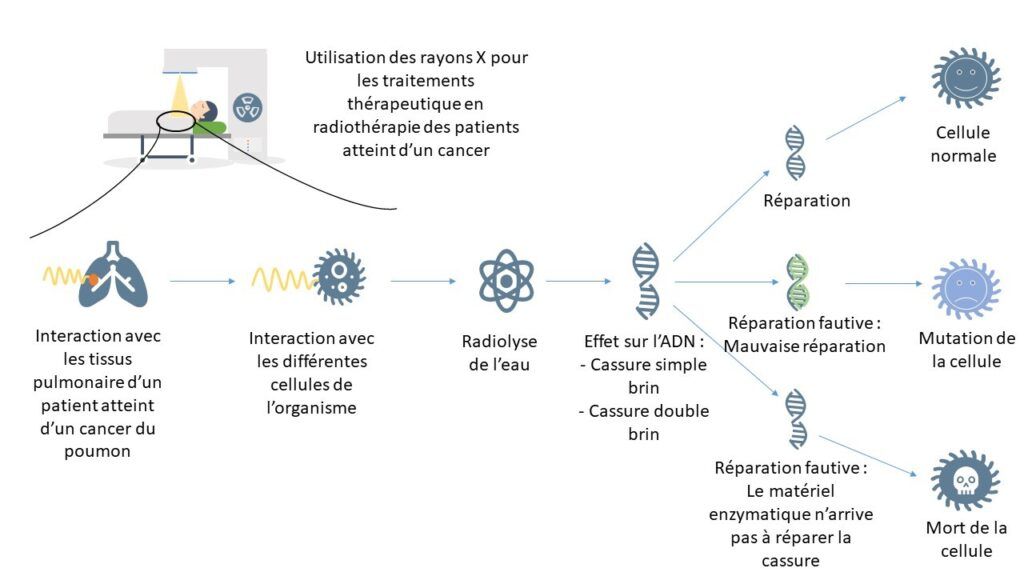
La radiothérapie permet de traiter des tumeurs cancéreuses grâce aux rayons ionisants. Pour délivrer ces rayons, il est utilisé des faisceaux de particules créés par des accélérateurs de particule. Les interactions avec la matière vont permettre la rupture de molécules d’ADN des noyaux cellulaire. Plus la dose est élevée, plus l’effet sera important sur les cellules cancéreuses. Dans une certaine limite, c’est le matériel enzymatique qui va réparer ces ruptures. Cependant, lorsque les ruptures sont trop importantes pour être réparées, les cellules sont vouées à mourir. Les conséquences sur les cellules sont dû au seuil de dose. On parle d’effet déterministe pour les effets se produisant à un certain seuil de dose et d’effet stochastique(aléatoire) qui dans ce cas peuvent intervenir peu importe la dose. Les organes plus sensibles aux doses sont les organes avec des cellules à division rapide (moelle osseuse, gonades…). Les cellules cancéreuses ayant un cycle de division rapide, celles-ci sont donc plus sensible aux rayons, d’où l’utilisation de protocole de dose en fonction du cancer.
Néanmoins, le fait d’augmenter la dose pour avoir plus d’effet sur les cellules cancéreuses peut entrainer des complications sur les OAR. Il est donc intéressant d’augmenter le nombre de séances avec une dose de 2Gy par séance pour avoir un impact sur les cellules cancéreuses tout en minimisant les effets sur les cellules saines. Il s’agit alors d’un traitement normofractionné.
b. La dosimétrie
Sur le scanner de dosimétrie, les volumes cibles sont délinéés par les médecins avec des marges prenant en compte le repositionnement, les mouvements interne du volume et les modifications morphologiques. Ces volumes répondent aux recommandations en rigueur. Les volumes cibles sont délinéés par le radiothérapeute sont : le GTV qui est le volume tumoral macroscopique, le CTV qui est le volume clinique comprenant le GTV et les extensions non visibles sur l’imagerie, l’ITV qui correspond à l’ensemble des GTV durant un cycle respiratoire et enfin le PTV qui intègre les incertitudes de positionnement, de mouvements du patient ou des volumes durant le traitement (Figure 20) [11] [12] [16]. Les marges CTV vers PTV allant jusqu’à 7mm au maximum au CORT37, il est important d’avoir un positionnement optimal pour le patient. Chaque année, les marges sont revues à la baisse de par la précision des accélérateurs mais aussi pour prendre en compte les effets radio biologique des tissus.
Figure 20 : Schéma des volumes cibles en radiothérapie
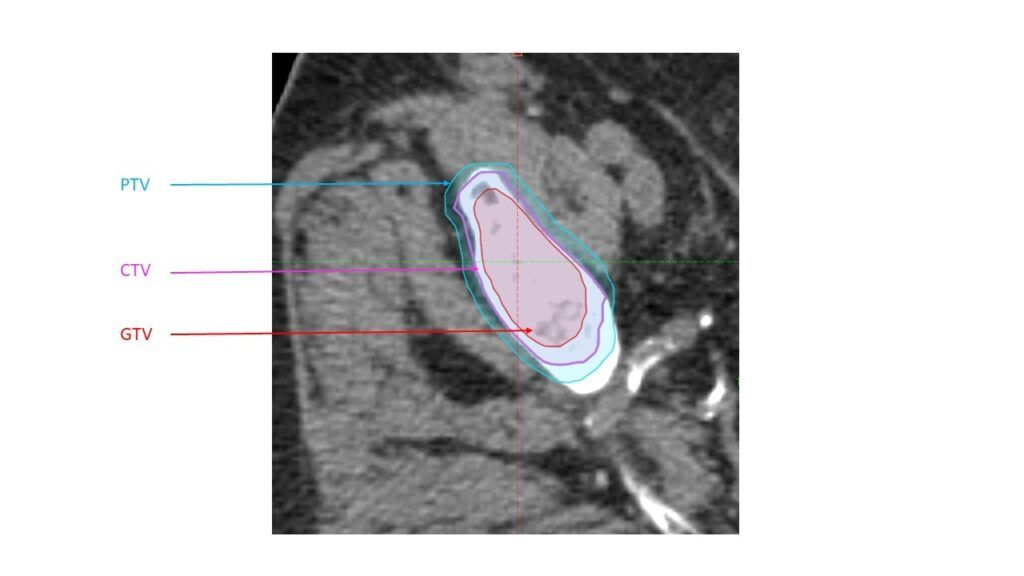
A la suite de cette délinéation, une dosimétrie est réalisée avec des gradients de doses permettant de délivrer la dose dans la tumeur tout en épargnant les OAR. De par la complexité des dosimétries dû à la technique et aux contours du médecin, il est important que le patient soit le plus proche possible de la position du scanner initial. Les techniciens de planification vont, à partir de ce scanner, optimiser les doses aux volumes cibles et OAR selon les contraintes SFRO et la prescription médicale. Pour cette optimisation plusieurs techniques sont disponibles.
c. Technique de traitement
Le choix de la technique se fait en fonction des nécessités d’optimisation. Il est possible de faire un traitement en :
- Radiothérapie conformationnelle 3D, qui consiste en l’utilisation de faisceaux d’irradiations fixe conformés au volume cible(Figure 20) [17].
- Radiothérapie conformationelle avec modulation d’intensité (RCMI) qui se base sur des faisceaux d’irradiations fixe avec modulation de la fluence pendant la séance. Le déplacement des lames et l’adaptation du débit de dose simultanément durant l’irradiation va permettre de conformer les isodoses au volume cible en créant des gradients de dose [17].
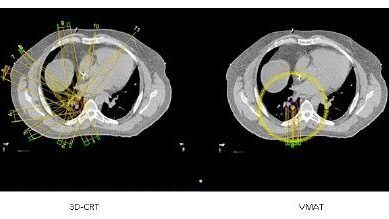
- Radiothérapie conformationelle avec modulation d’intensité en VMAT ou le bras de l’accélérateur est en rotation pendant l’irradiation. Cela permet de multiplier le nombre de faisceaux et ainsi les portes d’entrées. Ce qui amènera une plus grande épargne des OAR mais en contrepartie à une augmentation des faibles doses(Figure 21) [18].
- Stéréotaxie est une technique de traitement qui permet d’augmenter considérablement la dose prescrite par séance tout en épargnant les OAR. Pour ce traitement, des volumes plus petits qu’en radiothérapie normo fractionné sont traités [19].
Figure 21 : Technique de traitement en radiothérapie
2. Les problématiques du repositionnement du patient en radiothérapie
Les techniques de traitement en radiothérapie demandent une grande précision de positionnement. En effet, avec le développement des techniques en modulation d’intensité, les marges ont été diminuées dû à la précision de couverture des volumes cibles. Ainsi, les médecins souhaitent réduire les doses aux OAR tout en augmentant les doses dans les volumes cibles. Il est donc essentiel d’avoir un positionnement quotidien du patient très précis [20].
Comme nous avons pu le constater dans la partie I-7, le manipulateur doit assurer un positionnement du patient identique à celui du scanner de simulation/dosimétrie, à chaque séance de traitement. Le repositionnement du patient à chaque séance est un facteur important au bon déroulement du traitement. Cependant celui-ci est compliqué de par la complexité de mettre un patient dans la même position durant presque un mois et ceci chaque jour. A cette fin, les MERM utilisent plusieurs moyens : les contentions servant au maintien du patient, les lasers et les points de tatouage (réalisés au scanner) servant à l’alignement du patient. Cependant, cette technique à ses limites car les points de tatouages peuvent être bougés en déplaçant la peau sans déplacer le patient, ce qui peut engendrer un positionnement non reproductible malgré un système de contention fixe. En effet, les tatouages sur la peau du patient peuvent être décalés, ce qui entraine un mauvais positionnement du patient tout en étant sur les points [21]. La peau étant une surface pouvant être déplacer sans correspondance avec l’intérieur du patient, des repères cutanés ne sont pas forcément en adéquations avec le positionnement osseux ou des tissus mous internes. De plus, le fait de se contenter de 3 points ne permet pas forcément de repositionner le patient à l’identique de la position initiale. Les points de tatouages ont également un effet psychologique fort pour les patients, en effet ces points indélébiles peuvent rappeler de mauvais moment aux patients.
3. Etude de marché à partir des besoins relevés
Pour améliorer la reproductibilité du positionnement du patient à chaque séance de traitement, diminuer la dose au cœur et s’astreindre des problématiques liées au points de tatouages plusieurs solutions s’offraient au CORT37. Une étude de marché a alors été réalisé prenant en compte les différentes possibilités qui s’offraient.
a. Contentions
La première possibilité était de changer le parc de contention complètement. L’idée était donc de tester plusieurs fournisseurs de contentions (CIVCO, Meditest, Orfit, Meicen). Nous avons également contacté d’autres centres de radiothérapie afin d’avoir un retour sur les contentions qu’ils utilisaient. Après cette prospection, des contentions ont été choisies et des tests avec étude de repositionnement via l’imagerie embarquée ont été réalisés. Il a été testé le Sabella de Meditest et le Monarq de CIVCO (Figure 22) qui ont été comparé au matériel déjà en place.
Il en est ressorti que les contentions utilisées en routine étaient un peu moins performantes mais qu’elles induisaient moins d’erreurs de positionnement. Cela s’explique par le grand nombre d’accessoires disponibles et la multitude de réglages (support de bras, position des mains…) sur les contentions testées. Le système de contention déjà en place est satisfaisant mais vieillissant ce qui implique un renouvellement de ces contentions.
Figure 22 : Contentions testées au CORT37 (Sabella de Meditest et Monarq de Civco)


b. Repositionnement surfacique
La seconde solution était la possibilité d’utiliser un système d’optique permettant la reproductibilité du positionnement du patient mais également un suivi de la respiration durant le traitement (DIBH). Ce système repose sur le principe de stéréophotogrammétrie, qui grâce à des prises de vues stéréoscopiques permet la reconstruction précise de la surface. Il a été développé une technique appelé SGRT (Surface Guided RadioTherapy) qui va permettre, à partir de la reconstruction surfacique du contour externe du patient, obtenu au scanner de simulation, de repositionner le patient à chaque séance. Durant la séance, la position du patient acquise par les caméras est comparée en permanence avec la reconstruction surfacique des données DICOM du scanner de simulation. Le manipulateur a alors accès à un recalage entre ces deux positions en temps réel [22].
Le système offre également la possibilité d’une synchronisation respiratoire. Un retour visuel de l’amplitude respiratoire du patient permet de traiter les patients en inspiration bloqué, il s’agit du DIBH [23].
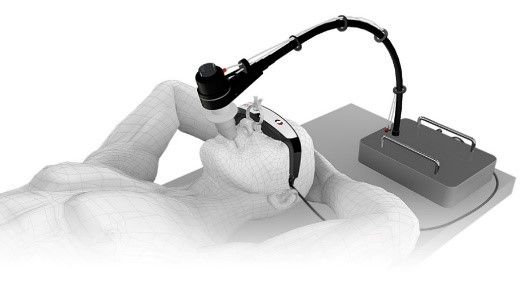
Pour la partie DIBH, une comparaison avec le spiromètre de la société Dyn’R (Figure23) a été étudié. Celui-ci permet une grande précision sur la phase respiratoire pour traiter les patients en inspiration bloqué [24].
Figure 23 : Spiromètre de la marque Dyn'R
Il existe différents fournisseurs dont les systèmes diffèrent, tels que :
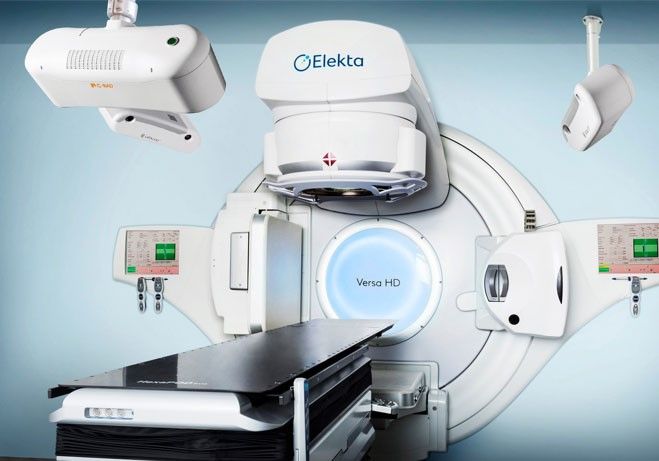
- VisionRT avec son système AlignRT (Figure 24) qui comporte 3 systèmes d’optiques, appelés pods, comportant chacun 2 caméras. Ce système repose sur des acquisitions stéréoscopiques et sur un projecteur de lumière rouge avec des formes géométriques particulières. La multiplication des optiques permet une reconstruction 3D du patient. Un algorithme de recalage rigide est utilisé pour déterminer les écarts entre la référence DICOM et la surface du patient en salle de traitement. AlignRT permet de synchroniser le traitement à la respiration avec un retour visuel au patient [25].
Figure 24 : Caméra de la marque VisionRT

Ce système est compatible avec les systèmes Varian puisqu’ils ont été en partenariat pendant Longtemps. Une centaine de systèmes sont implantés en France, ce qui a permis des visites et des retours d’expérience aisément. De plus, VisionRT est le seul fabricant permettant l’adaptabilité de son système sur les machines de traitement Halcyon. Il permet également des traitements synchronisés à la respiration
- C-RAD avec son système Catalyst (Figure 25) qui comporte jusqu’à 3 systèmes d’optiques contenant une caméra et un projecteur laser à triangulation optique. Ce système contrairement au système de VisionRT utilise un système de recalage non rigide qui permet de comparer la surface acquise avec la surface de référence. Il permet également des traitements synchronisés à la respiration. Le système est également composé d’un module permettant au patient d’avoir un retour visuel de son cycle respiratoire [25].
Figure 25 : Système surfacique de la marqueC-RAD
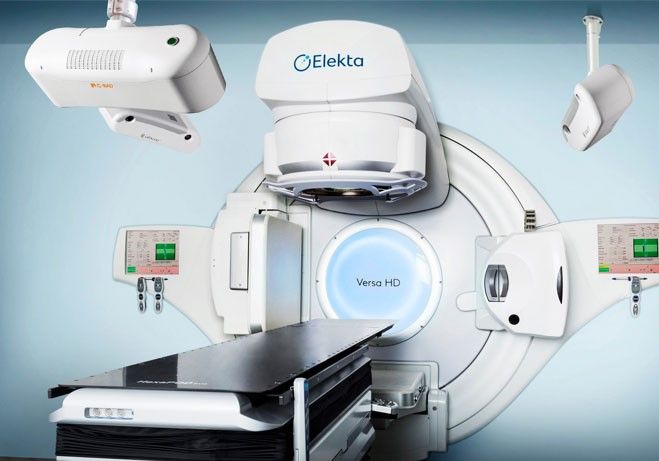
- Varian avec son système Identify (Figure 26) (anciennement Humediq). En plus de permettre le repositionnement du patient par un système d’optique, le système propose également de confirmer les contentions utilisées et leur emplacement avant la mise en place du patient sur la table par rapport à la configuration utilisée au scanner de simulation. Composé de 3 pods constituées de deux caméras et d’un projecteur, le système permet de vérifier les écarts de positionnement par acquisition stéréoscopique, avec une surveillance pendant le traitement. Il permet un arrêt du faisceau en cas de dépassement des tolérances. Ce système n’est malheureusement pas encore disponible par le fournisseur, un seul centre en France le possède et l’utilise comme centre de référence testeur.
Figure 26 : système surfacique de la marque Varian

- Brainlab avec son Exactrac Dynamic (Figure 27) qui est un système composé de capteurs plans pour l’imagerie kV et qui a développé sa solution proposant un système d’optique non irradiant. Il est composé de caméras, de projecteurs de motifs et d’un système de caméra thermique au pieds du patient. Ce système permet également un suivi respiratoire du patient.
Les bunkers n’étant pas équipé de capteurs plans et ayant déjà un système d’imagerie embarqué, le système de Brainlab aurait été redondant avec les équipements déjà présents sur les accélérateurs Clinac.
Figure 27 : Système surfacique de la marque Brainlab
Après cette prospection sur les différents systèmes cités, des déplacements dans des centres (Toulouse et Marseille) et à des congrès tels que la SFPM, l’ESTRO et la SFRO ont été fait. Il a donc été nécessaire par la suite de faire un retour aux équipes et à la direction tout en prospectant pour savoir ce qui serait le plus proche des attentes de chaque acteur du service.
4. Propositions et présentation à la direction et choix du système
Une première présentation a été faite lors d’une réunion, regroupant médecins, physiciens et cadre médicotechnique, pour présenter les différentes solutions à partir d’un cahier des charges comprenant les besoins de chaque acteur et les attentes de la direction. Une comparaison bibliographique entre le système de spiromètre et les systèmes de repositionnement surfacique a été présenté. Après discussion, le système de positionnement surfacique était le plus adapté à notre centre. En effet, le spiromètre permettait uniquement un suivi respiratoire basé sur le volume d’air expiré, alors que le système surfacique permettait une aide au repositionnement, un suivi pendant le traitement, un suivi respiratoire, ainsi que la quantification les modifications anatomiques [26].
Celui correspondant le mieux était le système AlignRT de VisionRT. Il répond également au budget alloué. De plus, celui-ci est compatible avec notre système actuel et permet d’être installé sur un Halcyon, qui est la prochaine machine installée au CORT37.
5. Prérequis installation et installation
Il a donc été décidé d’installer le système AlignRT sur deux machines de traitement. Dans un premier temps le Clinac 2 et Clinac 1 puis ensuite sur le 2émeTruebeam une fois celui-ci installé. Cependant, avec la crise COVID les travaux ont pris du retard et la livraison de la machine également, du fait du manque de matière première. Le système prévu pour le Clinac2 a été choisi en version Halcyon en prévision du changement du Clinac 2 pour un Halcyon. Le fait de commencer par un seul système comportait certains désavantages à l’utilisation du système, tels que le fait de ne pas pouvoir faire de DIBH, de ne pas pouvoir traiter sans points de tatouage ou encore le déséquilibre entre les machines. Pour cette raison il a été décidé après l’installation du premier système, de mettre en place le système prévu au Truebeam 4 sur le Clinac 1 avec un changement de machine du dispositif à l’installation du Truebeam 4. Mais pour installer ces systèmes des prérequis étaient à prévoir.
a. Prérequis
L’installation du premier système s’est déroulée du 8 au 10 fèvrier dans le bunker du Clinac 2. Un technicien de VisionRT est venu au préalable confirmer que le système pouvait-être installé sur cet accélérateur. Une fois ceci validé par le technicien, une liste de prérequis pour l’installation nous a été envoyée. Les prérequis nécessaires étaient les suivants :
- 1 prise électrique dans le faux-plafond du bunker
- Un interrupteur mural commandant la prise électrique du faux-plafond pour éteindre et allumer les caméras
- 1 prise électrique proche de l’emplacement de l’écran en pied de table dans le bunker
- Fournir/installer un support mural pour écran (27’’) /clavier/souris dans le bunker en pied de table
- Prévoir une goulotte pour le passage d’un câble réseau depuis le faux-plafond vers le support écran
- 1 prise électrique au pupitre de commande
- 1 prise réseaux brassée au pupitre permettant l’accès au réseau et la communication avec le TPS
- Fournir adresse IP, masque sous-réseaux et passerelle
- Prévoir un accès Internet pour la télémaintenance
En amont, pour toute la partie travaux nous avons donc pris contact avec une entreprise externe qui travaille régulièrement avec le CORT37. Et nous avons également transmis cette liste au service informatique pour les prérequis serveur et réseau informatique. La partie travaux n’a posé aucun problème, les interrupteurs et les prises ont été posés avant l’installation d’AlignRT.
Le problème était davantage d’ordre informatique. Plusieurs solutions étaient envisageables. La première solution, était de mettre en place un client unique AlignRT. Or, cela pouvait poser problème lors de l’installation du deuxième système, mais aussi car le système n’était pas connecté au serveur et utilisait uniquement le disque dur du PC. Après discussion avec l’informaticien, il en est ressorti qu’un tel système avait plus de chance d’être corrompu ou pouvait rencontrer des problèmes liés à un dysfonctionnement de disque dur. De plus, avec un tel système des coûts supplémentaires seront obligatoire lors du passage à un système serveur. La seconde solution, était un client multiple AlignRT avec serveur de la clinique unique. C’est la solution qui a été retenue car plus en adéquation avec le fonctionnement du service et l’avis du service informatique. Cependant, les serveurs du CORT37 manquant de place et d’autres projets incluant de l’espace informatique au même moment, le service informatique a dû dégager de l’espace pour pouvoir installer les prérequis d’AlignRT.
Il a également fallu revoir l’organisation de l’espace de travail au pupitre de traitement. En effet, l’installation d’AlignRT ajoute un écran et une tour. Après prospection de ce qui pouvait se faire pour rajouter cet écran, des plans avec les différents systèmes ont été proposés à l’ensemble des MERM pour savoir ce qui leur convenait le mieux. La décision fut unanime de décaler les écrans avec un support d’écrans doubles. Pour garder la configuration linéaire du pupitre tout en y implémentant un écran supplémentaire et en gardant une certaine ergonomie du poste favorable au travail des MERM (Figure 28).
Figure 28 : Pupitre après installation du système AlignRT

Un autre prérequis nécessaire était la pose d’une tablette en salle pour accueillir un clavier et une souris pour permettre la navigation sur un écran en salle avec un retour visuel des caméras. Dans un premier temps une tablette avait été installée par le service externe de travaux. Cependant, ce système n’était pas assez ergonomique et aurait pu occasionner des blessures du fait de son positionnement. Après discussion avec le fournisseur VisionRT, il en est ressorti que le clavier et la souris était sans fil. Il a alors été décidé de mettre en place une tablette mobile qui permettrait au manipulateur d’être au plus près du patient tout en pouvant naviguer sur l’écran en salle d’AlignRT.
Ces prérequis ont été réalisé avant l’installation du système dans le bunker et celle-ci a commencé le 8 février et devait durer jusqu’au 10 février.
b. Installation
Avant l’installation nous avons réceptionné le colis contenant les différentes pièces du système. Une validation du contenu du colis a été effectué par les techniciens avant le début de l’installation, aucun problème n’a été constaté. Néanmoins, comme il s’agissait d’un système Halcyon et non pour Clinac, il a été nécessaire de stocker l’anneau In-Bore contenant les caméras dans une zone de stockage jusqu’au changement de machine prévu dans plusieurs années.
Après avoir validé le contenu du colis, les techniciens ont fait les marquages pour le positionnement des pods en salle. Ce travail avait déjà été réalisé lors de la venue du technicien qui a validé la possibilité d’installer le système. Cependant, l’emplacement des caméras a dû être changé du fait de la position des raccords du faux plafond. Celui-ci empêchait de placer les mats des pods à l’endroit idéal. Il a donc fallu déporter les caméras via un accessoire.
Une fois les portants placés, les techniciens ont dû poser les caméras (Figure 29) et passer tous les câbles dans le faux-plafond jusqu’à la station extérieur. L’après-midi du 8 février le gros œuvre était fait.
Les techniciens se sont alors occupés de la partie informatique. La version du système n’était pas prévue pour un Clinac mais pour un Halcyon et était en version 7, avec comme attente la connexion à 5 caméras et non 3 comme nécessaire pour un Clinac. Après un downgrade de la version, les techniciens ont pu commencer à régler les pods.
Figure 29 : Salle de traitement avant et après installation du système AlignRT

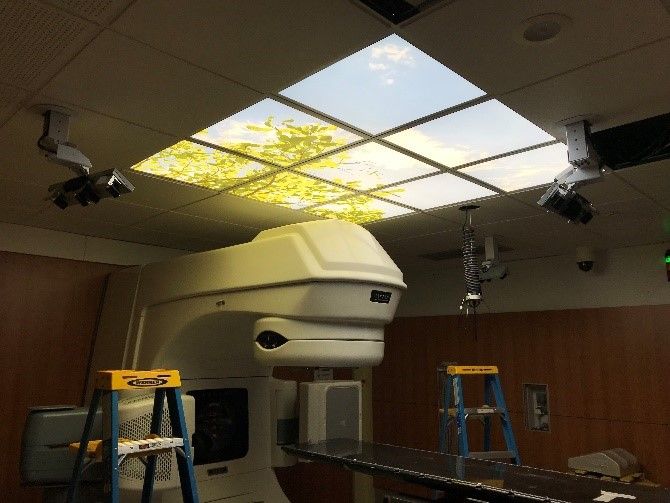
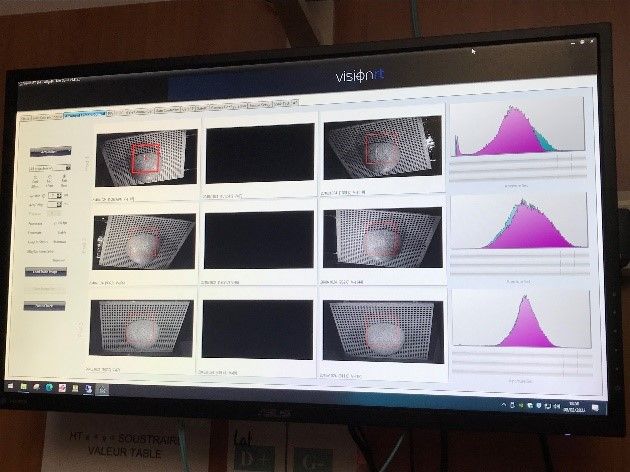
Le 9 février les techniciens avaient ainsi finalisé la partie informatique et le réglage mécanique des pods. Ils ont donc commencé la calibration du système le 9 février. Pour cela plusieurs fantômes ont été utilisés tels qu’une plaque de calibration servant également au contrôle qualité quotidien, une demi-sphère servant à régler la netteté, un fantôme constitué de deux protubérances permettant de régler la profondeur, les zones d’ombre et de valider l’utilisation des caméras ainsi que du logiciel et une plaque constituée de plusieurs points permettant une calibration de chaque caméra (Figure 30). Aucun problème n’a été relevé durant l’étalonnage du système.
Figure 30 : Etalonnage du système AlignRT
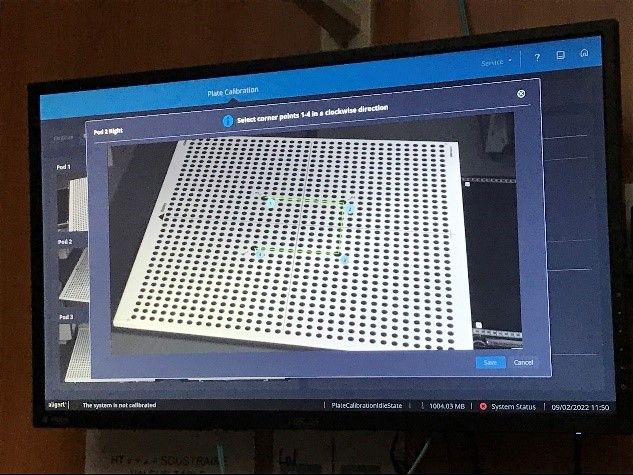
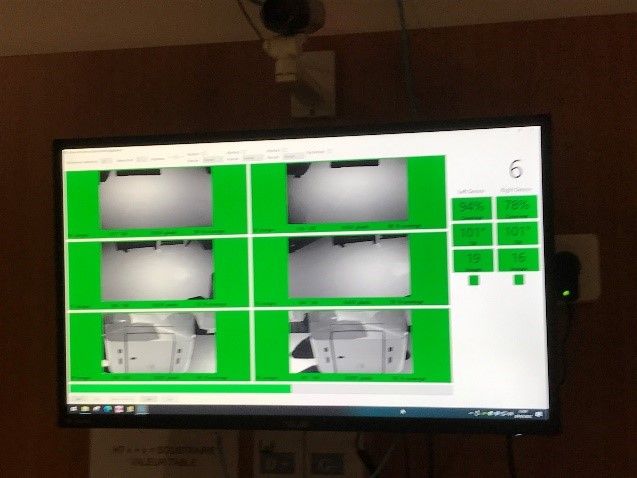
Après que les techniciens aient validé leur installation, nous sommes passés à la phase d’acceptante du système et de l’installation. Pour cela, un récapitulatif de chaque point a été réalisé avec les techniciens d’AlignRT. Aucun problème n’étant relevé, nous avons signé l’acceptance du système avec une journée d’avance sur le programme d’installation.
6. Formation du personnel
Pour la suite du projet, il était nécessaire de former les principaux utilisateurs du système, les MERM. Pour cela nous leur avons proposés sur la base du volontariat, de faire partie d’un groupe référent de 3 MERM, qui formerait par la suite les autres MERM à l’utilisation en routine clinique du dispositif. Les MERM ne connaissant pas l’outil, nous leur avons présenté, sous la forme d’une réunion de présentation de 45 minutes. A la suite de cette réunion quelques présentations du système au poste de traitement ont été effectué. Nous avons eu 4 candidats et en avons choisi 3, en prenant en compte les activités qu’ils faisaient déjà. Nous avons donc décidé de prendre des manipulateurs faisant moins de chose pour qu’ils aient davantage de temps à consacrer au projet.
Une fois le groupe référent formé, un retour sur l’installation a été fait en réunion technique avec les médecins/directions. Plusieurs problématiques ont été relevées sur le fait qu’un seul système ait été installé et que cela ne permettait pas de répondre à la totalité des besoins qu’ils avaient présentée. Il a donc été décidé à la suite de cette réunion qu’un deuxième système serait installé, une fois tous les manipulateurs formés en septembre 2022.
Une réunion avec le groupe référent, constitué d’un physicien, d’un médecin radiothérapeute, des 3 MERM et moi-même, a été réalisée de manière à étudier les risques que nous pourrions à priori rencontrer avec cette nouvelle technique et sa mise en place. Il en est ressorti qu’une absence de dynamique, une mauvaise gestion du projet, un manque de connaissance, un problème de restitution du travail et une mauvaise communication pouvaient être des points qui pourraient mener à une sous-utilisation du système (Figure 31). Pour cette raison, à la suite des formations, des réunions informelles ont été faites avec les membres du groupe référent pour gérer au mieux le projet.
Figure 31 : Diagramme d'Ishikawa pour la bonne réalisation du projet
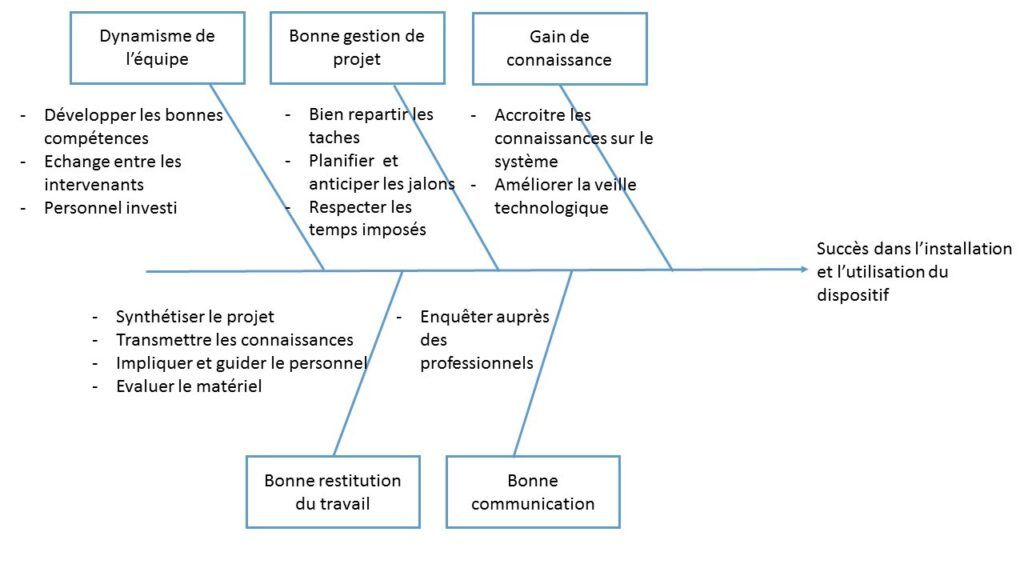
La gestion de ces points pouvant influer sur la bonne utilisation de l’outil, des formations proposées par VisionRT ont été programmées au mois de mars suite à l’installation. Les formations ont été réalisées de la façon décrite dans la Figure suivante (Figure 32) :
Figure 32 : Planning de formation
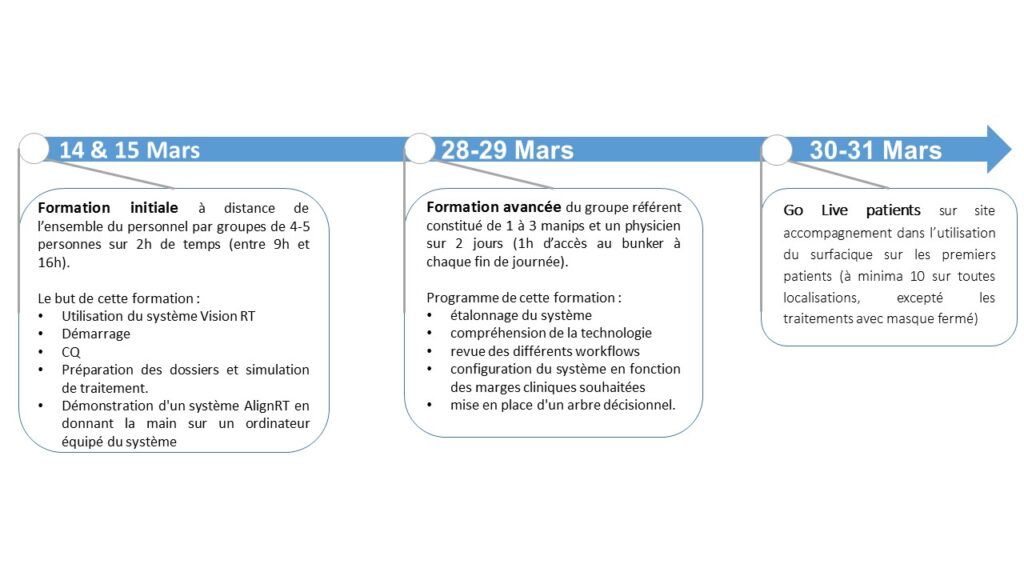
A la suite d’une réunion avec le formateur, nous avons mis en place un plan d’action pour les formations du personnel. Pendant cette réunion, la direction a décidé d’avancer l’installation du second dispositif au vu du retard d’installation du Truebeam 4 et l’intérêt non négligeable pour les patients. Il était donc nécessaire de former la totalité des MERM.
Les formations des MERM se sont faites par les MERM référents une semaine après la formation par AlignRT dans le but qu’ils puissent prendre en main l’utilisation du dispositif (Annexe 1).
Pour aider les MERM dans la réalisation des formations nous avons co-rédigé avec le physicien les documents liés à l’utilisation d’AlignRT. Nous avons ainsi rédigé 3 modes opératoires :
- Un pour la réalisation des CQ quotidiens, qui consiste en la mise en place d’une plaque de contrôle qualité qui donne les informations sur son bon positionnement et les critères à respecter pour la réussite du CQ. Les critères principaux étant la luminosité de la pièce, l’allumage des caméras avant le logiciel, pour un souci de synchronisation, mais également la température des caméras (Annexe 2)
- Un pour la préparation des dossiers pour les traitements avec utilisation d’AlignRT. Il aider les utilisateurs dans la préparation du dossier et la création des régions d’intérêts (Annexe 3).
- Un sur l’utilisation du système pendant le traitement (Annexe 4)
- Un arbre décisionnel permettant aux MERM de savoir quoi faire en cas de questionnement (Annexe 5)
Une date butoir pour la formation de tous les MERM a également été décidée correspondant à l’arrivée du second dispositif le 10 mai. La validation des formations s’est faite par une fiche de formation comprenant différents points essentiels à acquérir pour utiliser le dispositif en routine clinique et sans MERM référent. Une réunion a été effectuée en amont pour que les MERM référents aient le même discours, concordant avec la façon d’opérer en routine.
Il était également important de former les physiciens à l’utilisation du système. Pour cela une fiche d’évaluation a également été utilisée, abordant les différents points essentiels à l’utilisation du dispositif. A la différence de la formation des MERM, une partie sur le paramétrage et le trouble shooting a également été proposée. Une documentation apportant des informations sur les pannes ou problèmes pouvant être rencontrés a également été rédigée de manière à faciliter les interventions (Annexe 6).
Au niveau informatique, il a également été nécessaire de définir en amont les responsabilités des différents protagonistes. Pour cela des sessions particulières ont été créés avec des droits d’accès différents. Les MERM sont divisés en deux groupes, les MERM référents ont accès à une partie des paramétrages permettant l’archivage des dossiers après un certain temps alors que les autres MERM n’ont accès qu’aux onglets traitement et CQ quotidien. Les physiciens ont eu accès à la totalité des onglets et ont une responsabilité de suivi de CQ, de calibration du système, de création de nouveaux utilisateurs et d’intervention en cas de pannes.
7. Suivi, contrôle et maintenance
a. Suivi de formation
Le suivi du personnel formé a été délégué aux MERM référents de manière à ce qu’ils soient impliqués dans le projet. Quand un MERM rempli les critères de validation de sa formation, il peut alors utiliser le système en autonomie (voir annexe 1). Du fait qu’ils aient à gérer les formations, des rappels fréquents de la date butoir et de l’enjeu leur a été fait pour que le suivi soit correctement effectué et les formations dispensées à la totalité du pôle MERM. Il a également été important de suivre quelques formations au pupitre avec les MERM pour débriefer sur ce qu’il était important d’apporter comme information aux MERM en formation. En effet, certains points n’étaient pas abordés durant les premières formations mais après discussion avec les MERM formateurs, ils ont adapté leur discours et leur formation pour apporter les informations nécessaires à la bonne utilisation du dispositif. Des discussions avec les MERM formés ont également été réalisées pour vérifier que la pratique était homogène. Il en est ressorti que le discours de chaque MERM était cohérent et que la pratique l’était également.
Cependant, un suivi avec des retours réguliers devra être mis en place pour éviter les dérives d’utilisations tels que le suivi pendant le traitement des mouvements du patient par le MERM contrôlant la délivrance du traitement ou encore la réflexion sur les régions d’intérêt à délinéer.
b. CQ quotidien
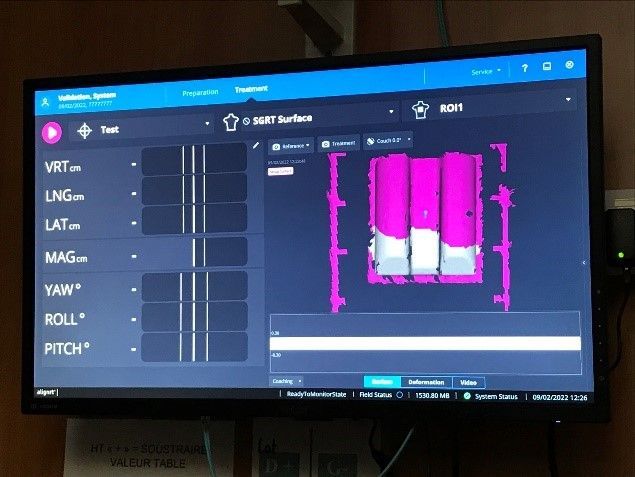
Il était également important de former les MERM et les physiciens au CQ quotidien. Un CQ est valable 24h, il est donc important que le contrôle soit réalisé tous les matins. Pour ce CQ, un ordre d’allumage des dispositifs est important pour une bonne synchronisation. En effet, dans un premier il faut éteindre/rallumer les caméras et s’assurer qu’elles aient atteintes la température attendue (entre 27 et 35°C). Dans un deuxième temps, il faut démarrer le logiciel AlignRT. Après le temps de préchauffage, il suffit de placer une plaque à l’isocentre de la machine (Figure 33). Le centrage se fait sur le réticule de la machine avec un champ ouvert au maximum (40x40cm) et à DSP 100cm (isocentre de traitement). Une fois la plaque placée correctement, il faut aller dans le module CQ quotidien du logiciel AlignRT. Si le CQ est réussi, c’est-à-dire que la valeur obtenue est inférieure à 0,6mm, le MERM peut utiliser le système. Il est important que le CQ n’ait pas échoué plus de 5 fois de suite sinon la base de données d’étalonnage est bloquée et il est alors nécessaire d’appeler le support. Pour cette raison, si le CQ échoue 2 fois, les MERM doivent appeler les physiciens pour prendre le relai et réaliser, par exemple, une nouvelle calibration du système.
Figure 33 : CQ quotidien d'AlignRT

Cette calibration se fait de la même façon que le CQ, mais n’est réalisable que par les physiciens (droits utilisateurs). Il peut être nécessaire de réaliser une calibration dans le cas où quelqu’un aurait accidentellement donné un coup dans un pods, ce qui pourrait la décaler.
En cas de problèmes plus important, il est possible d’appeler les formateurs et techniciens français pour une intervention. Seulement si personne n’est joignable il faut alors appeler le support anglais et fournir le numéro de série de l’appareil en panne. Au CORT37, du fait qu’il s’agisse d’un système Halcyon down grade, il est important de le signaler au support anglais pour qu’ils réalisent le bon diagnostic. La plupart des maintenances se fait à distance. Ils peuvent remettre une sauvegarde temporaire d’étalonnage, mais une intervention sera tout de même nécessaire par un technicien sur place.
c. Suivi d’utilisation et problématiques sur les contentions
Après quelques semaines d’utilisation du système nous avons pu remarquer avec les manipulateurs référents que les contentions avaient un impact sur le positionnement du patient. En effet, les repose-bras ayant du jeu au niveau des vis, lorsqu’un patient pose ses bras sur le support, nous pouvions remarquer une différence entre le scanner et la salle de traitement. Ceci s’explique par le fait que les contentions du scanner sont beaucoup moins utilisées que celles du Clinac2. Cela correspond à environ 5 patients par jour au scanner contre une quarantaine au traitement. De plus, les cales genoux et pieds du Clinac 2 étant abimées, il a été nécessaire de les changer quelques mois avant la mise en fonctionnement du système.
Cependant, après utilisation de ces nouvelles contentions, nous nous sommes rendu compte qu’elles n’avaient pas la même profondeur et avait donc un impact sur la position du patient. Ce décalage a pu être quantifié à l’aide d’AlignRT. Pour cela des patients scannés avec une cale mais traités avec une autre cale genou avaient un pitch affiché par AlignRT d’environ 2°. En utilisant la même cale, le roulis était affiché à 0°. Après cette vérification, il a été décidé d’écarter la cale unique différente et de renouveler le parc avec les mêmes cales pour chaque salle (salle scanner et bunkers).
Suite à l’installation d’AlignRT, il a donc été observé et confirmé que les contentions sont à revoir. Par la suite, il a été nécessaire de faire un état des lieux des contentions de la totalité du parc. Cela a permis de faire un inventaire de la totalité des contentions, de relever les références de chacune mais également son état et sa position dans le service. Après cette étude de 2 semaines, il en est ressorti qu’un renouvellement du parc était nécessaire. Une réunion avec le cadre du pôle physique et le cadre manipulateur a été prévue de manière à préparer un plan d’action. Deux choix se présentaient alors : renouveler le parc de contention actuel en neuf ou chercher du nouveau matériel. La recherche de matériel impliquait de passer par des phases d’études et y dédier du temps. Cependant avec les effectifs réduits, cela semblait trop chronophage. La première proposition a été retenue ; le parc de contention sera renouvelé à l’identique puis nous ferons des études sur ce qu’il est possible d’acheter dans quelques années.
8. Etude rétrospective de l’utilisation du système
Après 1 mois d’utilisation de ce système, il en ressort une satisfaction des utilisateurs et des retours positifs sur l’intérêt global du dispositif pour le positionnement des patients.
Le plus grand intérêt se révèle être pour la mise en place et le traitement des patientes atteintes d’un cancer du sein (Figure 34).
Comme il est possible de le voir sur la figure 34, la tête humérale est délinéée en rouge pour permettre un repositionnement au traitement sur l’imagerie kV. L’imagerie kV de gauche a été réalisé sans l’utilisation du système AlignRT, nous observons que la position de la tête humérale et donc du bras n’est pas optimale. Sur l’imagerie kV de droite, cette fois le système AlignRT est utilisé, la position de la tête humérale est conforme à ce qui été attendu. Nous observons également une différence sur le contour externe de la patiente. A gauche (sans AlignRT), il y a un écart entre la position attendue du scanner initial et l’imagerie kV du traitement. A droite (avec AlignRT), la position de la patiente est conforme à la position initiale. Cette différence peut se retrouver pour la plupart des patientes ou les MERM rencontre des difficultés de positionnement.
Figure 34 : Imagerie de positionnement illustrant la différence entre le positionnement sans(à gauche) et avec(à droite) AlignRT
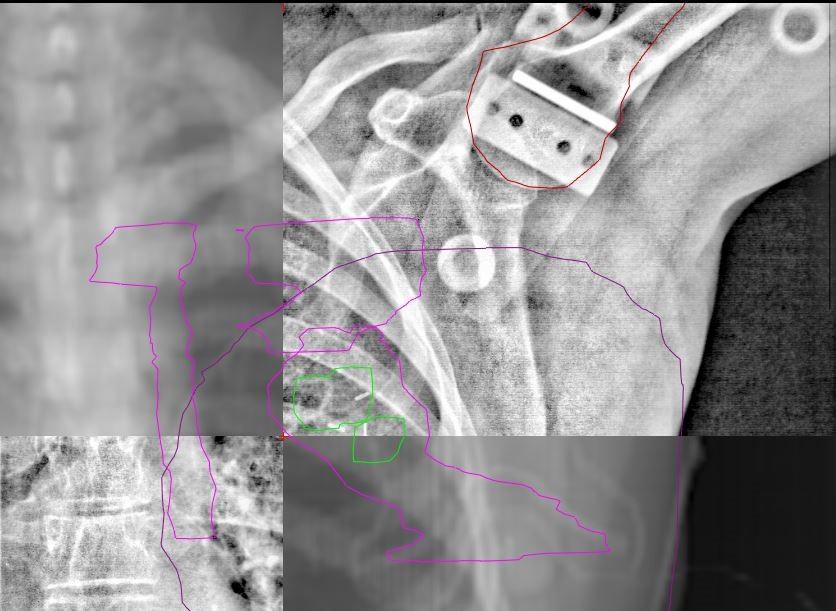
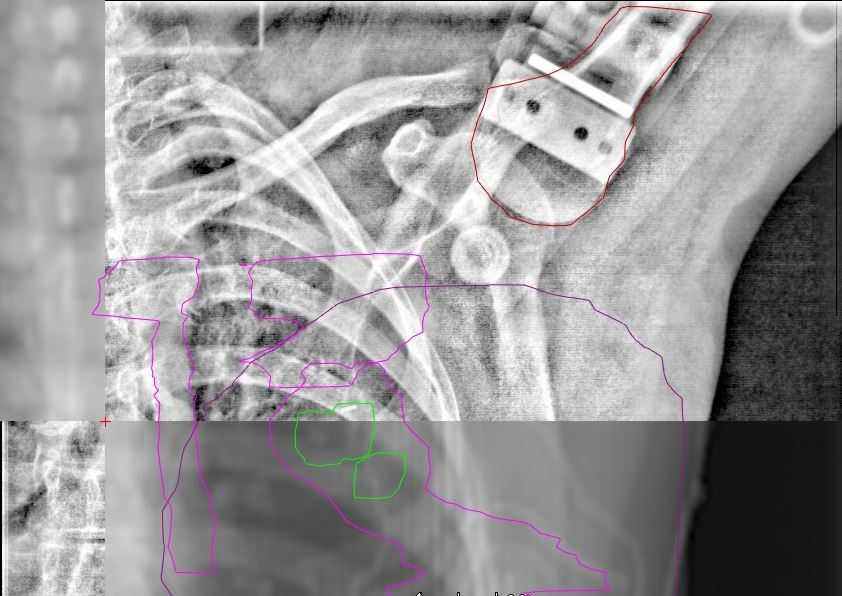
Cette imagerie de positionnement est réalisée après la mise en place du patient en salle, les MERM sont alors revenu au pupitre de traitement et la porte du bunker est fermée. De ce fait, si la position du patient n’est pas conforme au scanner initial, il sera nécessaire aux MERM de retourner en salle de traitement pour modifier la position du patient. Cependant, il est difficile de quantifier une telle modification de position en salle et plusieurs modifications après obtention de l’imagerie irradiante sont possible. Ce temps de repositionnement peut alourdir le temps de traitement et créé une incertitude de positionnement à chaque séance. Avec l’utilisation d’AlignRT, la validation de la position se fait en temps réel au moment de l’installation du patient en salle. Des aller-retour après l’imagerie irradiante est alors moins fréquente et le nombre d’imagerie irradiante est également moins importante. La rectitude de positionnement à chaque séance permet un traitement encore plus précis du volume cible à traiter et donc un traitement encore plus efficace pour le patient.
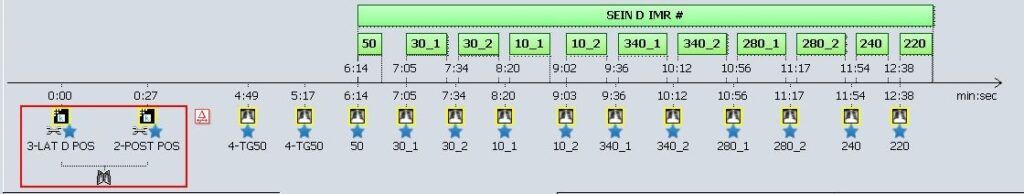
L’utilisation du système n’alourdit pas la prise en charge des patients. De ce fait le traitement n’est pas plus long. Il n’y a pas forcément de gain de temps sur le traitement par lui-même mais il y en a sur la mise en place dès le positionnement en salle. Il est possible de voir sur la Figure 33 que le temps de traitement peut être moins long avec AlignRT. Sans AlignRT le temps de mise en place est un peu plus court du fait qu’il n’y a pas le temps dédié à l’utilisation du système. Cependant, si nous comparons les temps de traitement après l’imagerie de positionnement (LAT D et POST) nous voyons un temps beaucoup plus long sans l’utilisation d’AlignRT, dû au repositionnement du patient par les MERM en salle de traitement (Figure 35). Ils sont alors obligés de refaire l’imagerie de positionnement pour valider leur décalage. Alors qu’avec le système AlignRT, la position est validée avec l’imagerie de positionnement et le traitement peut suivre son cours sans modifications. Nous observons alors une différence de temps de traitement de 3min entre les deux séances. Ce qui est un point positif pour les patients qui resteront moins longtemps sur la table de traitement immobile. Ceci implique également une diminution des mouvements des patients pendant le traitement qui pourraient engendrer une irradiation moins précise.
Figure 35 : Temps de traitement sans(image supérieure) et avec(image inférieure) AlignRT

Une étude sur les décalages après imagerie de positionnement a été réalisé sur 20 patientes traitées avec et sans AlignRT (Tableau 1). Les moyennes obtenues sur les décalages de table sont présentées dans le tableau suivant :
Tableau 1 : Résultats des décalages après réalisation de l'imagerie irradiante pour 20 patientes
| Sans AlignRT | Avec AlignRT | |
| Décalage vertical de la table de traitement | 0,6cm | 0,3cm |
| Décalage longitudinal de la table de traitement | 0,7cm | 0,3cm |
| Décalage latéral de la table de traitement | 0,5cm | 0,4cm |
| Rotation de la table de traitement | 1° | 0,5° |
Ces résultats permettent de se rendre compte de l’exactitude de positionnement avec le système AlignRT. En effet, les décalages réalisés avec l’utilisation d’AlignRT sont moins important. Ce qui signifie que le patient est correctement installé et que peu de mouvements de table seront réalisés pour essayer de se rapprocher la position attendue.
De plus, les MERM peuvent valider directement le gonflement du sein ou de la paroi et prévenir le médecin pour avoir la conduite adaptée à tenir. En effet, avec l’outil déformation il est possible de quantifier une modification morphologique du patient dont la validation sera complétée par l’imagerie irradiante. Sans le système AlignRT, il était nécessaire de faire un scanner de reprise pour s’assurer qu’il s’agissait d’une modification anatomique et non d’un problème de positionnement. Avec le système AlignRT, la position étant validée, l’utilisation de l’outil déformation permettra de quantifier la déformation. Il sera quand même nécessaire de réaliser un scanner de reprise pour adapter la dosimétrie mais le temps de reprise sera moins long car la justification de la prescription d’un scanner de reprise sera plus aisée.
Au début des formations les MERM ont relevés qu’ils étaient moins à l’écoute du patient, lors de l’installation de celui-ci sur la table, car ils se focalisaient plus sur le système. Néanmoins, maintenant que le dispositif est utilisé en routine, l’habitude de parler avec le patient est revenue.
L’utilisation des outils surface, déformation et vidéo est apparue assez évidente aux utilisateurs. Ils ont vite compris l’intérêt des 3 outils proposés et la façon dont ils pouvaient les utiliser en routine pour les aider et améliorer le traitement du patient.
Dans l’ensemble l’utilisation du système a été adoptée, permettant une amélioration certaine du positionnement du patient et donc de son traitement tout en apportant une aide certaine aux MERM.
9. Etude rétrospective sur la gestion du projet
Outre l’utilisation du système validée par la totalité des utilisateurs du centre, il est important de faire un retour sur la gestion de projet liée au dispositif pour améliorer la méthodologie pour le prochain projet de ce type [27].
a. Pré-installation et installation du système
Il est possible de relever dans un premier temps les problèmes rencontrés pour voir comment ceux-ci auraient pu être évités. Les principaux problèmes ont été rencontrés au moment de la pré-installation et de l’installation. En effet, lors de la pré-installation du fait d’une mauvaise communication entre le service technique de VisionRT et le CORT37, il a fallu revoir le système de support du clavier et de la souris en salle. L’information sur le fait que le clavier et la souris étaient sans fil n’avait pas été correctement donnée par VisionRT. De ce fait, un système de plaque avait été installé proche de l’endroit ou devrait se trouver l’écran en salle, ce qui gênait les MERM. Leur avis aurait pu être pris en compte plus tôt pour l’emplacement du support et du système utilisé. Ce qui a été fait par la suite en leur proposant dans un second temps, un système mobile de support.
Le changement de configuration du pupitre au traitement a été un autre problème de la pré installation. Différents projets d’aménagement ont été proposés aux MERM. Cependant, les avis de chacun était différent, la prise de décision a été compliqué. Pour leur éviter trop de changement il a été décidé de ne pas modifier la configuration linéaire du poste. Un support d’écran double a été le meilleur compromis.
Au moment de l’installation, aucun réel problème pouvant affecter la bonne mise en place du système n’a été relevé. Seuls l’utilisation de support de pods déportés et les problèmes informatiques qui auraient pu être géré en amont en incluant l’informaticien plus rapidement dans le projet. Cependant, après les formations, les techniciens n’avaient pas finalisé les filtres d’export des dossiers patients. Ceci n’a pas été vérifié du fait qu’aucun document fourni pas les techniciens pour la validation de la mise en place du système n’en faisait rapport.
b. Communication
Il en ressort que les principaux problèmes rencontrés lors de l’installation viennent d’un manque de communication entre le fournisseur et la clinique. Cependant, cela n’a que très peu affecté la mise en place du système. De plus, du fait de la prise rapide de décision les actions correctives ont été menées rapidement évitant des disfonctionnements dans la mise en place et l’utilisation du système. Néanmoins des axes d’améliorations par rapport à la communication avec le fournisseur peuvent être envisagés tels que définir un seul interlocuteur au sein du CORT37 et mieux appréhender les problèmes qui ont pu être rencontrés en amont.
Sur la gestion de projets, des difficultés ont pu être relevées sur le fait que la réunion de tous les référents de manière simultanée était compliquée. Malgré des retours réguliers avec les différents interlocuteurs, il a été compliqué de les réunir officiellement. Ceci s’explique par un manque de personnel dans le service au niveau du pôle médicotechnique. Il a tout de même était possible de se rassembler pour organiser les formations et valider le discours des référents aux futurs utilisateurs. Etant donné que nous avions un petit groupe de référents, il a été possible de transmettre les informations rapidement. La réactivité de chacun a permis de prendre des décisions rapides et de prévenir les difficultés en avance.
Cependant, le plus compliqué a été de réussir à impliquer la totalité des MERM pour qu’ils se rendent compte de l’utilité du système. Avant le début des formations, les MERM étaient assez sceptiques quant à l’utilisation du système. Malgré une réunion de présentation du système, ils avaient peur que cela alourdisse les traitements. Mais après formation et utilisation du système les doutes qui pouvaient persister ont été levés.
c. Autres problèmes
Des éléments extérieurs au système et à son utilisation auraient également pu ralentir le projet. Par exemple, il est important d’évoquer les problèmes rencontrés par rapport aux contentions vieillissantes. Celles-ci ayant un impact direct sur le positionnement du patient, il a pu être remarqué que certaines contentions ne permettaient pas d’exploiter pleinement le système. Une prise de décision rapide après l’étude sur les contentions a permis un renouvellement de certaines contentions. Ce qui va permettre d’utiliser le système AlignRT au mieux.
Ce qui a fait la réussite du projet est l’efficacité et la réactivité de chacun. Cela a dû passer par des compromis mais également une bonne coordination des membres de l’équipe. Même si dans un premier temps, il a été compliqué au MERM référent de bien s’organiser. Des rappels fréquents et une confiance mutuelle entre les membres du groupe ont permis de garantir des formations complètes aux utilisateurs. Passer du temps avec eux, a aidé à instaurer une meilleure communication entre nous, permettant une plus grande réactivité et surtout la mise en place d’une confiance réciproque. Ayant choisi comme référents 3 MERM avec des connaissances et des capacités différentes, un physicien, un médecin et moi-même cela a créer une complémentarité permettant de mener à bien ce projet. En effet, les MERM apportaient une expertise du terrain, le physicien et moi-même avions des connaissances plus techniques permettant des explications plus poussées du système ainsi qu’une gestion de projet et de management et le médecin avait un regard critique sur l’amélioration du traitement pour le patient.
Il faut tout de même relever que des améliorations sont toujours envisageable pour améliorer en continu la gestion de projet et la mise en place de nouveau dispositif.
10. Suite du projet
A la suite de la première installation, il a été pris la décision d’installer sur le Clinac 1, le deuxième système déjà acheté. La date d’installation étant un mois après cette décision, une organisation était à mettre en place rapidement pour la bonne installation du système.
a. Installation au Clinac 1
Un système étant déjà installé, nous ne partions pas de zéro. Nous avons donc repris les mêmes éléments que pour le premier système et avons programmé les interventions extérieures nécessaires au prérequis. Nous avons également intégré dès le début les ressources nécessaires à la bonne mise en place du système.
Or, le délai restreint entre la signature du devis et l’installation, il a fallu contacter les entreprises extérieures rapidement et prévoir leurs interventions sur des temps libres de bunker. Ne pouvant pas annuler le traitement des patients pour optimiser au mieux le temps, nous avons dû regrouper les interventions sur la même matinée que le premier jour d’installation.
Une problématique a été relevée très rapidement : la réorganisation du poste de traitement (Figure 36). En effet, celui-ci étant plus petit que sur l’autre accélérateur, une optimisation du poste était à prévoir rapidement. Nous avons donc étudié le problème avec le service informatique et le cadre médicotechnique. L’intervention d’un menuisier et l’achat de support d’écran a été réalisé pour pallier cette problématique.
Figure 36 : Pupitre de traitement du Clinac 1 avant et après installation de AlignRT


Il a également fallu négocier les prix de désinstallation du système AlignRT et de réinstallation dans le futur bunker. Puisque nous installions un système sur une machine vouée à être remplacé dans un futur proche, il fallait dores et déjà prévoir le démontage du système dans ce premier bunker puis l’installation dans le nouveau bunker. Des compromis ont donc dû être pris, tel que le fait de réutiliser les potences du 1er bunker et la réinstallation de ces potences par une autre entreprise que VisionRT. Vision RT n’interviendrait alors que pour l’installation des caméras et l’étalonnage de celles-ci.
Les acteurs ont donc été impliqués très rapidement dans cette seconde installation. Les délais ont été respectés permettant la bonne mise en place du système sur cette seconde machine. Les problèmes rencontrés ont été d’ordre informatique du côté de VisionRT. Les rapports de fin de séance ne pouvaient pas être enregistrés. Ce problème était déjà présent pour le premier système et n’a été réglé qu’avec l’intervention du support anglais deux jours après l’installation. Cependant, cela n’a pas empêché la bonne mise en place du système avec une installation en un jour et demi.
Le mardi matin trois sociétés extérieures étaient présentes sur le site du CORT37 pour intervenir à différents niveaux. Le menuisier pour la partie réorganisation du poste de traitement, les électriciens pour le tirage de câbles et la pose de prises suivant les prérequis demandés par VisionRT et enfin VisionRT pour l’installation du dispositif. Il m’a fallu gérer les trois interventions en même temps. Un paravent pour délimiter la zone d’intervention et les autres bunkers a été posé pour éviter que les intervenants ne croisent des patients mais aussi pour la tranquillité des équipes.
Les pods posées dans ce second bunker sont des systèmes dernière génération de VisionRT ayant comme intérêt supplémentaire, de ne pas avoir une lumière rouge trop importante et donc d’être moins gênante pour le patient. Un autre détail diffère, il s’agit du suivi de la température qui ne se fait plus via un écran mais à partir de LED.
Des erreurs ont été constatées dans les jours suivants l’installation :
- Des caméras plus longues à atteindre la température souhaitée, une demande d’information technique à VisionRT a été faite pour savoir si le problème est connu. Les caméras atteignent la température souhaitée en 40 min au lieu de 20 min. Ce qui peut empêcher l'utilisation du système le matin pendant un certain laps de temps.
- Des désynchronisations des pods qui se règlent en général par l’arrêt et le rallumage du système. Il s’agit de la solution proposée par VisionRT.
- Un CQ quotidien mauvais dès le premier jour d’installation qui s’est réglé par la réalisation d’une nouvelle calibration (un écart compris entre 1,2 et 1,4mm a été constaté entre les pods)
- Une erreur d’enregistrement lors de la fermeture d’un dossier qui en bloquait la fermeture. La mise en pause du système puis la fermeture du logiciel ont permis de solutionner le problème.
Ces pannes ont été réglées par des actions internes mais un retour à la société VisionRT a été fait pour avoir un second avis. Il a été relevé, par le support AlignRT, qu’il y avait un problème de firmware qui empêchait une des caméras d’atteindre la même température que les deux autres caméras. Ce défaut a été corrigé par le support AlignRT en réinstallant le firmware.
b. Futur du projet
L’intérêt de ce second système est la possibilité de mise en place du DIBH. Pour mettre en place cette technique, il est nécessaire d’avoir une bonne connaissance de l’utilisation du système mais aussi des connaissances sur le traitement du cancer du sein en radiothérapie. S’agissant d’une nouvelle technique, un groupe avec de nouveaux référents a été constitué. Pour cette raison il a été nécessaire de communiquer cette information à l’ensemble du service. En effet, la mise en place de cette technique aura un impact sur la totalité du service. Les secrétaires devront pouvoir expliquer aux patientes en quoi consiste cette technique de traitement, mais aussi pouvoir savoir si les patientes n’ont pas de contre-indication à l’usage de cette technique. Les médecins devront adapter leur discours et mettre en place des tests d’effort pour savoir si les patientes sont en capacité de bloquer leur respiration pendant un certain temps. Les dosimétristes devront adapter les techniques de traitement pour diminuer le temps de délivrance de la dose avec de l’arcthérapie plutôt que la technique IMRT. Les manipulateurs devront appréhender la technique pour prévoir les temps de scanner et de traitement suffisant, mais aussi connaitre la technique pour bien l’administrer au patient. Cette technique devant être mise en place en septembre une gestion du projet sera à prévoir de la part des différents protagonistes rapidement et en prenant en compte les départs en vacances.
c. Retour après utilisation des deux systèmes
Ce projet d’installation a demandé une implication de la plupart des acteurs concernés, du médecin à l’informaticien, en passant par le pôle physique, mais surtout par les MERM, ce qui demandera l’implication de la totalité des acteurs du CORT37.
Après un retour de la part du personnel concerné par l’utilisation d’AlignRT, il en ressort que le projet s’est correctement déroulé et que l’utilisation du système convainc la totalité des acteurs. De plus le patient ne voit aucune différence pour son traitement mais à des conditions de traitement supérieur à ce qui pouvait être proposé avant.
Il est possible de dire que l’écoute et le suivi qui ont été mis en place avec les différents protagonistes ont permis d’avoir une équipe motivée qui a su respecter les délais imposés. La réactivité de chacun a également permis de faire face aux problématiques rencontrées en un temps restreint, de faciliter l’installation et de ne pas ralentir le projet.
Cependant, nous avons pu constater des problématiques concernant les contentions et les méthodes de travail qui ont pu être solutionnées. Ces questionnements auraient toutefois pu être analysés en amont pour être solutionné plus précocement.
La prise en compte les risques et des outils qualité ont permis de construire un projet sûr et efficace où les acteurs principaux ont pu s’investir et y trouver leur compte. Dans l’ensemble, les résultats ont été une réussite aussi bien pour les praticiens que les patients.
Il reste maintenant un temps d’accompagnement des utilisateurs pour ne pas perdre de vue l’intérêt du système et les connaissances nécessaires à son utilisation. Ceci permettra de mettre en place de nouvelles techniques de traitement telles que le DIBH mais aussi un suivi du traitement pour les patients permettant au praticien une plus grande réactivité sur les conduites à tenir en cas de modification anatomique. Il faudra également essayer de garder la motivation présente pour la mise en place des nouvelles techniques (tatooless, DIBH…) dont les formations commenceront en septembre 2022 [27] [28].
III. Missions annexes d’ingénieur biomédical réalisées durant le stage dans un centre de radiothérapie privé
1. Acquisitions de matériels pour l’amélioration de la prise en charge des patients en curiethérapie
a. Contexte
Actuellement, le CORT37 réalise des traitements de curiethérapie gynécologique avec le matériel du fournisseur Bebig. Pour cela les médecins doivent monter au bloc opératoire dans un premier temps pour faire un examen sous AG (anesthésie générale) dans le but de définir la tumeur. Pour le moment tout se fait en clinique. Quelques jours plus tard, les médecins et les manipulateurs formés à la curiethérapie retourne avec la patiente au bloc opératoire poser les dispositifs de curiethérapie (Figure 37). Ensuite la patiente descend dans le service de radiothérapie pour effectuer un scanner afin de vérifier la bonne position des aiguilles du dispositif. Ce scanner servira également à la dosimétrie de curiethérapie. Cependant, si les aiguilles sont mal posées, il est impossible de refaire l’application, il faudra donc adapter la dosimétrie.
Un autre besoin décrit par les médecins était la mise en place de la curiethérapie de prostate [29]. De ces différents points un cahier des charges a été créé regroupant ces différents besoins. La solution à adopter devrait être facilement transportable entre le service de radiothérapie et le bloc opératoire permettant un suivi des aiguilles et de l’implantation de grains. Un plus serait que le système soit non irradiant. L’IRM étant un système trop onéreux et non envisageable au vu de la configuration du service, nous nous sommes dirigés vers l’échographe [30].
Figure 37 : Image de scanner d'une application de curiethérapie
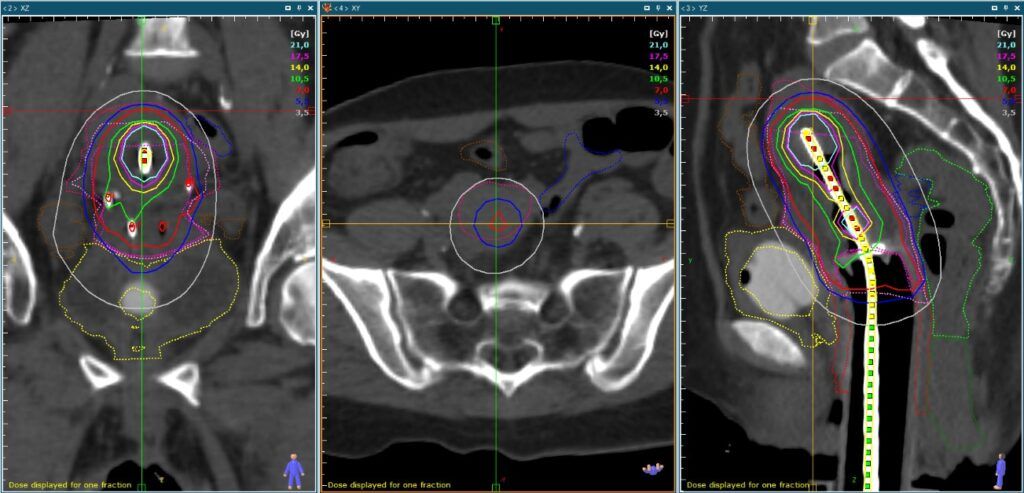
b. Méthode
Une fois les demandes nécessaires vues avec les médecins, il était également nécessaire d’avoir le prix qu’ils étaient prêts à engager, mais également le temps pour accéder à une solution. Il a donc fallu proposer aux médecins différentes solutions d’échographes. Différents points étaient à prendre en compte, tels que la mobilité du matériel, le type d’écran, le type de sondes nécessaires et les options. Nous avons donc contacté plusieurs fournisseurs pour faire un état des lieux du marché des échographes. Cette étude a ensuite été transmise aux médecins avec les explications nécessaires pour chaque système, avec leurs avantages et inconvénients en fonction de ce qu’ils souhaitaient. Il était également nécessaire de valider la communication entre le logiciel TPS de Bebig et l’échographe.
En partenariat avec la personne en charge de la facturation, nous avons cherché à savoir si l’acte était ou non facturable. Après quelques recherches, nous en avons déduit que dans la situation actuelle, nous ne pouvions pas facturer l’acte d’échographie. Nous avons ensuite fait une étude des prix d’un appareil, du prix de la maintenance par rapport à la facturation de l’acte de curiethérapie. Le résultat final était que l’achat d’un échographe n’était pas quelque chose de rentable, mais ne faisait pas passer la facturation de la curiethérapie en négatif. De plus, la radiothérapie permet de compenser un tel achat. Il a donc été décidé par la direction d’investir dans un échographe pour améliorer le traitement pour le patient [31].
Un comparatif des prix des échographes sur le marché a ensuite été réalisé. Des démonstrations des différents dispositifs ont été présentées. Il a également été nécessaire de prévoir des formations pour l’utilisation de l’appareil choisi. Les ressources humaines devront également être définies pour le bon fonctionnement du dispositif et la fluidité des activités dans le service.
D’autres points ont été discutés avec les médecins pour savoir s’ils souhaitaient que le dispositif soit utilisé pour d’autres utilités que la curiethérapie. Il a été décidé qu’il pourrait être utilisé pour les suspicion de globe vésical et d’autres cas pouvant être rencontrés dans le service de radiothérapie et pouvant avoir un impact sur le bien-être du patient.
Avec l’ingénieur biomédical de la clinique PSLV, la discussion autour d’une mutualisation d’un échographe a également été entamée. Cependant, la réalisation semblait compliquée pour plusieurs points :
- La responsabilité du matériel en cas de casse
- La disponibilité du dispositif
- La désinfection
- Les problèmes que nous pourrions nommer « politiques » entre les différents services
c. Résultats
Un médecin est allé en formation pour voir comment l’échographe est utilisé dans cette pratique pour se construire une idée plus concrète de l’utilisation du système en curiethérapie. Une fois cette formation réalisée, une validation de l’achat d’un échographe sera faite et le choix du dispositif sera discuté.
A la suite de cette validation, des démonstrations ont été programmées pour que les médecins choisissent le modèle qu’ils souhaitent acquérir. Les démonstrations sont prévues pour fin juin début juillet. Les fournisseurs étant contactés, le projet est pour le moment en attentes de ces démonstrations et les décisions d’intégration du matériel seront fait avant septembre.
Il a été nécessaire de bien définir les ressources humaines responsables du système dans le service, son emplacement, la désinfection de certaines sondes… Il faudra également prendre en compte les risques pouvant être liés à l’utilisation d’un tel système et prévoir des plans d’actions pour la bonne intégration et utilisation du dispositif au sein du service.
2. Intégration d’une GMAO
a. Contexte
Dans le service les CQ, des accélérateurs sont gérés par les physiciens et réalisés par les dosimétristes formés. Ces contrôles ont lieux 3 fois par mois, 1 fois sur chaque machine, avec un temps de 1 mois entre chaque contrôle pour être dans la réglementation. Pour ces contrôles, la solution Artiscan est utilisée, permettant d’avoir un suivi informatique des contrôles et mettant à disposition de ces utilisateurs des fantômes permettant la réalisation des différents modules. Une cuve à eau de 300L est également utilisée et a été récemment remplacé pour les CQ mensuel par une matrice permettant le contrôle de la dose (profils, rendements…). Il faut environ 5h pour réaliser et analyser les CQ pour une machine. Ce qui représente environ 15h dans un mois pour la réalisation et l’analyse des CQ des 3 machines. Les CQ scanners sont quant à eux suivis par un classeur avec les fiches de CQ format papier. Il est réalisé le CQ du zéro du scanner, des lasers et des UH du scanner. Une fois par an un CQ avec le CIRS (Figure 38) est réalisé pour le scanner et est maintenant suivi dans la base de donnée Artiscan [32].
Figure 38 : Photo et image scanner du CIRS

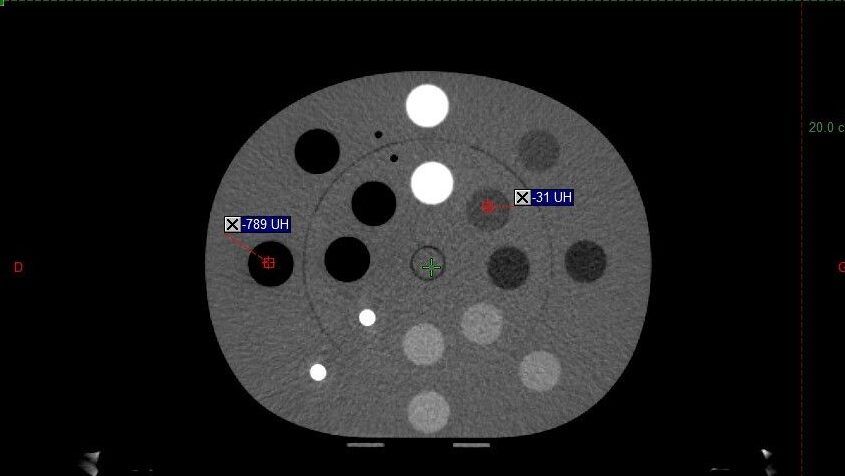
Pour ce qui est des maintenances, elles sont externalisées. Des PMI sont programmées par les techniciens Varian pour les accélérateurs ou GE pour le scanner. En cas de pannes machines, le support est appelé et s’il s’agit d’une panne importante la machine peut être mise à l’arrêt jusqu’à intervention du technicien. Il ne serait pas possible d’avoir des techniciens au CORT37, intervenant pour les pannes. Cela s’explique par le fait qu’il faudrait au moins deux techniciens et que ceux-ci, en dehors des maintenances, des pannes et des CQ n’auraient pas de travail au CORT37. Le suivi des maintenances préventives et curatives, est suivi grâce à un fichier dans un dossier sur le serveur du CORT37.
Pour ce qui est des appareils de mesure, ceux-ci sont régulièrement envoyés à l’étalonnage selon les préconisations du fabricant. Un suivi est réalisé à partir de fiches de vie sommaire. La matériovigilance est suivie via un classeur et des mails sont envoyés aux acteurs concernés et est suivi par un physicien médical. Peu de déclarations sont faites, car beaucoup de celles concernant la matériovigilance [33], sont rédigées par Varian, lié à des systèmes que nous ne possédons pas.
La matériovigilance est suivie via un classeur papier par un physicien. Au final, chaque personne gère une chose sans avoir connaissance de ce que font les autres. De plus, les informations sont parfois compliquées à trouver en l’absence de la personne responsable.
Les pannes sont suivies via le site MyVarian.com, et l’information d’une panne et de sa résolution sont notées dans un classeur papier présent au pupitre pour chaque machine. Si la panne ne peut être résolue sans l’intervention d’un technicien Varian, une demande d’intervention est réalisée par le physicien présent qui appelle donc le service client Varian et une affaire est ouverte. Une fois l’intervention terminée, le technicien crée un rapport informatique, qu’il envoie au physicien présent. Ce bon d’intervention est ensuite mis dans un dossier informatique. Les physiciens réalisent les contrôles nécessaires à la remise en route de la machine pour s’assurer que le problème est bien résolu et qu’aucun autre problème n’est détecté suite à l’intervention du technicien. Le physicien rempli ensuite le classeur papier des pannes et indique la résolution du problème et les actions mises en place pour valider le redémarrage des traitements.
Les CQ sont suivis sur la base Artiscan et dans un classeur Excel ou les physiciens indiquent les non-conformités et les actions mises en place. Les physiciens sont censés communiquer sur ces non-conformités mais également sur les dérives qui pourraient mener à une non-conformité. Pour cela le suivi est fait avec les graphiques Artiscan et le tableur Excel. Cependant il arrive que l’information soit lue au moment de l’analyse des CQ et non au moment de la réalisation des CQ ou la non-conformité pourrait être levée plus efficacement.
La gestion des stocks est également réalisée par certaines personnes et le suivi est parfois compliqué car chacun fait les choses sans concertation. Les fiches de vie des DM ne sont pas assez complètes, elles ne contiennent que les informations nécessaires aux physiciens, ce qui peut être problématique quand une personne d’un autre service a besoin d’informations et que les personnes responsables de ces fiches ne sont pas présentes dans le service.
Il y a également la gestion des maintenances liée au bâtiment qui est gérée par le cadre médicotechnique. Mais si la climatisation tombe en panne, les machines de traitements peuvent en être impactées. Ce qui implique que les physiciens puissent avoir accès aux informations liées aux intervenants extérieurs en cas de pannes de climatisation.
b. Méthode
Malgré l’utilisation de nombreux supports, une organisation bien rodée sur les CQ permet d’éviter les pannes bloquantes et permet un bon suivi des dérives, ainsi que des interventions rapides.
Le suivi des interventions des techniciens extérieurs est réalisé mais pourrait être amélioré tout comme celui de la matériovigilance. Des pannes entrainant le blocage de la machine pendant plusieurs jours peuvent arriver lorsque la pièce nécessaire à l’intervention n’est pas disponible. Cependant ce point ne peut être amélioré car les pièces sont gérées par Varian et non le CORT37 par lui-même. Ce qui implique des temps d’intervention parfois assez long du fait qu’il faille attendre le technicien pour un diagnostic puis la commande de la pièce.
Pour essayer d’améliorer le fonctionnement, une centralisation des informations était nécessaire avec un suivi des différentes interventions. Une réunion avec les différents chefs de pôle a donc été proposée pour essayer de trouver une solution.
Après un relevé des différentes problématiques relevées ci-avant, plusieurs solutions ont été proposées tels que revoir en totalité la pratique et la création d’outils Excel accessibles au chef de pôle. Cependant cela ne permettait pas d’alléger la pratique et les documents. La proposition d’une GMAO a alors été faite avec une explication claire de ce que cela représenté [34].
Après la deuxième réunion pour bien définir les besoins de chaque pôle, il a été décidé de faire appel à des fournisseurs pour avoir des démonstrations de logiciels. Une solution était déjà présente au CORT37 pour le pôle RH et comptabilité. Cette solution permettait, via un autre module, d’intégré une solution GMAO. Deux présentations de GMAO ont alors été faites. L’une par DimoMaint et la seconde par Qualishare (déjà présent pour le pôle RH et comptabilité). Le choix de ces deux solutions s’est fait pour Qualishare car la solution était déjà présente. Pour DimoMaint, elle permettait de remplir les attentes des chefs de pôles sans être une solution trop compliquée pour la structure qu’est le CORT37.
Une fois les deux présentations réalisées, une troisième réunion avec les chefs de pôles a été réalisée pour débattre du choix de la solution à mettre en place. Les deux solutions étaient différentes sur plusieurs points. Après discussion avec le pôle RH et l’informatique il en est ressorti que la solution Qualishare était complexe à mettre en place. Contrairement à cela, DimoMaint proposait un démarrage QuickStart qui permettrait un déploiement de la solution en 4 à 8 semaines.
A la suite de cette réunion des échanges avec des utilisateurs de DImoMaint ont été réalisé de manière à avoir des validations sur les différents points proposés par DimoMaint. Une fois toutes les informations souhaitaient par les chefs de pôles relevées, une présentation avec la qualiticienne a été faite pour présenter la solution à la direction avec une comparaison des différentes solutions étudiées.
Figure 39 : Cycle d'amélioration continu pour la mise en place d'une GMAO
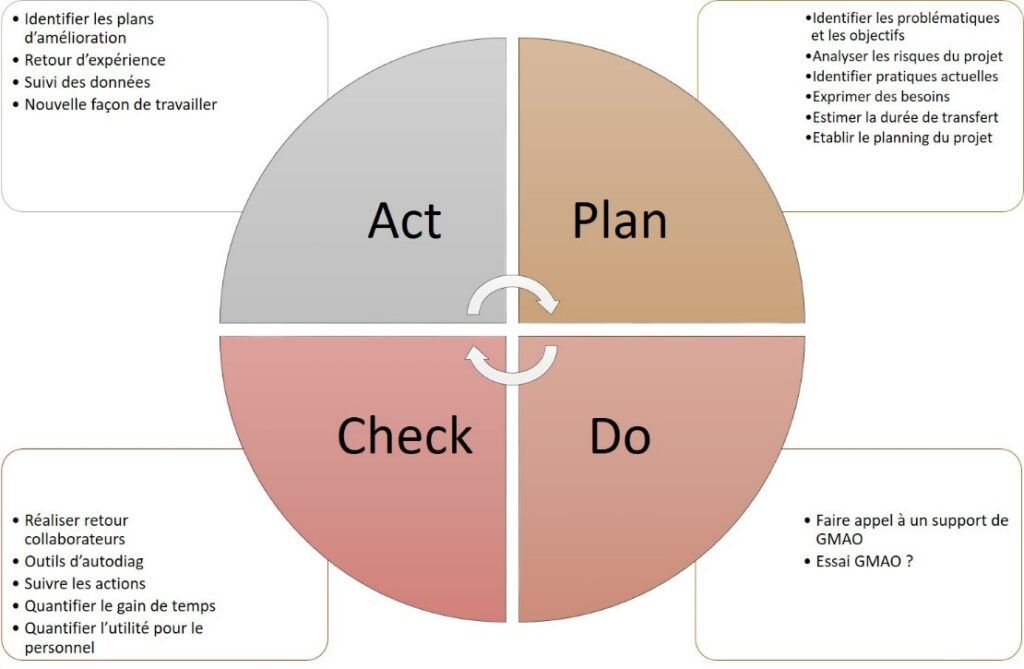
Une étude des ressources nécessaires a également été réalisée pour s’assurer que le déploiement pourrait se faire et que la solution continuerait à évoluer au CORT37. De plus, une présentation au personnel concerné a été faite pour que chacun s’implique et comprenne l’intérêt du système. La mise en place de cette solution a pour but de faciliter le travail du personnel impliqué et non de faire changer sa façon de travailler. Cela pourrait amener à un désintéressement du système à cause d’une charge de travail trop importante pour la mise en place, l’utilisation en routine et la modification de pratique. Il faut donc que cette solution apporte une aide à l’ensemble du personnel (Figure 39).
c. Résultats
Après une présentation aux différents salariés qui devront utiliser ce système, une présentation à la direction a été réalisée pour valider le projet. Après signature du devis, une mise en place rapide du système est prévue, en impliquant une ressource humaine dans le déploiement et la formation du personnel. Un regroupement des informations devra être réalisé ainsi qu’un rétro-planning pour pouvoir respecter les délais instaurés par la direction, qui nécessite un déploiement avant septembre 2022.
La solution devrait pouvoir apporter un gain de temps et un suivi des actions plus pertinent et plus lisible pour la totalité des acteurs.
IV. Bilan personnel
Durant ce stage de fin d’étude j’ai pu mettre à profit les connaissances théoriques acquises pendant les cours dispensés à l’UTC. Grâce aux multiples tâches et missions réalisées pendant ce stage. Voici un résumé des compétences et connaissances acquises pendant ces 6 mois (Tableau 2).
Tableau 2 : bilan personnel
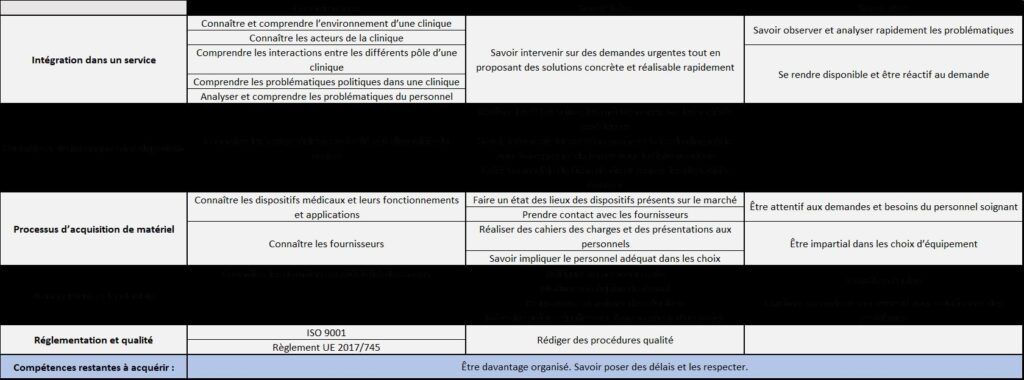
Conclusion
Dans un domaine médical relativement complexe de par son organisation ainsi que son évolution dans bien des domaines (informatique, physique, médical, ingénierie…), la mise en place d’un nouveau système dans un centre de radiothérapie demande un investissement important de l’ensemble du personnel.
Les évolutions technologiques aident les professionnels de santé à adapter les traitements pour augmenter les doses dans les tumeurs et diminuer les doses aux OAR pour fournir aux patients un traitement des plus efficace et personnalisé. Les caméras surfaciques font partie intégrante de ces évolutions grâce aux différentes possibilités qu’elles proposent.
Le système de repositionnement surfacique mis en place au CORT37 a permis d’améliorer la mise en place quotidienne du patient. Avant l’utilisation de ce système, le repositionnement s’appuyé sur un système de contention, de lasers ainsi que d’imagerie irradiante quotidienne. Cependant, l’utilisation des lasers et des contentions n’étaient parfois pas suffisante et impliquait la multiplication d’imagerie irradiante pour valider le positionnement. Ceci augmentait le temps de traitement mais également l’irradiation du patient. Ceci n’est plus le cas avec le système de repositionnement surfacique qui permet la validation de la position du patient dès la mise en place sur la table de traitement.
Malgré un intérêt très clair pour le patient, l’utilisation en routine d’un tel système peut parfois paraitre abstrait pour les professionnels de santé lorsque ceci n’y voit pas un intérêt flagrant et une perte de temps dans leur routine de travail. C’est pour cette raison que l’utilisation d’outils qualité, la prise de rôle de leadership et de management est important pour mener à bien ce genre de projet et motiver le personnel soignant. Il est également important de souligner que de tels projets ne sont réalisables que grâce aux compétences de chacun mis en œuvre pour permettre sa réussite.
Une gestion des risques a été essentielle mais malgré cela plusieurs problématiques ont été remarqués, essentiellement dû à l’intervention d’acteurs extérieurs et d’une méconnaissance de la totalité des points ayant un impact sur le système.
Ces différentes problématiques ont néanmoins été rapidement solutionnées par la mise en place d’actions efficaces.
Maintenant que ce système est en routine clinique, l’adaptabilité et l’utilisation par les MERM seront essentielles pour la mise en place de nouvelles techniques de manière à rendre les traitements optimaux pour les patients.
Annexes
Annexe 1 :
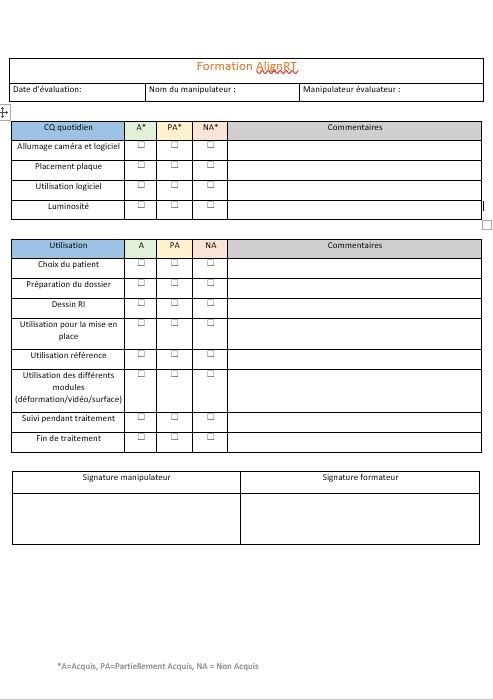
Annexe 2 :
- Déroulement de ce mode opératoire
Ce document doit être appliqué par l’équipe des médico-techniciens du Centre d’Oncologie et de Radiothérapie de Chambray les Tours.
- Démarrage système
Le matin, au moment de la chauffe de l’accélérateur, allumer les caméras en salle de traitement.
Plusieurs LED clignotent, les caméras sont prêtes quand toutes les LED sont vertes.
Le temps de chauffe est d’environ 20 min (la température de chaque caméra doit être entre 25-35°C (affichée sur l’écran de chaque caméra).
Remarque : si les caméras n’ont pas été éteintes la veille, il suffit juste de les éteindre et les rallumer avec l’interrupteur en laissant un intervalle de 20 secondes.
Après avoir allumé les caméras, il faut allumer l’ordinateur et le logiciel.
Remarque : si cet ordre d’allumage n’est pas respecté, il peut y avoir un problème de synchronisation des dispositifs.
- Réalisation du CQ quotidien
- Centrage de la plaque
En salle de traitement, centrer la plaque du contrôle sur la table de traitement.
Mettre une barre d’indexation en H0 pour aider son alignement.
Le bras et le collimateur doivent être à 0°.
Centrer la plaque sur le réticule (champ lumineux d’au moins 25x25 cm²) à DSP100 cm et la flèche « Gantry » vers la tête de l’accélérateur.
Plaque à centrer pour le CQ quotidien
- Réalisation du contrôle
Le contrôle est réalisable soit en salle de traitement ou soit à l’extérieur sur l’ordinateur. Dans le logiciel, cliquer sur « CQ Quotidien » (copie d’écran ci-dessous).
Le contrôle quotidien est valable 24h. La présence d’une croix rouge à côté de l’icône du contrôle quotidien indique qu’il est à réaliser. Il est également possible de le faire même s’il n’y a pas la croix rouge.
Il est impossible d’utiliser Align RT tant que la croix rouge est présente pour le contrôle qualité quotidien.
Icône du contrôle quotidien (à faire, croix rouge)
Cliquer sur « Commencer ».
Vérifier que le contrôle est conforme et cliquer sur « Terminer »
Si ce n’est pas le cas, revérifier le positionnement de la plaque et refaire le contrôle.
Si le CQ est mauvais une deuxième fois, appeler le physicien.
Résultat d’un contrôle conforme
- Problèmes rencontrés
Dans le cas de contrôle quotidien non conforme, il faut vérifier :
- la luminosité : mettre plus de luminosité pour que la plaque soit bien éclairée ;
- vérifier qu’il n’y a pas eu de coups dans la caméra, pas d’intervention sur le plafond lumineux, des travaux…
- un mauvais centrage de la plaque ;
Remarque : si le contrôle est mauvais 5 fois de suite, le logiciel se bloque.
- Informations
En cas de problème, il est possible de contacter Vision RT à l’adresse teamfr@visionrt.com pour le support français ou uktechsupport@visionrt.com tél : +442083496519 pour le support international.
Le numéro de série de chaque appareil Align RT se trouve sur la tour de l’ordinateur.
Annexe 3 :

Annexe 4 :

Annexe 5 :
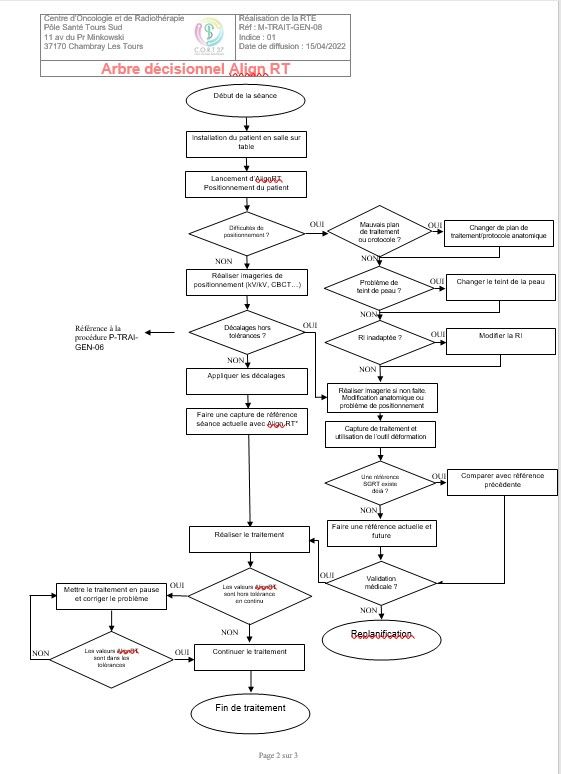
Annexe 6 :
| Redémarrage quotidien | |
| Synchronisation des caméras | Eteindre pendant une vingtaine de seconde les caméras et les redémarrer. |
| Problème service Windows | Redémarrer le service Windows |
| Température des caméras | Les caméras ne sont pas allumées depuis assez longtemps. Il faut attendre 20min entre l’allumage et l’utilisation de celles-ci. (25-35°C) |
| CQ quotidien | |
| La détection de la plaque ne se fait pas correctement. | Vérifier que celle-ci n’est pas détériorée |
| Hors tolérance | Plaque mal positionnée. Caméra déréglée. Problème de luminosité Après 2 essais hors tolérance, appeler un physicien. |
| Préparation | |
| Problème d’import, plan corrompu. | Supprimer et réimporter le plan. |
| Mauvais protocole localisation | Supprimer et réimporter le plan. |
| Mauvaise RI | Suivre le protocole de définition de RI |
| Traitement | |
| Perte d’information | Adapter la luminosité. Changer la couleur de peau. Occlusion d’une caméra. Papier/Contention. Zone RI trop importante ou manquant d’informations (vérifier nombre images/seconde) |
| Perte connexion | Resynchroniser les caméras |
| Décalage important | Vérifier que le plan de traitement choisi concorde avec le plan traité (ex : RA ou RA RED) |