IDS296 – Soigner par le son : mécanismes, enjeux et perspectives des ultrasons thérapeutiques
Les projets ou stages publiés auxquels vous accédez sont des rapports d'étudiants et doivent être pris comme tels. Il peuvent donc comporter des imperfections ou des imprécisions que tout lecteur doit admettre et donc supporter. Il ont été réalisés pendant les périodes de formation et constituent avant-tout des travaux de compilation bibliographique, d'initiation et d'analyse sur des thématiques associées aux concepts, méthodes, outils et expériences sur les démarches qualité dans les organisations ou sur les technologies en santé.
Si, malgré nos précautions, vous avez des raisons de contester ce droit de diffusion libre, merci de nous en faire part (master@utc.fr), nous nous efforcerons d'y apporter une réponse rapide. L'objectif de la présentation des travaux sur le web est de permettre l'accès à l'information et d'augmenter ainsi la qualité des échanges professionnels.
Nous ne faisons aucun usage commercial des travaux de projet ou de stage publiés, par conséquent les citations des informations et l'emploi des outils mis à disposition sont totalement libres. Dans ce cas, nous vous demandons de respecter les règles d'éthique en citant explicitement et complètement vos sources bibliographiques.
Bonne lecture...
Auteurs




Contacts
- Bintou DEMBELE : bintou.dembele1903@gmail.com
- Maël-Marie L'INTANF : maelintanf@gmail.com
- Elisa POUILLY : pouillyelisa@gmail.com
- Kaan TURGUT : kaan80turgut@hotmail.com
A rappeler pour tout usage : B.DEMBELE, M-M.L'INTANF, E.POUILLY, K.TURGUT « Soigner par le son : mécanismes, enjeux et perspectives des ultrasons thérapeutiques », Université de Technologie de Compiègne (France), Master Ingénierie de la Santé, Mémoire de Projet, janvier 2026, https://travaux.master.utc.fr/, réf n° IDS296, https://travaux.master.utc.fr/formations-master/ingenierie-de-la-sante/ids296/, https://doi.org/10.34746/ids296
Résumé
Depuis plusieurs décennies, l’utilisation des ultrasons en médecine occupe une place importante notamment pour le diagnostic avec des modalités comme l’échographie. En thérapeutique, leur utilisation est beaucoup moins connue et limitée. Bien que les applications usuelles soient rares, l’intérêt clinique pour les ultrasons thérapeutiques ne cesse de croître pour leur nature non-ionisante et relativement atraumatique comparé à d’autres types d’onde.
Cela ouvre la voie à des indications qui n’existaient pas jusqu’alors ou qui utilisaient des méthodes plus invasives et agressives. Les technologies HIFU et LIPUS, explorées dans ce mémoire, ouvrent l’accès à des alternatives prometteuses à des problèmes complexes comme l’ouverture réversible de barrières biologiques pour la délivrance ciblée de médicaments, la destruction thermique des tissus tumoraux ou encore la stimulation de la régénération tissulaire.
Dans cette étude, nous présentons les caractéristiques physiques des ultrasons, leurs différentes modalités de génération, d'interaction avec le corps humain et d’utilisation. Nous vous présenterons également, à travers le HIFU et le LIPUS, les applications innovantes pour lesquelles elles peuvent être utilisées. Nous finirons par souligner leurs apports pour la médecine ainsi que les limites rencontrées pour leur utilisation ainsi que les perspectives à venir.
Abstract
For several decades, the use of ultrasound in medicine has played an important role, particularly for diagnosis through modalities such as ultrasound imaging. In therapeutics, however, its use is far less well known and remains limited. Although routine applications are rare, clinical interest in therapeutic ultrasound continues to grow due to its non-ionizing and relatively atraumatic nature compared with other types of waves.This paves the way for indications that did not previously exist, or that relied on more invasive and aggressive methods. The HIFU and LIPUS technologies explored in this thesis provide access to promising alternatives for complex challenges such as the reversible opening of biological barriers for targeted drug delivery, the thermal ablation of tumor tissue, and the stimulation of tissue regeneration.
In this study, we present the physical characteristics of ultrasound, its various modes of generation, its interactions with the human body, and its uses. We will also present, through HIFU and LIPUS, innovative applications for which these technologies can be employed. Finally, we will highlight their contributions to medicine, the limitations encountered in their use and future perspectives.
Özet
Son birkaç on yıldır, ultrasonların tıpta kullanımı özellikle ultrasonografi gibi görüntüleme yöntemleri aracılığıyla tanı alanında önemli bir yer tutmaktadır. ultrasonların terapötik amaçlı kullanımı daha az bilinmekte ve halen görece sınırlı kalmaktadır. Bununla birlikte, terapötik ultrasonlara olan klinik ilgi, diğer dalga türlerine kıyasla iyonize edici olmamaları ve nispeten atraumatik özellikleri nedeniyle giderek artmaktadır.
Bu gelişme, daha önce var olmayan ya da daha invaziv ve agresif yöntemlere dayanan yeni terapötik endikasyonların ortaya çıkmasına olanak sağlamaktadır. Bu tezde incelenen HIFU ve LIPUS teknolojileri, hedefe yönelik ilaç taşınması için biyolojik bariyerlerin geri dönüşümlü olarak açılması, tümör dokularının termal ablasyonu ve doku rejenerasyonunun uyarılması gibi karmaşık tıbbi sorunlara yönelik umut verici alternatifler sunmaktadır.
Bu çalışmada, ultrasonların fiziksel özellikleri, farklı üretim yöntemleri, insan vücudu ile etkileşimleri ve kullanım alanları sunulmaktadır. Ayrıca HIFU ve LIPUS üzerinden, bu teknolojilerin kullanılabildiği yenilikçi terapötik uygulamalar ele alınmaktadır. Son olarak, bu yöntemlerin tıbba sağladığı katkılar, kullanım sırasında karşılaşılan sınırlamalar ve geleceğe yönelik perspektifler vurgulanmaktadır.
Téléchargements


Liste des acronymes
- BHE : Barrière Hémato-Encéphalique
- DM : Dispositif Médical
- HIFU : High Intensity Focalized Ultrasounds
- IA : Intelligence Artificielle
- IEC : International Electrotechnical Commission (Commission électrotechnique internationale)
- ISO : International Organization for Standardization (Organisation internationale de normalisation)
- LIPUS : Low Intensity Pulsed Ultrasounds
- US : Ultrasons
- USD : Ultrasons Diagnostiques
- UST : Ultrasons thérapeutiques
- TI : Indice Thermique
Les ultrasons thérapeutiques
Introduction
Contexte historique des ultrasons en médecine
Le phénomène physique des US, définis comme des ondes acoustiques de fréquence supérieure à 20 kHz, échappant à la perception auditive humaine, est soupçonné dès la fin du XVIIIᵉ siècle par le biologiste italien Lazzaro Spallanzani, qui observe en 1794 la capacité des chauves-souris à s’orienter dans l’obscurité. Un siècle plus tard, en 1880, Pierre et Jacques Curie mettent en évidence le principe de la piézoélectricité, ouvrant la voie à la génération et à la détection contrôlée des US. Cette découverte constitue le fondement des développements futurs, tant dans le domaine diagnostique que thérapeutique. Dès la fin des années 1920, Paul Langevin découvre le potentiel des US de haute puissance pour générer de la chaleur dans les structures osseuses et pour altérer la texture des tissus animaux, préparant ainsi le terrain pour les premières applications cliniques [1].
À mesure que ces avancées technologiques se sont structurées, leur utilisation clinique a nécessité la mise en place d’un cadre réglementaire spécifique.
Contexte réglementaire des ultrasons thérapeutiques en France
L’utilisation des UST est, comme toute pratique médicale, délimitée par un cadre réglementaire imposé par différents organismes nationaux, communautaires et internationaux. Le respect de ces exigences et recommandations permet d’assurer une utilisation fiable et durable des UST.
Le règlement européen 2017/745 ou règlement du dispositif médical (MDR) [4] classifie les dispositifs d’UST dans la catégorie des dispositifs temporaires étant utilisés pendant des périodes continues de moins d’une heure. Les UST font également partie de la catégorie des dispositifs actifs thérapeutiques, des dispositifs alimentés par une source d’énergie et ayant pour action de “soutenir, modifier, remplacer ou restaurer des fonctions ou des structures biologiques en vue de traiter ou de soulager une maladie, une blessure ou une infirmité” (Annexe VIII du MDR).
Ces dispositifs sont donc généralement de classe IIa et IIb selon le niveau d’énergie des ondes délivrées et du site traité. Il existe de rares applications pour lesquelles les UST sont catégorisés en classe III. Les US utilisés dans un but physiothérapeutique sont plutôt inoffensifs, ils sont donc classés dans la classe IIa. Certaines autres technologies innovantes comme les US focalisés à haute intensité font encourir des risques aux patients de par leur nature, leur densité ainsi que les sites traités par ces technologies. Ces dispositifs sont donc classés IIb.
Les dispositifs d’UST doivent répondre à plusieurs normes généralistes, dont la norme ISO 13485 relative au système de management de la qualité des dispositifs médicaux, la norme IEC 60601-1 portant sur la sécurité et la performance des équipements électromédicaux, ainsi que la norme ISO 14971 concernant la gestion des risques associés.
Des normes plus spécifiques encadrent également les UST. La norme IEC 60601-1-2 s’applique lorsque les dispositifs sont utilisés en présence de champs électromagnétiques, afin de garantir la sécurité et la performance malgré d’éventuelles interférences. La norme IEC 60601-2-62 définit quant à elle les exigences propres aux équipements HIFU. Enfin, la série IEC 62127 (parties 1 à 3) décrit les méthodes de mesure et de calibration des champs ultrasonores ainsi que les caractéristiques attendues des hydrophones utilisés pour ces mesures.
Enjeux de l'utilisations des ultrasons thérapeutiques
L’emploi des UST soulève de nombreux enjeux. Nous détaillerons les enjeux socio-économiques et technologiques.
Enjeux socio-économiques
En avril 2025, la Focused Ultrasound Foundation annonce avoir dépassé le cap du million de patients traités dans le monde, pour plus de 70 indications, incluant Alzheimer, Parkinson, tremblement essentiel, fibromes utérins ou diverses tumeurs.
Enjeux technologiques
Les UST posent aussi des défis techniques : assurer une précision millimétrique pour concentrer l’énergie sur la zone cible, garantir un haut niveau de sécurité pour éviter les dommages collatéraux, et tirer parti des avancées de l’imagerie pour optimiser le guidage thérapeutique. Enfin, la montée en puissance d’équipements plus compacts et portables facilite leur déploiement et soutient leur diffusion en clinique.
Problématique
À mesure que les technologies s’affinent et que les indications s’élargissent, une question demeure centrale et oriente aujourd’hui la recherche comme la pratique clinique :
Quels sont les fondements physiques, les mécanismes d’action, les limites et les bénéfices des ultrasons thérapeutiques, et dans quels contextes cliniques sont-ils appliqués ?
Pour répondre à cette problématique, ce mémoire s’organise en trois grandes parties. La première présente les principes physiques des ultrasons, en distinguant leurs applications diagnostiques et thérapeutiques. La seconde décrit les principales modalités d’UST, notamment le HIFU et le LIPUS, ainsi que leurs mécanismes d’action et leurs domaines d’application clinique. Enfin, la troisième partie analyse les apports, les limites et les perspectives d’évolution de ces technologies, en mettant en lumière les innovations susceptibles de favoriser leur intégration future dans les pratiques de soin.
Cadre d’utilisation des ondes sonores
Les ondes sonores sont utilisées dans de nombreux contextes médicaux, mais leurs finalités et leurs modalités varient considérablement selon les disciplines. Elles interviennent aussi bien dans l’imagerie diagnostique, la rééducation fonctionnelle, certaines techniques interventionnelles, que dans des pratiques non-thérapeutiques comme la médecine esthétique. Ces usages reposent sur des intensités, des mécanismes d’action et des cadres réglementaires très différents.
Dans le cadre de ce mémoire, l’étude se concentrera exclusivement sur les ultrasons employés comme modalité thérapeutique à visée médicale. Ce choix implique d’écarter plusieurs domaines connexes. Les applications utilisées en kinésithérapie par exemple, relèvent principalement de la physiothérapie et visent l’amélioration fonctionnelle plutôt que le traitement d’une pathologie. De même, les pratiques de médecine esthétique n’ont pas pour objectif la prise en charge d’un trouble médical ; elles poursuivent une finalité cosmétique (remodelage, raffermissement, rajeunissement) et obéissent à un encadrement réglementaire distinct de celui des dispositifs médicaux destinés au soin.
Intégrer ces usages pourrait créer une confusion entre des pratiques hétérogènes qui ne reposent ni sur les mêmes mécanismes physiques, ni sur les mêmes contraintes cliniques ou réglementaires. Le périmètre est centré sur les ultrasons thérapeutiques stricto sensu, cohérent avec l’objet du mémoire et avec l’analyse des dispositifs étudiés dans les chapitres suivants.
I. Physique des ultrasons
I.1. Les principes physiques et paramètres des ultrasons appliqués au diagnostic
Les US sont des ondes vibratoires qui se propagent dans un support matériel, c’est une onde mécanique qui se propage dans l’espace et la matière au cours du temps. Les US ont une fréquence comprise entre 20 kHz et 200 MHz [6].
Pour l’échographie, il existe plusieurs modes d’imagerie. Le mode B ou appelé le mode 2D est un mode qui permet d’afficher notre image en échelle de gris. Plus le signal est fort et plus le point sera brillant. Il y a quatre paramètres importants pour le mode B :
- La résolution de contraste : permet de mieux voir des structures proches dans le niveau de gris.
- La résolution spatiale : c’est la capacité de distinguer 2 points l’un à côté de l’autre ou l’un sur l’autre.
- La résolution latérale : elle dépend du temps, de la pénétration et de la densité de ligne (nombre de lignes d’acquisition).
- La résolution axiale : elle dépend de la fréquence.
Les ultrasons sont définis par plusieurs paramètres importants [7] :
- La fréquence : la fréquence correspond au nombre d’oscillations par seconde en Hertz. Plus la fréquence va augmenter (7–15 MHz), meilleure sera la résolution de l’image, mais la pénétration dans les tissus va diminuer, car les hautes fréquences seront plus absorbées que les basses fréquences. On utilisera les basses fréquences (1–5 MHz) pour les examens d’imageries en profondeur.
- La longueur d’onde : elle agit sur notre onde ultrasonore et est en relation directe avec la fréquence. La longueur d’onde va dépendre de la fréquence et de la célérité. Plus la fréquence va être grande et plus la longueur d’onde est courte ce qui entraînera une meilleure résolution spatiale.
- La vitesse de propagation : elle dépend des propriétés physiques du milieu comme la densité et la compressibilité.
- L'impédance acoustique : l’impédance correspond à la résistance du milieu à la propagation de l’onde US. La différence d’impédance entre deux tissus détermine la réflexion de l’onde US.
- L’intensité : c’est la puissance acoustique transmise par unité de surface. Elle indique l’énergie transportée par l’onde US.
- La puissance : la puissance correspond à la quantité d’énergie émise par la sonde par unité de temps. Elle permet de déterminer la force du signal émis et donc la luminosité de notre image. Cependant, il faut faire attention au risque d’échauffement qui augmente avec une augmentation de la puissance. L’indice thermique permet de vérifier que le risque d’échauffement n’arrive pas.
Maintenant, les principaux paramètres des US définis, détaillons leurs caractéristiques : Dans le cas de l’échographie, des fréquences entre 1 et 50 MHz sont utilisées. Pour les examens des organes se trouvant en profondeur, des US dit basse fréquence sont employés (entre 1 et 5 MHz). L’utilisation de ces basses fréquences permet d’aller voir en profondeur cependant on aura moins de détails sur notre image. Pour les examens de tissus en superficie, ce seront des US haute fréquence utilisés (entre 7 et 15 MHz). Ici c’est l’inverse, la résolution sera bonne mais la pénétration.
Pour la longueur d’onde, plus la fréquence va augmenter et plus la longueur d’onde diminue, de ce fait pour des fréquences comprises entre 1 et 10 MHz, la longueur d’onde varie entre 1.54 mm pour une longueur d’onde de 1 MHz et 0.15 mm pour 10 MHz. La vitesse de propagation dépend du milieu. Dans le cas des ultrasons, les principales valeurs de vitesse sont celles de l’air (340 m/s), les tissus mous (1540 m/s) et les os (3500 m/s).
Pour l’impédance acoustique, elle dépend également du milieu traversé. L’impédance est mesurée en Rayl (kg.m^-2 .s^-1). En reprenant le milieu cité précédemment, dans l’air l’impédance est de 400 Rayl, dans les tissus mous l’impédance est d’environ 1,6 × 10⁶ Rayl et pour les os, elle est de 7,75 × 10⁶.
L’intensité se mesure en W/m². Les valeurs de l’intensité dépendent du mode d'échographie utilisé. En mode B, l’intensité est comprise entre 0.001 et 0.1 W/cm² tandis qu’en doppler pulsé, l’intensité est comprise entre 0,5 et 1 W/cm². Pour finir la puissance qui se mesure en watt dépend du mode et de la profondeur de l’image. Elle est comprise entre 1 et 100 mW.
Il existe également deux indicateurs de sécurité. L’indice mécanique et l’indice thermique. L’indice mécanique est un indicateur du risque des effets mécaniques des US sur les tissus. Cet indice augmente si la pression du faisceau augmente et il diminue quand la fréquence augmente. L’indice thermique est un indicateur du risque d’échauffement tissulaire causé par l’absorption de l’onde US. Les facteurs qui influencent l’indice thermique sont la puissance du faisceau et la durée d’exposition.
Avec les ultrasons de diagnostic, l’indice mécanique doit être inférieur à 1.9 et l’indice thermique doit être inférieur à 1 pour la majorité des examens mais pour certains tissus sensibles (yeux, testicules, moelle épinière), l’indice thermique (TI) doit être inférieur à 0,5. Si jamais l’indice thermique est supérieur à 2 alors on a un vrai risque de surchauffe. Entre 1 et 2, une élévation de 2°C sur le tissu ciblé peut être détectée.
Pour générer ces ultrasons de diagnostic, l’échographe envoie une impulsion électrique brève de l’ordre de la microseconde en direction du cristal piézoélectrique contenu dans la sonde. Celle-ci est constituée de plusieurs centaines de cristaux contenus dans un boîtier permettant de focaliser, diriger notre onde sonore générée. Le cristal piézo-électrique possède une spécificité qui lui permet de se déformer mécaniquement lorsqu’il est soumis à une tension électrique. De plus, lorsque ce cristal est déformé mécaniquement, il produit une tension électrique [3].
Ex : pour une sonde de 3 MHz, alors l’impulsion électrique contiendra des cycles d’oscillation a 3 MHz.
Le cristal va, sous l’effet de la tension électrique, se contracter et se dilater rapidement. Le cristal va donc vibrer, ce qui va générer une onde mécanique. L’onde ultrasonore sera transmise directement dans le milieu en contact avec la sonde. Pour l’échographie, du gel constitué d’eau dégazée afin de supprimer l'impédance de l’air est utilisé et permet aux US de pouvoir pénétrer dans le corps humain.
I.2. Ultrasons thérapeutiques : les paramètres d'utilisations et effets biologiques
Les UST sont des ondes mécaniques longitudinales avec une fréquence comprise entre 0.5 et 3 MHz. Elles sont utilisées pour transmettre de l’énergie aux tissus biologiques afin de produire différents effets thérapeutiques, détaillés par la suite [7]. Pour générer un UST, le même principe que pour les USD est utilisé : l’effet piézo-électrique. Tout commence par la génération d’un signal électrique sinusoïdal d’une certaine fréquence. Ce signal est envoyé selon deux modes :
- En mode continu, le signal est émis en permanence. Ce mode est utilisé lorsque le praticien cherche à obtenir les effets thermiques [8].
- En mode pulsé, le signal est interrompu avec un intervalle de temps régulier. Il est utilisé lorsque le praticien veut obtenir les effets mécaniques avec une faible augmentation de température [8].
Le cristal piézoélectrique oscille mécaniquement et va créer une onde ultrasonore longitudinale qui sera par la suite transmise de la tête de la sonde vers le patient. Si la sonde ne bouge pas alors l’onde va pleinement pénétrer les tissus et le maximum d'énergie est concentré sur la zone cible. Si la sonde est déplacée, l'énergie sera alors diffusée de manière homogène.
Les UST sont des US avec une fréquence beaucoup plus basse que celle des USD. L’objectif est de transmettre de l’énergie directement au tissu afin de produire un effet biologique. Les UST de fréquence comprise entre 0.5 et 1 permettent d’aller plus en profondeur et de traiter des structures profondes. Pour le traitement des tissus en superficie, des fréquences plus élevées comprises entre 2 et 3 MHz, sont utilisées.
En ce qui concerne la longueur d’onde des UST, il s’agit du même principe que pour les USD, plus la fréquence augmente et plus la longueur d’onde diminue. À des fréquences de 0.5 MHz, la longueur d’onde sera d’environ 3.08 mm, pour 1 MHz environ 1.54 mm.
La vitesse de propagation reste la même pour les USD car elle dépend du milieu traversé par l’onde. De même pour l’impédance acoustique.
L'intensité est le paramètre le plus important pour les UST. En effet, il détermine la quantité d’énergie qui sera délivrée aux tissus. En général, l’intensité est comprise entre 0.1 et 3 W/cm². Si un effet thermique est recherché, alors il faut une intensité de minimum 0.8 W/cm² pour que l’échauffement recherché soit significatif (augmentation d’1 à 5 degrés selon la durée d’utilisation des UST) [9]. Pour observer l’effet mécanique, il faut des intensités inférieures à 0.5 W/cm² donc faible, mais pendant une durée beaucoup plus longue (de plusieurs minutes). Enfin si c’est un effet destructif qui est recherché, comme avec l’HIFU, les intensités peuvent atteindre plusieurs centaines voir milliers de W/cm² mais pendant une durée très courte de quelques secondes à 1 minute maximum.
La puissance des UST va également dépendre de la surface à traiter et de la profondeur. En moyenne la puissance émise par la tête de la sonde est comprise entre 1 et 15 W mais, elle peut monter à plusieurs dizaines voire centaines de Watt pour concentrer l’énergie sur une zone bien précise.
Les UST ont plusieurs effets sur les tissus, et certains sont recherchés à atteindre pour obtenir l’effet thérapeutique :
Les effets thermiques : pour obtenir l’échauffement local, l’onde ultrasonore va traverser le tissu biologique cible et une partie de l'énergie de l’onde sera absorbée et convertie en chaleur. Pour que cette conversion se fasse, on aura trois mécanismes principaux :
- L’absorption viscothermique : les tissus n’étant pas totalement élastiques, une partie de l’énergie vibratoire de l’onde est dissipée et est convertie en chaleur. Plus la fréquence augmente et plus l’absorption augmente, de ce fait il y aura un chauffage qui sera plus important en haute fréquence.
- Le frottement au niveau cellulaire : ici, les structures tissulaires oscillent avec l’effet de l’onde. Toutes ces micro-oscillations vont produire des frottements internes qui seront convertis en chaleur.
- Le dernier mécanisme est la relaxation moléculaire : les molécules telles que les protéines ou l’eau absorbent mieux certaines fréquences d’ultrasons. Elles vont convertir l'énergie de l’onde absorbée en chaleur.
Plusieurs paramètres vont agir sur cette production de chaleur. Le paramètre qui agit le plus sur la quantité de chaleur produite est l’intensité acoustique. Plus l’intensité acoustique augmente et plus l’échauffement sera fort et la température augmente brutalement. Pour les tissus en superficie, plus la fréquence est élevée, plus l’absorption sera plus rapide et les tissus chaufferont intensivement [10].
Le mode d’émission agit aussi sur l’effet thermique. Si l’onde ultrasonore est produite en continu, alors la montée thermique sera importante. Cela est utilisé notamment pour le HIFU. Si l’onde est émise en pulsé, l’effet thermique sera réduit. Le mode pulsé est notamment utilisé dans le LIPUS.
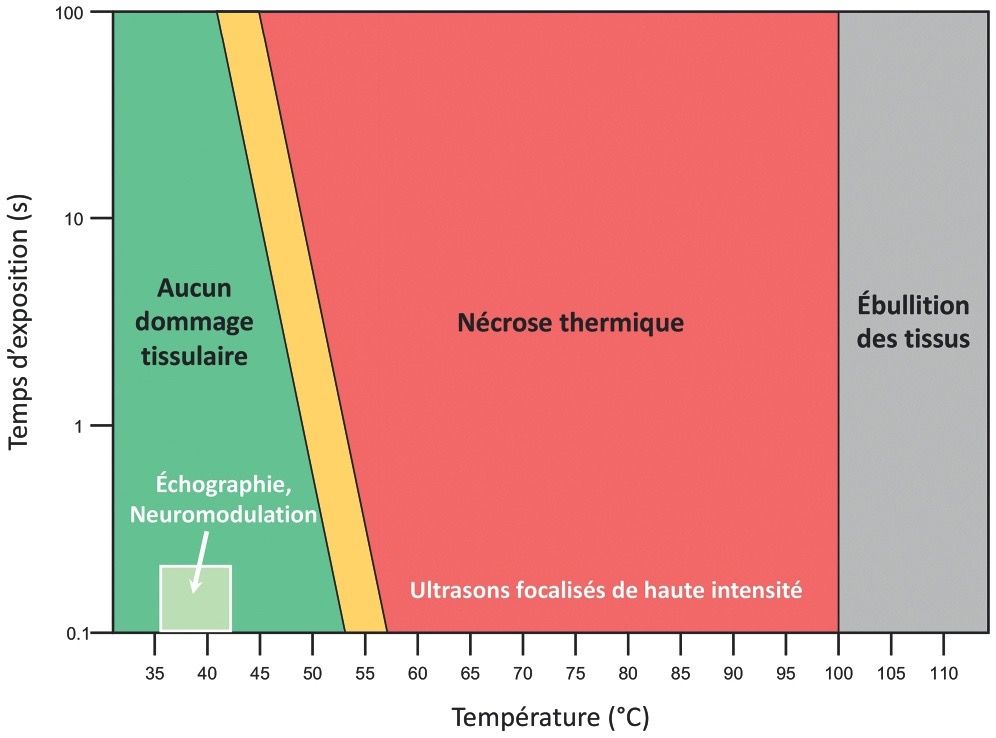
L’effet thermique va avoir plusieurs conséquences sur les tissus et vaisseaux cible. Notamment l’augmentation de la circulation sanguine, de l’apport en oxygène afin de favoriser la réparation et la guérison des tissus. Il peut également avoir un effet de mort cellulaire causé par le chauffage que l’on peut mesurer par la dose thermique comme le montre la figure 1. Pour déterminer cette dose thermique, il faut associer les informations sur le degré et la durée d’augmentation de la température au niveau du tissu cible. Si jamais le seuil d’intensité ou de durée est dépassé, il peut avoir l’apparition d'effets néfastes comme une coagulation ou bien une nécrose des tissus.
Figure 1 : Relation entre la dose thermique et l’effet biologique dans les tissus.
(©David Attali, Physique pour la médecine Paris) [11]
➤ Les effets non-thermiques ou mécaniques : ces effets sont principalement retrouvés lors de l’emploi des US pulsés ou des US à des intensités modérées afin d’éviter une surchauffe.
Il y a 3 effets mécaniques influencés par les US :
- La force de rayonnement [12]: cette force consiste en un transfert de la quantité de mouvement de l’onde aux tissus dû aux différentes interactions de l’onde comme l’absorption, la réflexion ou la diffusion avec le tissu cible. Ici, il y a une pression qui est exercée en continu sur le tissu. Lorsque l’onde est absorbée par le tissu, elle perd de l'énergie tandis que le tissu lui gagne de la quantité de mouvement produite par l’onde ce qui entraîne une poussée. Quand l’onde est réfléchie, le changement de direction de l’onde va produire une poussée qui sera encore plus forte. Il y a également ce phénomène lorsque l’onde est diffusée. De plus, si l’émission est en continu de l’US alors la force sera continue. Si c’est émis en pulsé, la force sera impulsionnelle.
La force de rayonnement agit sur le déplacement des membranes ou du cytosquelette de la cellule et active les canaux ioniques mécanosensibles et les voies de signalisation mécaniques. Ces effets sont très importants pour la régénération osseuse et sont utilisés pour le LIPUS. - Le flux de fluide, ou également appelé streaming acoustique [12]: correspond au mouvement du fluide généré par les US qui va venir créer un courant. L’ultrason va venir créer une poussée continue et le fluide va se mettre à couler. L’écoulement est stable, unidirectionnel et superposé au mouvement vibratoire des particules. Ce flux apparaît à cause d’un déséquilibre des forces dans le fluide. L’onde US crée un champ de pression oscillant qui une fois absorbé va transmettre de la quantité de mouvement au fluide. Cette quantité de mouvement s’additionne et produit une force nette qui donne un courant du fluide stable. Le streaming acoustique va provoquer plusieurs effets. Il y a notamment un déplacement du fluide autour des cellules pour avoir une augmentation du transport d’oxygène, une amélioration de l’élimination des déchets métaboliques. Il y a également le cisaillement de la membrane cellulaire, car le flux va provoquer une traction sur les membranes qui activent les récepteurs mécanosensibles et augmente la perméabilité membranaire. Cela permet d'activer la régénération cellulaire et de faciliter la pénétration des ions calcium. Enfin, pour le LIPUS, il y a un effet de stimulation des fibroblastes et ostéoblaste. En effet, le flux de fluide va contribuer à augmenter la production de prostaglandine E2, la multiplication cellulaire et l’expression des facteurs de croissance qui sont essentiels pour la consolidation des os par le LIPUS.
Le streaming acoustique dépend de plusieurs paramètres de l’échographe notamment : - L’intensité : plus l’intensité est élevée et plus le flux est rapide. Avec le LIPUS, même en faible intensité, le streaming reste efficace.
- La fréquence : plus la fréquence augmente et plus le streaming augmentera également, car en augmentant la fréquence, l’absorption viscothermique augmente et par conséquent la force motrice.
- La durée et le mode d’émission : si l’émission est continue alors le flux sera constant et fort tandis que si l’émission est pulsée (comme c’est le cas pour le LIPUS) alors le flux sera intermittent mais efficace.
Ces 2 effets vont être influencés par l’intensité moyenne temporelle (I SPTA) et la fréquence. De plus, l’atténuation du milieu va influencer la force de rayonnement et la viscosité du liquide va quant à elle agir sur le flux du fluide [12].
-
La cavitation : la cavitation correspond aux oscillations de microbulles de gaz présentes dans le sang sous l’effet d’un champ ultrasonore. Elle permet de moduler temporairement et de façon réversible la perméabilité vasculaire, notamment au niveau du cerveau, en dilatant les jonctions entre cellules endothéliales afin de laisser passer un traitement sans endommager les vaisseaux. On distingue deux formes de cavitation [12]:
La cavitation inertielle apparaît lorsque les bulles se dilatent de manière excessive pendant la phase de basse pression, dépassant parfois plus de deux fois leur taille initiale. Lors de la phase de haute pression, la bulle se contracte brutalement et peut s’effondrer. Cet effondrement peut générer des effets mécaniques susceptibles d’endommager ou de détruire les structures voisines.
La cavitation stable, au contraire, correspond à des oscillations régulières des bulles sous l’effet des ultrasons. Ce régime contrôlé limite le risque de lésions irréversibles et permet une utilisation thérapeutique, notamment pour augmenter de façon transitoire la perméabilité vasculaire.
Tableau 1 : Comparatif entre les US diagnostiques et les US thérapeutiques
| US Thérapeutiques | US Diagnostiques | |
| Fréquence | 0.5-3 MHz (basse fréquence pour transmettre l'énergie au tissu) Entre 0.5-1, traitement des structures en profondeur et entre 2-3, traitement des structures en superficie | 1-5 MHz (basse fréquence) pour observer les structures en profondeur et 7-15 MHz (haute fréquence) pour les structures superficielles |
| Intensité | Entre 0.1 et 3 W/cm². Pour obtenir l’effet thermique, besoin d’une intensité supérieure ou égal a 0.8 W/cm² Pour obtenir un effet mécanique, intensité inférieure à 0.5 W/cm²Pour un effet destructif, intensité de plusieurs centaines voir milliers de W/cm² | Compris entre 0.001 et 0.1 W/cm² |
| Puissance | Entre 1 et 15 WPour le HIFU, plusieurs dizaines ou centaines de Watt | Entre 1 et 100mW |
| Durée d’utilisation | 5 à 15 minutes par zone que l’on traite. Peut monter jusqu'à 30 minutes pour les traitements ciblés | Quelques secondes à 30 min. maximum selon l’examen. (Plus long en obstétrique et cardiologie) mais exposition locale brève car mouvements de la sonde |
| Effets produits | Effets thermiques et mécaniques | Production d’images par réflexion des US sur les différentes structures internes |
| Utilisations | Voir chapitre II.1.3 et II.2.3 | Pour imagerie non invasive et non ionisante en temps réel en obstétrique, cardiologie, vasculaire, etc |
| Risques / indice Sécurité | Risque de brûlure tissulaire, de cavitation non contrôlée. Il faut veiller à ce que l’indice thermique reste modéré et l’indice mécanique est mesuré en permanence pour éviter des risques de cavitation non contrôlée | Index thermique et mécanique en dessous des seuils critiques donc pas de risque potentiel |
| Mode d’émission | Mode continu : la vibration est permanente, utilisé pour obtenir principalement l’effet thermiqueMode pulsé : vibration en intermittence, les effets mécaniques sont prédominants | Mode émission pulsée pour reconstruire une image en temps réel sans risques thermiques ou mécaniques. |
II. Applications des ultrasons thérapeutiques
On distingue 2 techniques d’utilisation des UST : l’HIFU et le LIPUS qui seront présentés dans cette partie.
II.1. High Intensity Focalized Ultrasounds
Étudions à présent la première technique d’UST, l’HIFU ;
II.1.1. Mode d’action : Principe de fonctionnement de la génération de l’onde ultrasonore de haute intensité et focalisée
La technologie HIFU repose sur la production, la conversion et la focalisation de l’énergie ultrasonore de très haute intensité afin de détruire sélectivement des tissus biologiques par élévation thermique et cavitation [13].
Nous avons déjà vu ci-dessus comment générer une onde US. Nous voulons maintenant savoir comment nous obtenons la haute intensité et comment nous focalisons le faisceau afin d’atteindre l’objectif final de destruction sélective de tissus pathologiques.
La conversion électro-mécanique intervient comme expliqué plus haut : le signal électrique alimente un transducteur piézo-électrique. Pour maximiser le rendement, le transducteur est taillé à la fréquence de résonance souhaitée, ce qui permet d’obtenir une amplitude de vibration maximale pour une puissance électrique donnée. Certains dispositifs utilisent des transducteurs multicouches, montés de manière à obtenir de grandes excursions mécaniques avec une tension plus faible. Un système de refroidissement maintient la stabilité thermique et évite la dérive de la fréquence de résonance [14].
Comme décrit plus haut, on cherche à éviter la réflexion des ondes US. C’est pourquoi une couche d’adaptation d’impédance pour optimiser le transfert de l’énergie acoustique et minimiser les pertes. Il y a 2 familles d’HIFU :
- HIFU immersif représenté par la figure 2 (type Haifu JC) : le transducteur est entièrement plongé dans un bain d’eau dégagée situé sous une membrane fine acoustiquement transparente. Le patient repose directement sur cette membrane, qui isole l’eau mais laisse passer les US. Le transducteur, monté sur un dispositif motorisé, se déplace dans l’eau pour venir se positionner au plus près de la membrane et focaliser précisément le faisceau sur la zone cible ;
- HIFU à contact direct : à l’inverse, la tête US est appliquée sur la peau. Un gel d’échographie sert de couche d’adaptation.
La focalisation de l’énergie acoustique poussée à l’extrême est la spécificité de l’HIFU [15].
On distingue 2 approches :
- Transducteur concave mono-faisceau : la surface émettrice est façonnée en calotte sphérique, permettant la convergence géométrique des ondes vers un foyer fixe.
- Réseau multi-éléments (phased array) : constitué de nombreux petits éléments piézo-électriques indépendants, il permet de piloter électroniquement la focalisation et de déplacer le foyer en 3 dimensions grâce à un contrôle de phase précis. Au point focal, les ondes se superposent en phase, créant une pression acoustique extrêmement élevée, suffisante pour provoquer une élévation focale de température, entre 60 et 90°C, et la destruction des cellules cibles.
Figure 2 : Exemple d’une machine HIFU immersive avec système échographique embarqué avec le détail de chacun des éléments la composant : appareil JC200 de Chongqing Haifu Company [16]
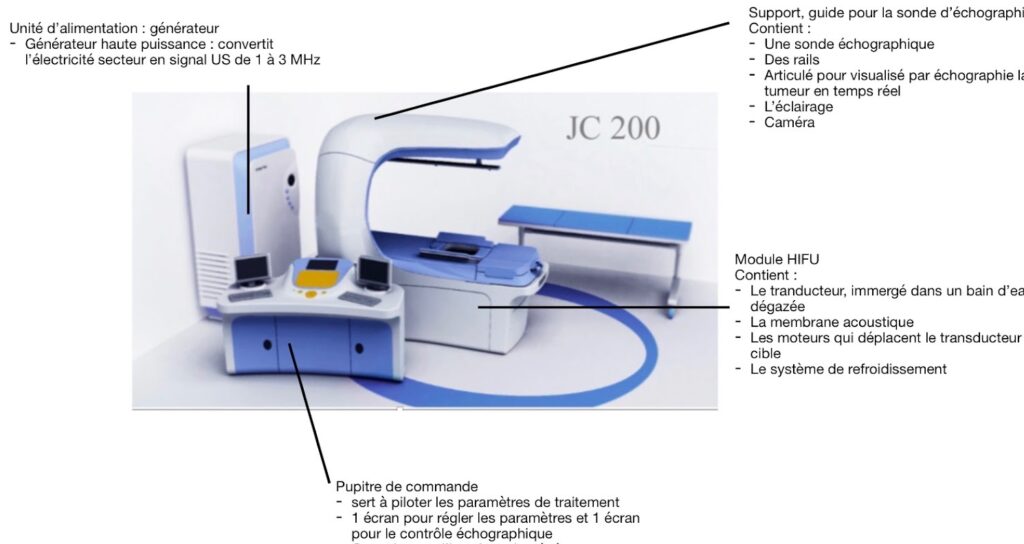
II.1.2. Caractéristiques technologiques de l’HIFU
L’architecture générale du système se compose généralement de trois unités principales : l’unité de génération et de contrôle d’énergie, comprenant les alimentations haute tension, le générateur RF, l’amplificateur de puissance et les circuits de commande des transducteurs. L’unité d’émission acoustique, intégrant le ou les transducteurs HIFU (fixes ou multi-éléments) et le système de couplage patient (eau dégazée, membrane ou ballon souple afin d’assurer une transmission maximisée des ondes US entre le transducteur et les tissus). L’unité d’imagerie et de pilotage, qui assure la planification, le guidage, la visualisation et la boucle de rétroaction pendant le traitement.
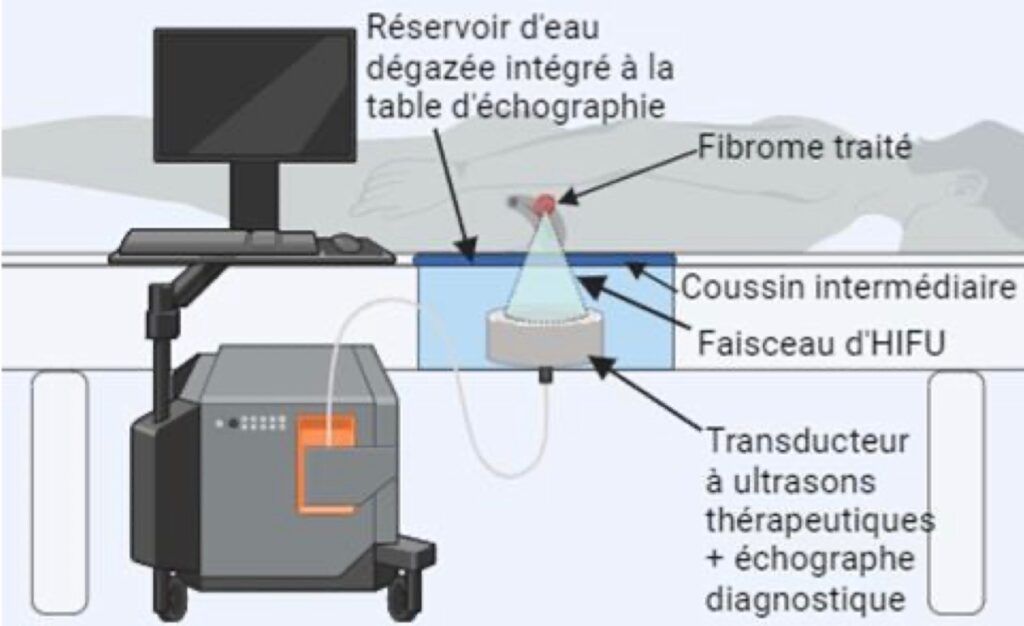
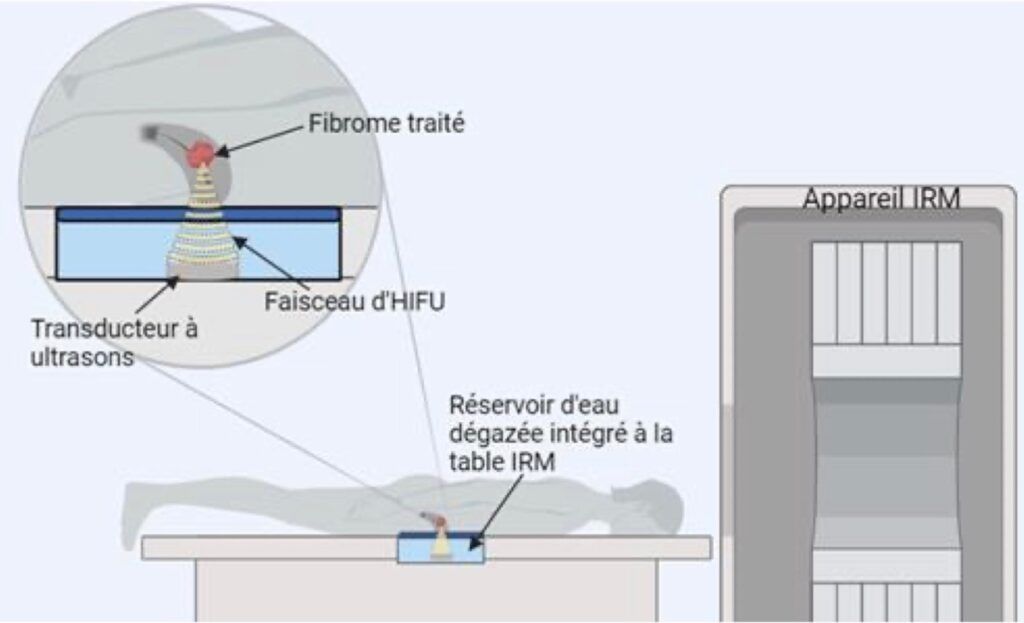
Le système d’imagerie embarquée associé à l’HIFU repose soit sur une échographie en temps réel (via une sonde d’USD intégrée), soit sur une IRM, dans laquelle l’appareil est placé dans le tunnel afin d’assurer un guidage par cartographie thermique (figure 3). Ce système d’imagerie permet de localiser précisément la cible (prostate, fibrome, tumeur hépatique), d’assurer le suivi thermique en temps réel et de contrôler le déplacement du foyer acoustique.
Figure 3 : Exemple de configuration HIFU pour le traitement de fibromes utérins [17]
L’interface et la commande logicielle du système HIFU reposent sur un poste opérateur équipé d’un logiciel de planification incluant la segmentation anatomique et la définition du volume cible, à l’image des traitements de radiothérapie (figure 4 et figure 5). Ce logiciel contrôle automatiquement la puissance, la durée, la position du foyer et la fréquence de tir. Une boucle de sécurité interrompt le traitement en cas de surchauffe, de déviation du faisceau ou d’anomalie de réflexion. Le transducteur peut être robotisé pour un positionnement précis, tandis que l’interface affiche en continu les données d’imagerie et de température.
Figure 4 : Exemple de délinéation des volumes d’un fibrome utérin dans le cadre d’un traitement par HIFU [18]
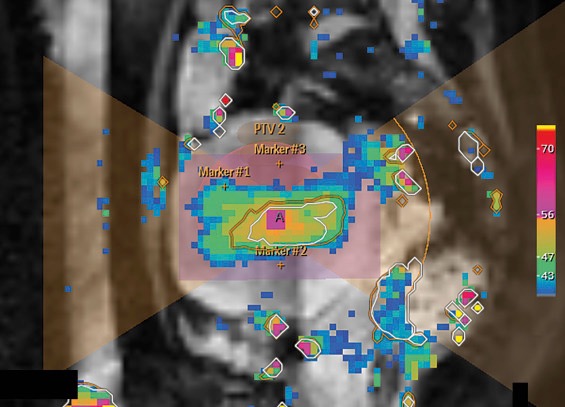
Figure 5 : Interface de planification de traitement par HIFU d’une tumeur prostatique [19]
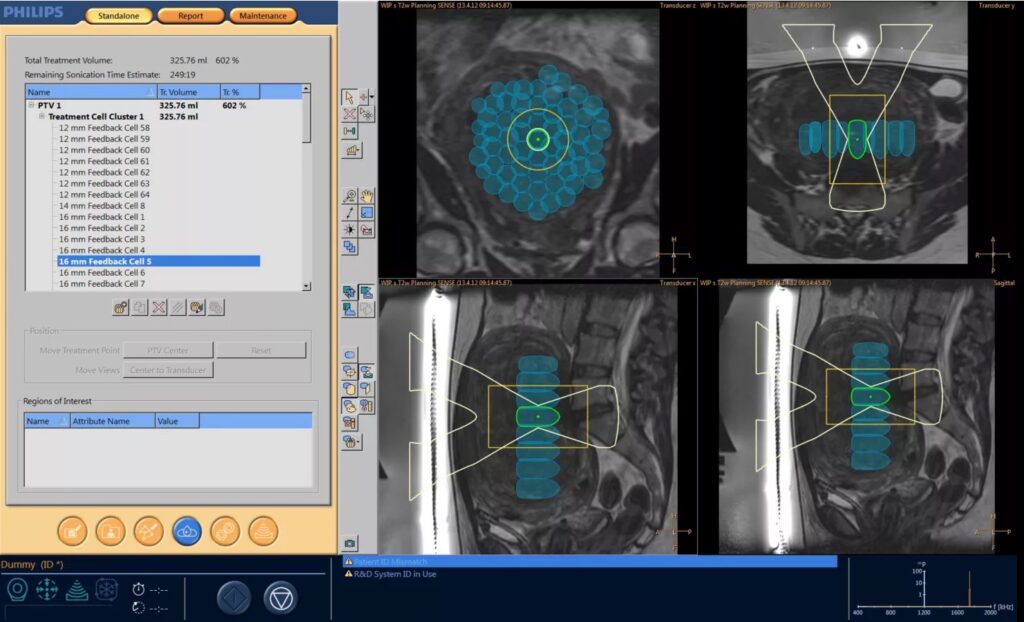
En ce qui concerne la sécurité, des capteurs thermiques assurent la protection du transducteur et de la peau, avec refroidissement actif. Le système mesure la puissance réfléchie pour détecter tout défaut de couplage ou présence d’air.
L'indice mécanique est largement supérieur à la valeur de référence précédemment citée surtout dans ce cadre, afin d’avoir l’effet de cavitation pour détruire les tissus cibles. L’indice thermique est également supérieur à celui des USD. Ici, il sera compris entre 1 et 5 pour avoir une augmentation volontaire de 1 à 5 degrés. En HIFU, il y a une augmentation du TI supérieure à 10 pour provoquer une chauffe rapide et faire coaguler ou nécroser le tissu.
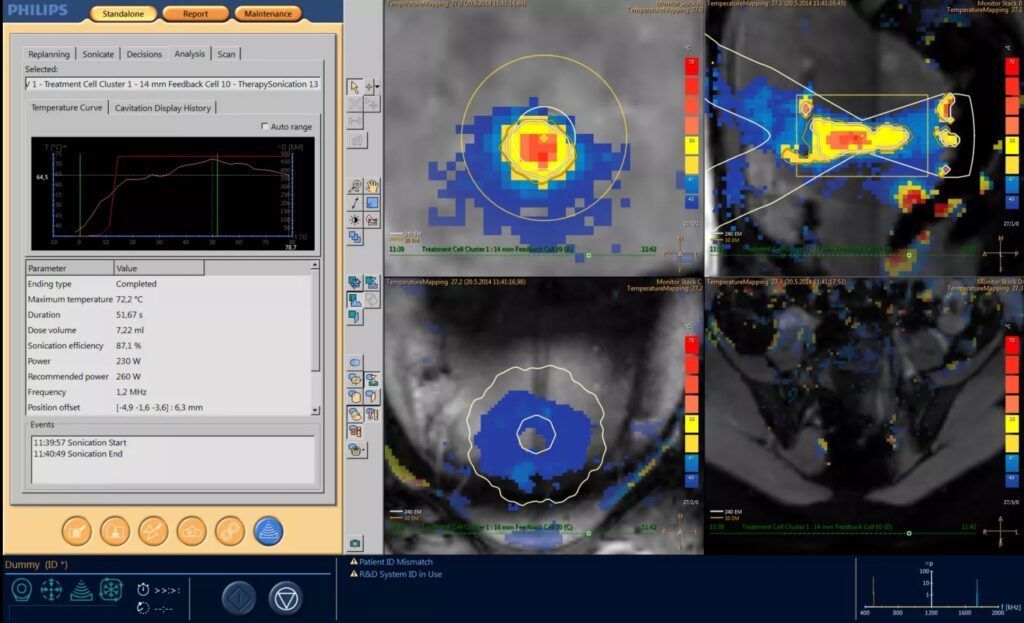
Parfois, la procédure se déroule directement sous IRM. Cela permet d’utiliser des séquences sensibles à la température pour suivre en temps réel l’échauffement des tissus, tout en contrôlant précisément la position du patient. Ce guidage continu aide à maintenir le ciblage optimal du volume à traiter et à sécuriser l’ensemble du geste (figure 6).
Figure 6 : Interface de contrôle de la température par IRM d’un traitement par HIFU de tumeur prostatique [19]
II.1.3. Applications cliniques de l’HIFU
Après avoir décrit plus haut les différents effets physiques induits par les ultrasons sur les tissus biologiques, nous pouvons à présent examiner la manière dont ces phénomènes se manifestent spécifiquement en HIFU et comment ceux-ci sont exploités en pratique clinique. En HIFU, les effets thermiques et mécaniques sont recherchés.
Lorsqu’une onde US de haute intensité est focalisée en un point unique, l’énergie acoustique déposée dans les tissus est en majorité convertie en chaleur par absorption. Au foyer, la densité de puissance est telle que la température peut atteindre 60 à 90°C en quelques secondes, seuil à partir duquel la coagulation protéique, la dénaturation des structures cellules et une nécrose de coagulation apparaissent de manière localisée. L’effet se produit dans quelques mm³, tandis que les tissus traversés avant le point focal ne subissent qu’un échauffement modéré grâce à la focalisation du faisceau et la différence importante d’intensité entre le foyer et les zones périphériques [20].
Les effets thermiques constituent le mécanisme principal recherché dans la majorité des indications cliniques suivantes :
En oncologie, le HIFU permet de détruire sélectivement des tumeurs tout en limitant les lésions des tissus adjacents. Dans le cancer de la prostate localisé, il peut être appliqué en traitement focal ou total. La technique est évaluée pour des tumeurs hépatiques, pancréatiques, rénales ou mammaires, notamment chez des patients non opérables. En soins palliatifs, il est utilisé pour les métastases osseuses dans un objectif antalgique, via une dénervation thermique [21].
En gynécologie, le HIFU permet le traitement non invasif des léiomyomes et fibromes utérins, avec un excellent profil de tolérance [22].
En neurochirurgie fonctionnelle, sous guidage IRM, il permet des thalamotomies non invasives dans les tremblements essentiels ou certaines formes de maladie de Parkinson, avec un ciblage millimétrique. Des travaux explorent également l’ablation de foyers épileptogènes [23].
Finalement, les effets thermiques reposent sur 3 phénomènes :
- le dépôt d’énergie rapide, proportionnel à l’absorption acoustique du tissu,
- la montée en température très localisée, et limitée par la diffusion thermique latérale,
- et les effets irréversibles (coagulation, nécrose), lorsque le seuil thermique est atteint.
Figure 7 : Evolution des bulles de cavitation selon la pression acoustique : cavitation stable vs cavitation inertielle et leurs effets cellulaires [25]
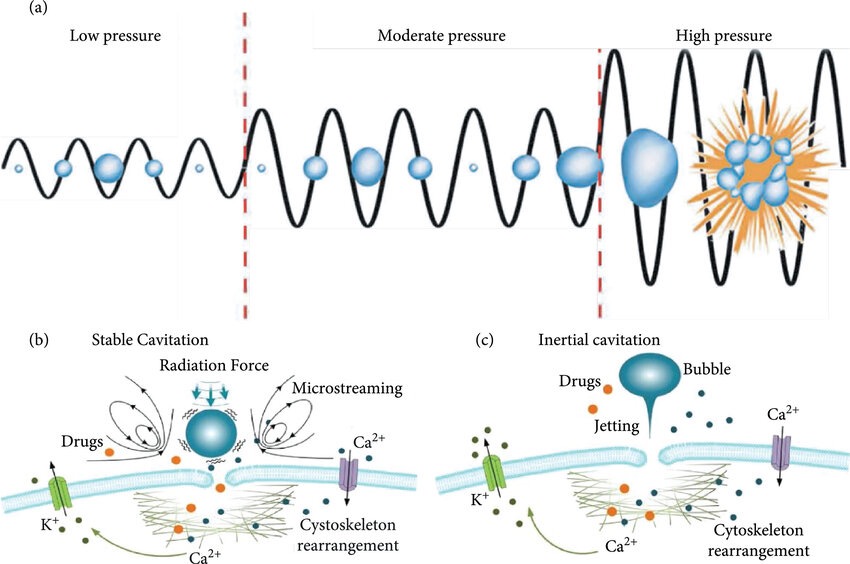
Elle va être utilisée en lithotritie extracorporelle par exemple pour détruire des calculs rénaux. Cet effet peu contrôlable va être délibérément évité lorsqu’on recherche à faire de l’HIFU thermique afin de préserver la précision de la lésion. Cependant, ce phénomène est volontairement recherché dans certaines techniques d’HIFU mécanique, dont l’exemple le plus abouti est l’histotripsie [26]. Cette approche utilise de très courtes impulsions de haute pression pour générer un nuage dense de bulles qui s’effondrent de manière synchronisée, produisant des micro-jets et des ondes de choc capables de fragmenter sélectivement des tissus mous. L’histotripsie est étudiée pour la destruction mécanique de tissus hépatiques ou rénaux, mais également pour des applications en cardiologie structurelle. Dans ce contexte, la cavitation inertielle constitue le mécanisme central du traitement, contrairement au HIFU thermique traditionnel qui repose sur l’élévation de température.
Au-delà de ses usages en oncologie ou neurologie cités ci-dessus, l’HIFU trouve également des applications émergentes en cardiologie pour le traitement des rétrécissements vasculaire aortique pour restaurer la mobilité de cette valve au moyen d’une intervention non invasif sans recourir à la chirurgie de remplacement valvulaire ou le TAVI. Par exemple, le dispositif Valvosoft® (figure 9), encore en phase d’évaluation clinique et non autorisé à être mis sur le marché actuellement, utilise l’HIFU pour assouplir mécaniquement les cuspides aortiques calcifiées. La technique repose sur la fragmentation contrôlée sous échographie des micro-calcifications et une réduction de la rigidité des feuillées, sans création de lésion thermique via des pressions acoustiques élevées sans implosions de bulle, ce sont des effets mécaniques directs de pression dans un régime non thermique.
En réalité, les 2 phénomènes peuvent coexister :
- à basse fréquence et haute intensité, la cavitation domine ;
- à fréquence plus élevée, l’absorption thermique est prépondérante.
Ces exemples illustrent la diversité des domaines concernés par HIFU : plus de 70 indications sont aujourd’hui répertoriées, couvrant quasiment toutes les spécialités médicales (figure 8.
Figure 8 : IRM de fibrome utérin avant (gauche) et après (droite) traitement par HIFU. On observe un centre nécrotique à droite, symbole d’une thermodestruction par les ultrasons [27]
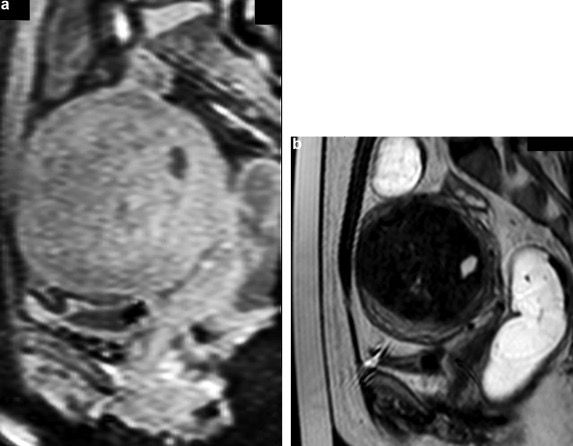
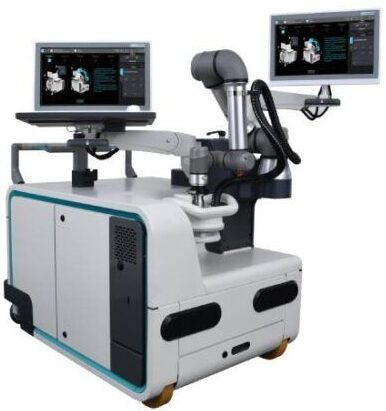
Figure 9 : Machine Valvosoft ® – Cardiawave [28]
II.2. Low Intensity Pulsed Ultrasound
Parlons maintenant de la deuxième technique d’UST.
II.2.1. Mode d’action : Principe de fonctionnement de la génération des ultrasons pulsés à basse intensité
Les ultrasons pulsés à basse intensité sont utilisés pour des applications plus douces comme la stimulation des cellules, communément dans le cadre de la régénération de tissus.
II.2.2. Caractéristiques technologiques du LIPUS
La composition d’un dispositif LIPUS présente plusieurs similitudes structurelles avec les autres appareils ultrasonores, mais se distingue surtout par des choix techniques orientés vers la génération d’ondes de très faible intensité. Comme pour tout système ultrasonore, l’élément central est le transducteur piézoélectrique. Le transducteur électrique utilisé est souvent un disque PZT de 2 à 4 cm de diamètre. Toutefois, contrairement aux transducteurs utilisés en HIFU, qui sont plus massifs, fortement focalisés et conçus pour supporter des puissances élevées, celui du LIPUS est plus léger et optimisé pour vibrer de manière stable à faible amplitude. En interne, il inclut des dispositifs d’amortissement qui permettent de maintenir une émission régulière sans échauffement excessif, ce qui est indispensable pour garantir l’absence d’effet thermique. L’applicateur est par ailleurs plus simple que celui des systèmes HIFU : il n’intègre pas de lentille acoustique ou de géométrie complexe destinée à concentrer l’énergie en profondeur. Il est, au contraire, conçu pour diffuser un faisceau large et homogène, adapté à une stimulation mécanique douce des tissus [30].
Le module électronique de génération du signal constitue une autre différence importante. Un dispositif LIPUS contient un générateur haute fréquence qui délivre un signal très faible et très stable, configuré en mode pulsé avec un cycle d’impulsions précis. Il n’y a pas de gestion des puissances élevées, de systèmes de refroidissement, ainsi que des contrôles de sécurité avancés pour éviter les lésions thermiques comme pour le HIFU. Dans le LIPUS, le refroidissement est minimal, voire inutile, car l’intensité de l’onde est très faible. L’alimentation du dispositif est également simple puisque les appareils LIPUS fonctionnent facilement sur batterie rechargeable, ce qui permet la mise à disposition de dispositifs portables et légers.
Les dispositifs LIPUS comprennent aussi un microcontrôleur destiné à gérer l’émission pulsée, le temps de traitement et les autotests de sécurité. Enfin, l’interface utilisateur de ces appareils reste volontairement minimaliste et adaptée à une utilisation quotidienne même par des patients non spécialistes. Ainsi, même si le HIFU et le LIPUS reposent sur le même principe physique avec l’utilisation d’un transducteur piézoélectrique, la composition d’un dispositif LIPUS est plus légère, moins focalisée, moins énergivore et orientée vers une stimulation mécanique non thermique.
II.2.3. Applications cliniques du LIPUS
Comme expliqué précédemment, les ondes pulsées à basse intensité permettent de stimuler la régénération des tissus. Au fil du temps, la technique a fait ses preuves en application clinique pour différents types de tissus et avec des effets variés. De nouvelles applications plus modernes ont été découvertes après avoir fait le constat que le traitement par LIPUS permettait un certain nombre d’avantages. En effet, il est possible d’utiliser ces traitements de manière répétitive au quotidien, ils ne sont pas invasifs et par sa nature, l’apparition d’effets secondaires néfastes est très peu probable.
Le LIPUS, présenté en figure 10, est utilisé depuis de nombreuses années par les professionnels de santé pour la consolidation du tissu osseux notamment après une fracture. L’utilisation dès le début de la récupération permet d’accélérer la formation du cal osseux jusqu’à 30%. Les retards de consolidation et pseudarthroses peuvent également être traités par LIPUS comme montré en figure 11. L’effet de ces ondes acoustiques sur les cellules ostéoblastiques est la libération de facteurs de croissance [29]. Certains dispositifs utilisés directement par les patients à leur domicile ont également été développés pour permettre un traitement plus fréquent et donc plus rapide et efficace. Les ultrasons pulsés sont également utilisés sur des tissus annexes des os. Ils sont notamment connus pour leur usage dans la régénération de certains tissus mous comme les tendons après une chirurgie post rupture , les ligaments et les cartilages dans certains cas d'arthrose.
Figure 10 : Appareil LIPUS pour la consolidation osseuse [31]
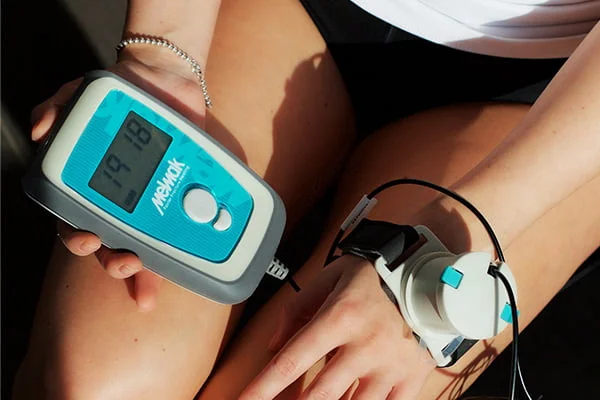
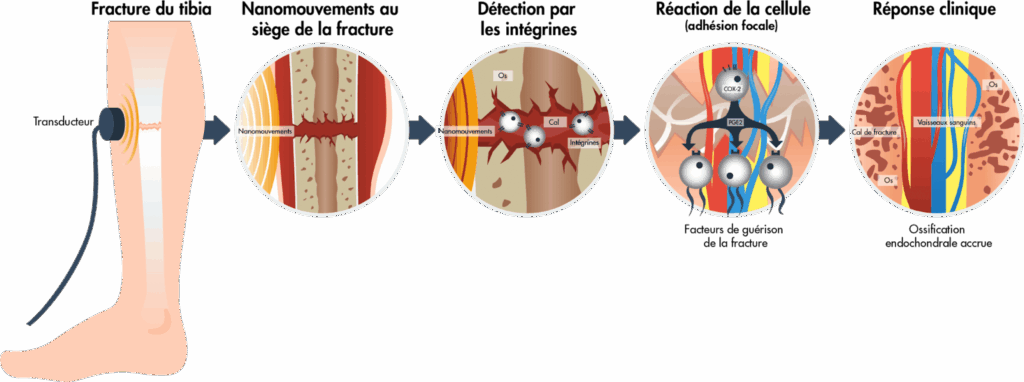
Figure 11 : Schéma de l’effet du LIPUS sur la consolidation d’une fracture [29]
COX-2 = cyclo-oxygénase-2 ; PGE2 = prostaglandine E2
Le LIPUS permet également de stimuler l’angiogenèse, c’est-à-dire la création de nouveaux vaisseaux sanguins. Cette application permet de faciliter le traitement d’affections comme les plaies chroniques pour les patients souffrant de pathologies qui impactent la capacité de cicatrisation comme chez les diabétiques ou les cas d’ulcères [32].
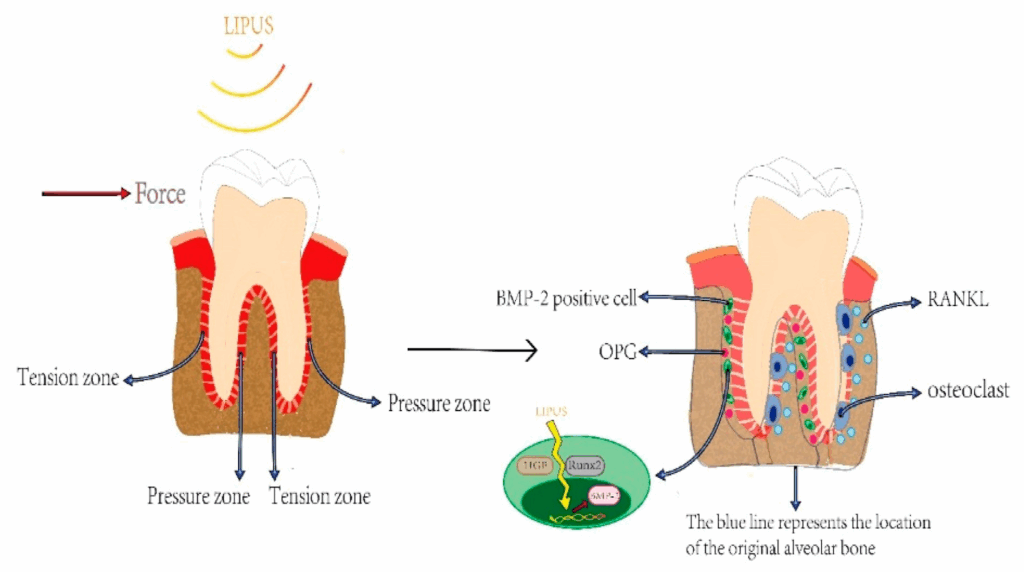
Les ondes pulsées commencent à être étudiées pour ses effets sur d’autres tissus comme le muscle ou la gencive. Les observations mettent en évidence une amélioration de la cicatrisation, une stimulation des cellules impliquées dans la réparation tissulaire et une réduction de l’inflammation locale, ce qui ouvre des perspectives intéressantes en odontologie ou en chirurgie buccale. Le LIPUS est également de plus en plus utilisé en combinaison avec d’autres techniques cliniques pour les soins dentaires comme le montre la figure 12. Elle permet d'accélérer et d’optimiser la cicatrisation après les chirurgies. Les stimulations agissent sur les gencives, le tissu osseux, pulpaire, les tissus mous et ligaments dentaires [33].
Figure 12 : Schéma de l’effet du LIPUS sur le remodelage osseux orthodontique [33]
Dans le domaine nerveux, plusieurs travaux indiquent que le LIPUS pourrait favoriser la récupération après une lésion périphérique en améliorant la régénération axonale et en modulant les réactions inflammatoires autour du nerf atteint, ce qui en ferait un outil potentiel dans la prise en charge des neuropathies traumatiques. Parallèlement, l’utilisation du LIPUS, une forme focalisée à très faible intensité appliquée au cerveau, suscite un intérêt croissant en raison de sa capacité à agir en profondeur de manière non invasive, contrairement aux techniques de neuromodulation plus lourdes. Les premières études explorent ses effets sur l’activité neuronale dans des indications telles que la dépression résistante, certaines maladies neurologiques ou l’épilepsie, avec des résultats encore préliminaires mais prometteurs [34].
Figure 13 : Schéma de la barrière hémato-encéphalique et du passage des molécules au travers de celle-ci [21]
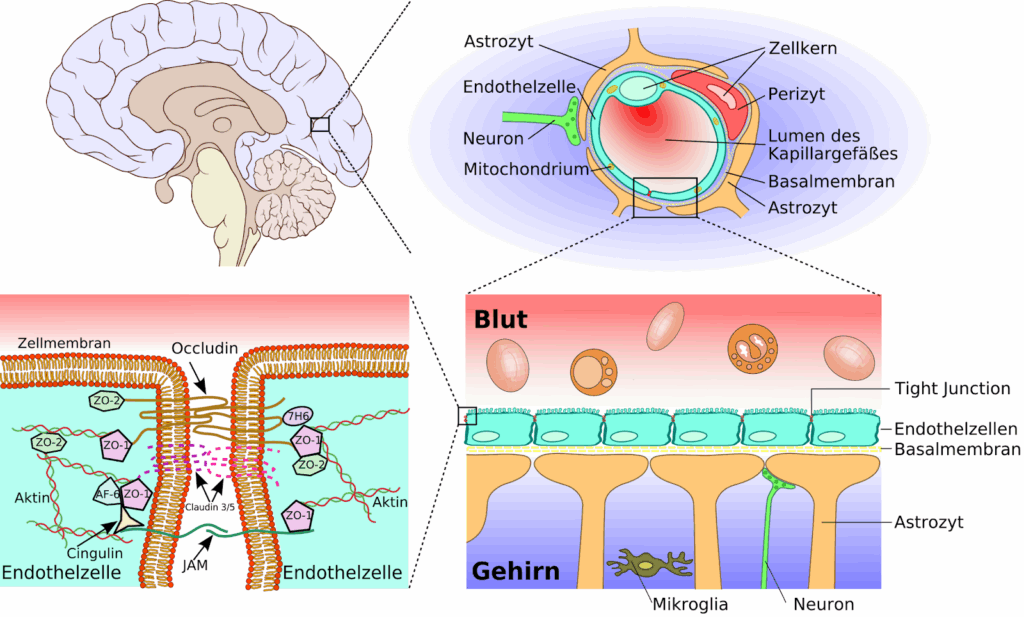
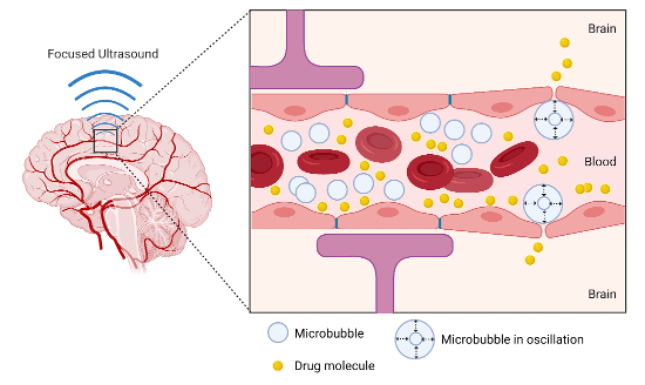
Figure 14 : Schéma de l’ouverture de la BHE par LIPUS associé à des microbulles [37]
Nous avons étudié les technologies LIPUS et HIFU, voici maintenant un tableau comparatif et récapitulatif des propriétés de ces ondes.
Tableau 2 : Comparatif des propriétés des ondes HIFU et LIPUS
| HIFU | LIPUS | |
| Fréquence | 1-10 MHz selon la profondeur des tissus à traiter | 1-1,5 MHz en pratique |
| Intensité | 1000-10 000 W/cm² | 30 mW/cm² |
| Puissance | Plusieurs centaines de watts | Quelques milliwatts à quelques watts |
| Mode | Continu | Pulsé |
| Effets | Majoritairement thermiquesCoagulation et nécrose des tissusCavitation inertielle | MécaniquesActivation de voies de signalisation cellulaireCavitation stable |
| Applications | Ablation thermique de tumeursDestruction ciblée | Stimulation de la régénération tissulaire Administration de thérapeutiquesNeuromodulation |
| Risques | Risques de surchauffe et de lyse tissus sains avoisinants | Pas de chauffe donc pas de véritables risques |
Figure 15 : Comparaison entre l’HIFU et le LIPUS [38]
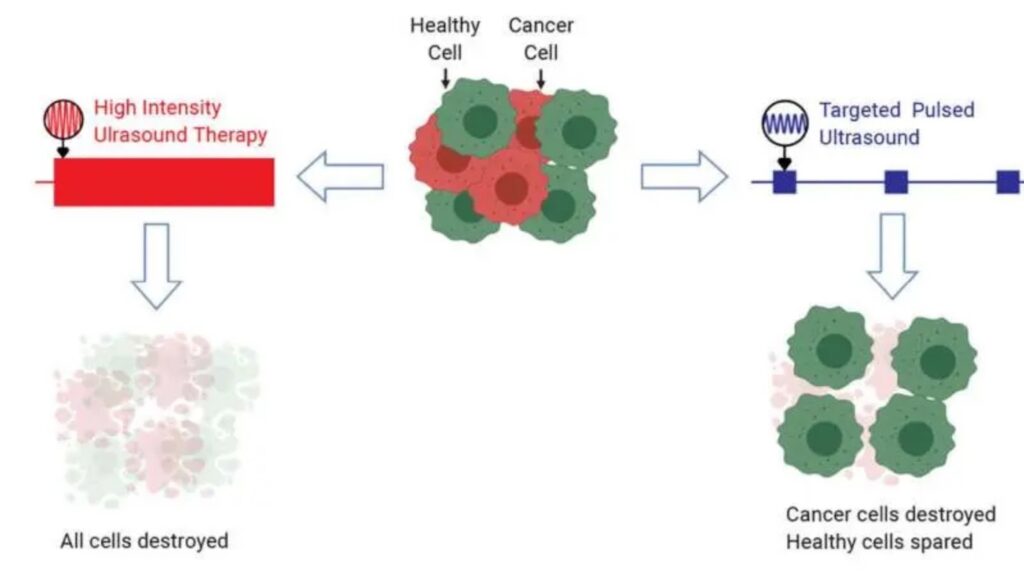
“Les ultrasons pulsés ciblés tirent parti des propriétés mécaniques uniques des cellules cancéreuses, afin de les détruire tout en épargnant les cellules saines. Ce schéma compare l’impact d’une thérapie par ultrasons de haute intensité (à gauche) avec le nouveau type de thérapie proposé, soit à ultrasons de faible intensité (à droite). Dans ce dernier cas, les cellules saines sont épargnées. Crédits : David Mittelstein”
III. Apports, limites et perspectives de l’utilisation des ultrasons thérapeutiques
Les UST, qu’ils soient à haute ou faible intensité, représentent aujourd’hui un véritable progrès dans la prise en charge des patients. Ces deux technologies apportent des alternatives moins invasives, mieux ciblées et potentiellement plus confortables que les approches conventionnelles. Les résultats cliniques témoignent de leur intérêt croissant, mais nécessitent d’aller encore plus loin.
III.1. Apports des ultrasons thérapeutiques vis-à-vis approches conventionnelles
Les UST offrent une solution innovante à de nombreuses contraintes des thérapies traditionnelles, notamment pour les affections où l'accès au tissu visé est ardu, tel que le cerveau. Leur contribution principale est leur capacité à fournir de l'énergie ou un effet mécanique de façon ciblée, sur des volumes précisément délimités, à l'instar de la radiothérapie. À l'aide de la visualisation par ultrasons et de la focalisation ultrasonore, on peut traiter des volumes millimétriques ou cibler plusieurs points dans un même organe, tout en préservant au mieux les structures saines avoisinantes. L'intégration des UST à une approche de médecine dirigée par l'image représente un autre atout crucial. Les techniques récentes fusionnent l'imagerie par résonance magnétique et le scanner afin de créer une réplique numérique du cerveau, ce qui permet d'intégrer la variabilité anatomique du crâne (telle que l'épaisseur et la densité osseuse) et de rectifier les distorsions acoustiques. Ce jumeau numérique offre une assistance pour la neuronavigation : l'opérateur est ainsi capable de placer la sonde à ultrasons avec une exactitude millimétrique et d'établir les volumes cibles à traiter, similaire à la planification en radiothérapie, mais sans faire appel aux radiations ionisantes. Une autre contribution essentielle des UST est leur nature peu ou non invasive. Les interventions se font sans ouverture, généralement sur une simple chaise médicale ou un siège inclinable, en utilisant un dispositif de retenue pour restreindre les mouvements. Cette méthode diminue le danger infectieux, minimise les complications immédiates et ouvre la possibilité de séances successives, ce qui est particulièrement pertinent dans le domaine du cancer ou des maladies chroniques. Dans certains contextes, les UST s'intègrent dans le processus de la radiothérapie ou de la neuro-oncologie, en se servant d'organisations préexistantes (comme les services de radiologie ou de radiothérapie), ce qui simplifie leur incorporation clinique.
Dans le contexte précis du cerveau et de la BHE, les UST proposent une contribution qui n'est pas disponible via d'autres techniques : l'opportunité d'ouvrir temporairement et localement cette barrière pour faciliter le transfert de molécules thérapeutiques qui ne pénètrent généralement pas dans le tissu cérébral (anticorps thérapeutiques, vecteurs de thérapie génique, oligonucléotides antisens, etc.). En associant des impulsions ultrasonores de faible puissance (LIPUS) et l'administration de microbulles de contraste, on peut créer une contrainte mécanique maîtrisée sur la paroi des capillaires cérébraux, ouvrir temporairement les jonctions cellulaires, puis les laisser se refermer d'elles-mêmes. Cette méthode répond à une nécessité médicale fondamentale non comblée : le traitement efficace des tumeurs cérébrales ou des affections neurodégénératives en ciblant le cerveau sans chirurgie lourde.
III.2. Limites actuelles de l’utilisation des ultrasons thérapeutiques
En dépit de leurs nombreux atouts, les UST souffrent toujours de plusieurs contraintes techniques, cliniques et réglementaires qui entravent leur déploiement à grande échelle.
III.2.1. Contraintes physiques et anatomiques
La diffusion des US est fortement liée aux caractéristiques mécaniques des tissus qu'ils traversent. Les réflexions et pertes d'énergie significatives causées par les interfaces osseuses et aériennes (crâne, poumons, intestins) restreignent l'efficacité dans certaines régions anatomiques. Pour le cerveau, la diversité individuelle du crâne (épaisseur, densité, structure osseuse) peut engendrer des distorsions acoustiques susceptibles de dérouter le rayon focalisé. Afin de remédier à ces effets, les systèmes les plus récents mettent en œuvre une calibration basée sur un jumeau numérique (fusion IRM-Scanner) qui rectifie partiellement la diffusion à travers l'os. Toutefois, cette compensation n'est pas sans imperfections et exige une modélisation complexe, ce qui entraîne une consommation de temps de calcul et une dépendance vis-à-vis du logiciel.
III.2.2. Maîtrise de la dose ultrasonore
La dosimétrie dans ce cadre n'est pas encore entièrement normalisée. À l'opposé de la radiothérapie, qui fournit une dose mesurable et répétable, la quantité d'énergie véritablement transmise aux tissus est influencée par une multitude de facteurs (intensité, fréquence, absorption, perfusion). Dans des applications telles que l'ouverture de la BHE, une intensité excessive peut causer une cavitation inertielle et induire des micro-dégâts au niveau des capillaires. En revanche, une intensité trop basse rend le traitement inefficace. Les dispositifs les plus récents intègrent une écoute acoustique en temps réel pour ajuster automatiquement la puissance et rester dans le régime de cavitation stable, limitant ainsi les risques vasculaires. Cette surveillance améliore la sécurité, mais complexifie la conception matérielle et logicielle.
III.2.3. Fenêtre thérapeutique et efficacité biologique
L'ouverture de la BHE par LIPUS reste une mesure temporaire : elle dure quelques minutes pour les molécules de grande taille, et peut aller jusqu'à plusieurs heures pour les plus petites. Cette restriction nécessite un alignement précis entre la sonification et la concentration plasmatique maximale du médicament administré par injection intraveineuse. Une erreur de synchronisation diminue considérablement l'efficacité du passage médicamenteux. En outre, certains effets secondaires biologiques ont été notés, y compris une neuroinflammation stérile passagère associée à une activation temporaire des cellules microgliales. Bien que cette réaction soit généralement bénigne, il est important de la surveiller pour prévenir les risques accumulés lors de traitements répétés.
III.2.4. Aspects techniques et ergonomiques
Les systèmes HIFU et LIPUS de nouvelle génération s'appuient sur une électronique de puissance sophistiquée, un contrôle à multiples émetteurs et des détecteurs acoustiques intégrés. La calibration et l'entretien de ces équipements demandent une compétence technique approfondie. Il faut rester constamment vigilant face aux contraintes associées au refroidissement, à la stabilité de la fréquence de résonance et à la qualité du couplage acoustique. Parallèlement, le positionnement du patient et la précision extrême du faisceau exigent une immobilisation stricte (chaise ou minerve), ce qui peut s'avérer inconfortable ou restrictif pour certaines populations, en particulier les enfants.
III.2.5. Limites réglementaires et d’adoption clinique
Comme vu dans l’introduction, les UST nécessitent une adhésion à plus de vingt normes (ISO 13485, IEC 60601, ISO 14971, exigences de cybersécurité et RGPD). Cette obligation réglementaire retarde fréquemment les études cliniques et l'introduction sur le marché. En outre, le prix d'achat élevé, la formation requise pour le personnel et la rareté des IRM entravent leur propagation. Même si des solutions alternatives à l'IRM, comme la neuronavigation et le jumeau numérique, atténuent ces restrictions, leur adoption demeure principalement dans les centres spécialisés.
III.2.6. Limites cliniques et médico-économiques
Les éléments cliniques restent variés en fonction des indications. Tandis que les résultats concernant les fibromes utérins, la prostate ou les douleurs osseuses sont prometteurs, les informations sur les applications neurologiques demeurent restreintes. Les preuves thérapeutiques, les critères de remboursement et la justification du rapport coût-efficacité ne sont pas encore suffisants pour une mise en œuvre à grande échelle. Par ailleurs, les tests en cours devront valider la répétabilité, la sécurité cumulative et la pérennité des effets.
III.3. Innovations actuelles : Vers une intégration complète des ultrasons thérapeutiques dans la chaîne de soin
Les évolutions récentes des UST portent principalement sur l’optimisation du ciblage, l’amélioration de l’accessibilité clinique, le renforcement des preuves thérapeutiques et l’intégration progressive de l’IA dans la chaîne de soin.
III.3.1 Vers une planification proche de la radiothérapie
Une première perspective importante consiste à rapprocher la planification des UST de celle utilisée en radiothérapie. L’objectif est de :
- Définir des volumes cibles (tumeur, zone de relais, régions à risque) à partir d’images multimodales (IRM, scanner, éventuellement TEP)
- Déterminer précisément les contours des tumeurs et des structures à préserver.
- Planifier la trajectoire et les paramètres des tirs d’US (position des foyers, nombre de tirs, intensité, durée) de façon systématique et reproductible.
III.3.2. Accessibilité et acceptabilité
Une autre perspective concerne l’accessibilité des UST. Les dispositifs tendent à évoluer vers des systèmes plus compacts, intégrables en service de radiologie ou de radiothérapie, avec des interfaces simplifiées et des protocoles standardisés. L’objectif est de réduire la dépendance aux équipements lourds (IRM dédiées, salles spécialisées) et de permettre une utilisation plus large en routine. L’acceptabilité par les patients est aussi un enjeu : positionnement plus confortable, durée de séance raisonnable, réduction du bruit et des contraintes d’immobilisation. Une meilleure information sur le caractère non invasif, l’absence de rayonnement ionisant et la possibilité de répéter les séances peut également améliorer l’adhésion aux traitements par UST, en particulier dans les pathologies chroniques.
III.3.3. Renforcement des preuves thérapeutiques
Pour que les UST puissent occuper une position stable dans les stratégies thérapeutiques, il est indispensable d'intensifier les preuves cliniques. Les orientations envisagées comprennent : la réalisation d'études multicentriques comparant l'UST combiné à un traitement standard, avec le traitement standard seul, l'établissement d'indicateurs solides (tels que la survie globale, la survie sans progression, le contrôle local et la qualité de vie), la création de registres de patients pour suivre la sécurité et l'efficacité sur une longue période. Ces informations sont essentielles pour persuader les décideurs, les institutions de santé et les financeurs, afin d'obtenir un remboursement organisé et une inclusion dans les recommandations de bonnes pratiques. La diffusion grand public d’appareils à ultrasons vendus pour une vingtaine d’euros sur des plateformes commerciales interroge sur la crédibilité des technologies médicales basées sur les ultrasons. Cette accessibilité crée une confusion entre dispositifs réglementés, validés cliniquement, et gadgets grand public sans encadrement ni preuves scientifiques tangibles à visée quasi exclusivement esthétique. Bien que nous l’ayons exclu de notre étude, la kinésithérapie reste un bon exemple dans ce contexte. Les UST sont utilisés depuis plusieurs décennies, mais leurs bénéfices restent limités. Les méta-analyses récentes montrent une efficacité faible ou incertaine dans la majorité des indications (tendinopathies, douleurs lombaires, cicatrices), et de nombreuses études plus anciennes souffraient d’un manque de rigueur méthodologique, entraînant des conclusions trop optimistes. Cette situation alimente une perception ambivalente : d’un côté, la technologie semble banalisée ; de l’autre, son intérêt clinique apparaît nuancé et très dépendant du niveau de preuve ce qui appuie nos choix.
III.3.4. Intégration de l’intelligence artificielle dans la chaîne de soin
L’intelligence artificielle (IA) représente un axe majeur d’innovation pour les UST. Plusieurs applications sont envisagées :
- Segmentation automatique des tumeurs et des organes à risque à partir des images IRM ou scanner, afin d’accélérer et d'homogénéiser la délinéation des volumes cibles. En ce qui concerne la planification des traitements (suggérer automatiquement les paramètres de l'US, perfectionner le placement des foyers, simuler la propagation dans les tissus). Contrôle en temps réel pendant la séance : analyse des signaux acoustiques, détection précoce d’un régime de cavitation dangereux, ajustement automatique de la puissance ou de la position du faisceau.
- Modélisation prédictive de la réaction tissulaire (probabilité d’ouverture de la BHE, probabilité de contrôle tumoral, danger d’incident).
Conclusion
L’étude que nous avons menée sur les UST met en lumière l’ampleur des progrès accomplis depuis les premières découvertes de la piézoélectricité jusqu’aux technologies modernes de traitements. Cette évolution traduit la convergence de la physique, de la biologie cellulaire, de l’ingénierie et de la médecine, ouvrant ainsi la voie à une approche de soin innovante, non invasive et ciblée, répondant alors aux nouvelles méthodes de prise en soin des patients.
Les UST reposent sur un principe physique simple, mais mobilisent des technologies sophistiquées. Les deux grandes modalités que nous avons étudiées, l’HIFU et le LIPUS, illustrent la diversité des applications possibles à ce jour. Ces techniques permettent aujourd’hui d’envisager des traitements ciblés pour diverses pathologies : de la neurologie, à l’oncologie en passant par la cardiologie.
Cependant, ces avancées s’accompagnent de limites et défis. La maîtrise de la “dose ultrasonore”, la standardisation des protocoles, la précision de la zone à traiter ou encore la détermination de l’utilisateur final demeurent des enjeux pour garantir la sécurité et la reproductibilité des traitements.
Ouverture
L’évolution des ultrasons thérapeutiques invite désormais à s’intéresser aux étapes qui permettront leur passage d’innovations prometteuses à outils pleinement intégrés dans la pratique clinique. Les travaux en cours, qu’ils concernent la standardisation des protocoles, le guidage par l’image ou la modélisation de la propagation ultrasonore, montrent que cette technologie reste en construction. Les recherches futures devront préciser les indications où les UST apportent une valeur ajoutée mesurable, consolider les données cliniques et définir les conditions d’une utilisation sécurisée, reproductible et accessible. Dans cette perspective, l’intégration progressive de l’intelligence artificielle, l’amélioration des systèmes de navigation et l’étude de nouvelles applications thérapeutiques constituent des pistes majeures.