IDS300 – Les innovations biomédicales au service de la prise en charge d'urgence de l'AVC
DOI mémoire
https://doi.org/10.34746/ids300Catégories
Les projets ou stages publiés auxquels vous accédez sont des rapports d'étudiants et doivent être pris comme tels. Il peuvent donc comporter des imperfections ou des imprécisions que tout lecteur doit admettre et donc supporter. Il ont été réalisés pendant les périodes de formation et constituent avant-tout des travaux de compilation bibliographique, d'initiation et d'analyse sur des thématiques associées aux concepts, méthodes, outils et expériences sur les démarches qualité dans les organisations ou sur les technologies en santé.
Si, malgré nos précautions, vous avez des raisons de contester ce droit de diffusion libre, merci de nous en faire part (master@utc.fr), nous nous efforcerons d'y apporter une réponse rapide. L'objectif de la présentation des travaux sur le web est de permettre l'accès à l'information et d'augmenter ainsi la qualité des échanges professionnels.
Nous ne faisons aucun usage commercial des travaux de projet ou de stage publiés, par conséquent les citations des informations et l'emploi des outils mis à disposition sont totalement libres. Dans ce cas, nous vous demandons de respecter les règles d'éthique en citant explicitement et complètement vos sources bibliographiques.
Bonne lecture...
Auteurs





Contacts
- Léa EDME : lea.edmepr@gmail.com
- Yanis GHOUAR : yanis.ghouar@tutamail.com
- Margaux IBLED : margaux.ibled59@gmail.com
- Nicolas JOUVET : nicolasjouvet@gmail.com
- Olivia TONAGA : leleneolivia.tonaga@gmail.com
Citation
A rappeler pour tout usage : M. IBLED, L. EDME, O. TONAGA, N. JOUVET, Y. GHOUAR, « Les innovations biomédicales au service de la prise en charge d'urgence de l'AVC », Université de Technologie de Compiègne (France), Master Ingénierie de la Santé, Parcours Technologies Biomédicales et Territoires de Santé, Mémoire de Projet, janvier 2026, https://travaux.master.utc.fr/, réf n° IDS300, https://travaux.master.utc.fr/formations-master/ingenierie-de-la-sante/ids300/, https://doi.org/10.34746/ids300
Résumé
L’Accident Vasculaire Cérébral (AVC) résulte d’une perturbation aiguë de la circulation sanguine cérébrale, entraînant une sous-oxygénation des tissus et des déficits fonctionnels de sévérité variable. En raison de sa forte prévalence et d’une incidence croissante chez les moins de 65 ans, l’AVC constitue un enjeu majeur de santé publique. La dimension temporelle est déterminante : une prise en charge rapide et coordonnée améliore significativement le pronostic et limite les séquelles.
Ce rapport analyse les projets permettant d’optimiser la prise en charge de l’AVC, en intégrant les innovations biomédicales et en renforçant la coordination des soins. Il présente d’abord la physiopathologie de l’AVC, puis la chaîne actuelle de secours et les traitements disponibles selon les types d’AVC. Enfin, il développe les innovations biomédicales utilisables dans le diagnostic, l’orientation et la gestion thérapeutique des patients.
Abstract
Stroke results from an acute disruption of cerebral blood flow, leading to tissue hypoxia and functional impairments of varying severity. Due to its high prevalence and a growing incidence among those under 65, stroke is a major public health issue. Time is a critical factor, as rapid and coordinated care significantly improves outcomes and reduces long-term disability.
This report examines strategies to optimize stroke management by integrating biomedical innovations and enhancing care coordination. It first reviews the pathophysiology of stroke, then details the current emergency chain and treatment options according to stroke type. Finally, it develops biomedical innovations that can be used in the diagnosis, patient triage, and therapeutic interventions.
Téléchargements


Liste des abréviations
- AIT : Accident Ischémique Transitoire
- ALD : Affection de Longues Durées
- APA : Activité Physique Adaptée
- ARS : Agence Régionale de Santé
- ASPHALT : Acute Stroke : prehospital versus in-hospitAL initiation of recanalization Therapy
- AVC : Accident Vasculaire Cérébral
- BOOSTER : Brain clOt persOnalized therapeutic Strategies for sTroke Emergent Reperfusion
- CHU : Centre Hospitalier Universitaire
- DGOS : Direction Générale de l’Offre des Soins
- DICOM : Digital Imaging and Communications in Medicine
- DWI : Diffusion-Weighted Imaging
- ESO : European Stroke Organisation
- FLAIR : FLuid-Attenuated Inversion Recovery
- GHU : Groupes Hospitalo-Universitaires
- HAS : Haute Autorité de Santé
- HDS : Hébergeur de Données de Santé
- INSERM : Institut National de la Santé et de la Recherche Médicale
- IRM : Imagerie à Résonance Magnétique
- LDL : Low-density lipoproteins
- MDPH : Maison Départementale des Personnes Handicapées
- OMS : Organisation Mondiale de la Santé
- PPS : Plan de Soins Personnalisé
- PRME : Programme de Recherche Médico-Economique
- RGPD : Règlement Général sur la Protection des Données
- SAMU : Service d’Aide Médicale d’Urgence
- SAU : Service d’Accueil des Urgences
- SMUR : Service Mobile d’Urgence et de Réanimation
- SFNR : Société Française de Neuroradiologie
- TDM : Tomodensitométrie
- TM : Thrombectomie Mécanique
- UNV(M) : Unité Neurovasculaire (Mobile)
Introduction
L’Accident Vasculaire Cérébral (AVC) correspond à une interruption ou à une altération brutale de la circulation sanguine cérébrale, provoquant une diminution de l’oxygénation d’une zone plus ou moins étendue du cerveau. Cette hypoxie entraîne fréquemment des déficits fonctionnels qui peuvent être moteurs, cognitifs, langagiers ou mnésiques (problèmes de mémoire) et dont la réversibilité dépend étroitement de la durée et de l’étendue de la privation en oxygène.
Cette pathologie est un enjeu majeur de santé publique en raison de sa forte prévalence, et que son incidence chez les moins de 65 ans est en augmentation [1]. L’AVC représente un tournant dans la vie d’un patient atteint, on parle souvent “d’après” AVC, en évoquant une vie bien souvent modifiée.
En effet, l’AVC est la première cause de handicap moteur non traumatique, et la 2ème cause de démence (après la maladie d’Alzheimer) [2]. Sa prise en charge et l’étude des solutions existantes est donc un sujet d’enjeu public. La notion de temporalité est centrale dans la prise en charge de l’AVC, et ce, dès l’apparition des symptômes chez le patient. Plus le patient est intégré rapidement dans la chaîne de soins, plus les chances de récupération fonctionnelle sont élevées.
L’orientation du projet consiste à répondre à la problématique suivante :
Comment optimiser la prise en charge de la phase aiguë de l'AVC ischémique, en intégrant les innovations biomédicales et en améliorant la coordination des soins pour limiter la mortalité et les séquelles des patients ?
Pour répondre à cette problématique, le premier chapitre présentera les bases physiopathologiques de l’AVC ainsi que la prise en charge actuelle, de la prévention en passant par le traitement et finissant par la rééducation. Puis, le second chapitre abordera les innovations biomédicales et organisationnelles récentes, susceptibles de renforcer la rapidité, la précision et l’efficacité du parcours de soins des patients victimes d’un AVC.
I. Comprendre l'AVC : de la physiopathologie à la prévention
1. Contexte et enjeux de la prise en charge de l’AVC
La prise en charge de l’AVC a beaucoup évolué au cours des dernières années. Bien que la pathologie soit ancienne, la structuration de la prise en charge a débuté en 2003, avec un renforcement en 2009 via la création des filières territoriales de soins coordonnées ainsi que par la mise en place d’Unités Neuro-Vasculaires (UNV) [3]. Les UNV, ayant pour but de réunir des équipes spécialisées, ont été renforcées par le Plan d’Actions National AVC 2010-2014.
La Direction Générale de l’Offre des Soins (DGOS) explicite notamment le besoin de coordination des équipes d’intervention d’urgence sur site, mais également au cours de l’hospitalisation du patient concerné, et ce, jusqu’à sa rééducation [4].
Depuis 2015, les UNV sont déployées à travers la France, avec un recensement de 140 unités en 2022 (dont 40 de recours et 100 de proximité) [5]. L’organisation des soins s’est adaptée avec la mise en place de centres d’accueil de neuroradiologie interventionnelle. La Société Française de Neuroradiologie (SFNR) fait état au 1er janvier 2021 de 42 centres d'accueil. Ils sont équipés d’une salle d’angiographie et sont autorisés par l’Agence Régionale de Santé (ARS) à réaliser des actes de thrombectomie mécanique (TM).
La SFNR fait également état de 137 neuroradiologues interventionnels titulaires et 7189 TM réalisées en 2020 [6].
Le vieillissement de la population et l’augmentation des facteurs de risques expliquent la forte prévalence de l’AVC. En 2019, on estime à 12,2 millions le nombre de nouveaux cas d’accident vasculaire cérébral dans le monde, avec 140 000 AVC annuels en France [2,7]. L’AVC est la première cause de handicap chez l’adulte et la deuxième cause de mortalité.
Chez les femmes, l’AVC est la première cause de mortalité [8]. L’enjeu est donc d’améliorer l’accès aux soins pour réduire le nombre de décès et de séquelles liés à cette pathologie.
L’Accident Vasculaire Cérébral est une urgence médicale qui nécessite l’intervention d’équipes de secours formées à cet effet. En effet, on estime que chaque minute, près de 2 millions de neurones meurent lors d’un AVC sévère, d’où l'expression “Time is Brain” [7].
L’appel au 15, Service d’Aide Médicale d’Urgence (SAMU), ou au 112, Numéro d’urgence européen est donc indispensable, car une prise en charge rapide permet de réduire la mortalité de 30% et de limiter les séquelles [9].
Il est possible de distinguer les enjeux selon les quatre acteurs principaux : les patients, les établissements de santé, les autorités sanitaires et les fabricants de dispositifs médicaux.
Pour les patients, une prise en charge rapide et adaptée devrait permettre de réduire la mortalité et limiter les handicaps moteurs et cognitifs. L’objectif est de réduire les délais de prise en charge par une imagerie diagnostique d’urgence et une accessibilité des moyens thérapeutiques. En cas de séquelles irréversibles, la mise en place d’activités rééducatives devrait assurer une réinsertion familiale, sociale et professionnelle. Le suivi post-AVC est donc crucial pour permettre aux patients de s’épanouir malgré cette pathologie.
Pour les établissements de santé, on distingue le Service d’Accueil des Urgences (SAU) de proximité et les Unités Neuro-Vasculaires qui regroupent des équipes pluriprofessionnelles spécialisées dans la prise en charge de l’AVC. Plusieurs problématiques subsistent telles que l’accès à un examen d’imagerie médicale, nécessaire avant de prendre une décision thérapeutique, et qui reste insuffisant avec une offre inégale selon les territoires. De même, les circuits intra-hospitaliers sont parfois inadaptés à une prise en charge en urgence. De nouvelles innovations biomédicales, présentées dans la suite de ce rapport, sont ainsi développées pour améliorer l'offre de soin et favoriser l'égalité d'accès.
Pour les autorités sanitaires, les circulaires du 3 novembre 2003, relatives à la prise en charge des accidents vasculaires cérébraux, et du 22 mars 2007, relatives à la mise en place des UNV dans la prise en charge des patients présentant un AVC ou un Accident Ischémique Transitoire (AIT), ont permis de renforcer l’accès aux soins. La constitution de filières AVC s’inscrit comme un axe majeur du plan national AVC qui a vocation à être décliné et mis en œuvre par chaque ARS en cohérence avec son plan stratégique régional de santé. L’objectif est d’offrir à chaque patient un « Plan de Soins Personnalisé » (PPS). Malgré les moyens déployés, plus de 225 000 personnes sont actuellement classées de façon permanente au régime des Affections de Longues Durées (ALD) du type « accident vasculaire cérébral invalidant » par l’Assurance Maladie [10]. Les travaux menés dans le cadre du Comité de pilotage sur les AVC concluent à une dépense annuelle pour le système de santé d’environ 8,3 milliards d’euros dont 5,9 milliards pour le secteur de soins et 2,4 milliards d’euros pour le secteur médico-social.
Ces chiffres s’expliquent en partie par le taux encore insuffisant de patients pris en charge dans le délai critique de 4h30 suite à l’apparition des premiers symptômes et estimé à 32% [11]. Il s’agit donc d’un enjeu de santé publique complexe et significatif.
Pour les fabricants de dispositifs médicaux, l’innovation au service de l’amélioration des techniques de prise en charge de l’AVC est essentielle pour assurer leur place sur le marché. En plus des progrès possibles sur les modalités d’imageries diagnostiques ou les outils chirurgicaux existants, de nombreux projets cherchent à réorganiser et fluidifier le parcours patient. Il est possible de citer le consortium BOOSTER (Brain clOt persOnalized therapeutic Strategies for sTroke Emergent Reperfusion) lancé en 2019 et qui regroupe des équipes médicales, de recherches et des partenaires industriels. L’objectif est de faire émerger une médecine personnalisée des AVC en situation d'urgence à l’aide d’une analyse sanguine délocalisée (Point of Care). En s’appuyant notamment sur des algorithmes de deep-learning, la stratification des patients en fonction des caractéristiques du caillot est désormais envisageable. Par ailleurs, des travaux sont également menés pour l’exploitation de systèmes non-invasifs et prédictifs des risques d’AVC à partir des caractéristiques vasculaires des patients [12]. Enfin, la récupération neurologique reste un enjeu et un champ de recherche important pour essayer de mieux comprendre les mécanismes de neuroplasticité et d'améliorer la récupération des déficiences.
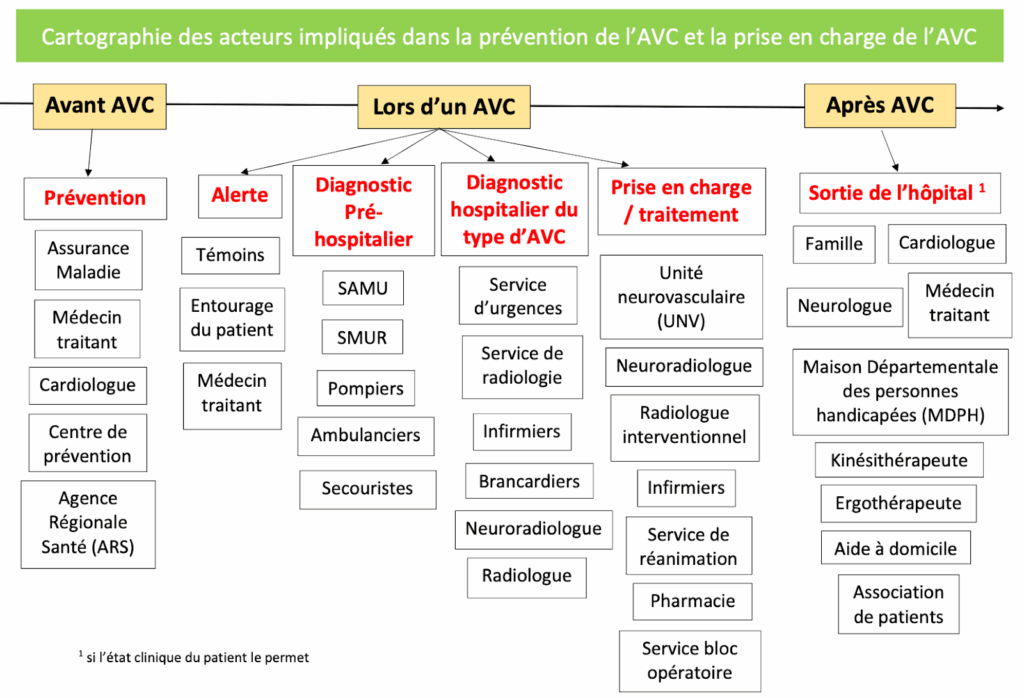
Finalement, il est possible de visualiser l’ensemble des acteurs qui interviennent de la prévention de l’AVC au suivi post-AVC sur la Figure 1 ci-dessous. Cette pluralité d’acteurs montre bien la complexité de la prise en charge de l’AVC, de la prévention au suivi post-AVC.
Figure 1 : Cartographie des acteurs impliqués dans la prise en charge de l’AVC (Source : Auteur.e.s)
2. Généralités et bases physiopathologiques de l’AVC
2.1. Physiologie du système neurovasculaire
Le cerveau est un organe complexe essentiel à la vie. Il permet d’assurer les fonctions motrices (avec le contrôle des muscles volontaires), sensitive et cognitive en gérant la pensée, le langage ou encore la mémoire. Plusieurs lobes sont présents au niveau cérébral, régissant des zones du corps différentes. Lors de la survenue d’un AVC, les zones affectées auront donc des conséquences différentes en fonction du patient. Lorsque l’hémisphère droit est atteint, c’est la moitié controlatérale gauche qui en pâtit, et inversement : on parle de décussation.
La vascularisation du cerveau est très singulière car elle repose sur deux systèmes artériels (carotides internes et artères vertébrales) reliés par le cercle de Willis, une boucle de sécurité qui garantit la continuité de l’irrigation en cas d’obstruction. Elle se distingue aussi par un réseau capillaire spécialisé formant la barrière hémato-encéphalique, protégeant les neurones. Enfin, son organisation dense et constante répond aux besoins énergétiques exceptionnels du cerveau qui consomme près de 20 % de l’énergie corporelle [13].
Différentes artères peuvent être touchées, et il en découle une distinction des types d’AVC, parmi lesquels on trouve : l’infarctus cérébral carotidien, l’infarctus cérébral vertébrobasilaire, les petits infarctus profonds ou « lacunes » profondes, l’infarctus cérébral jonctionnel ou encore la thrombose veineuse cérébrale [14].
2.2. Définition, mécanismes et types d’AVC
L’AVC est une urgence médicale due à l’interruption brutale d’afflux sanguin dans une région cérébrale plus ou moins étendue. Deux types d’AVC peuvent être distingués [7] :
- AVC ischémique : Il représente 85% des cas d’AVC et traduit l’obstruction d’un vaisseau sanguin par thrombose ou embolie. Une thrombose peut se définir comme la formation d’un caillot de sang au niveau d’une veine ou d’une artère, pouvant créer une phlébite quand il y a obstruction d’une veine, ou bien provoquer une embolie s’il y a migration du caillot. Une embolie correspond à la présence d’un caillot, d’une bulle d’air, ou autre substance obstructive d’un vaisseau sanguin cérébrale. L’obstruction empêche le sang d’atteindre certaines zones cérébrales, entraînant alors une privation d’oxygène et de nutriments.
- AVC hémorragique : Il représente 15% des cas d’AVC et traduit la rupture d’un vaisseau sanguin. Cette dernière provoque un épanchement du sang (hémorragie) dans les tissus cérébraux qui sont alors comprimés : la bonne circulation locale est interrompue.
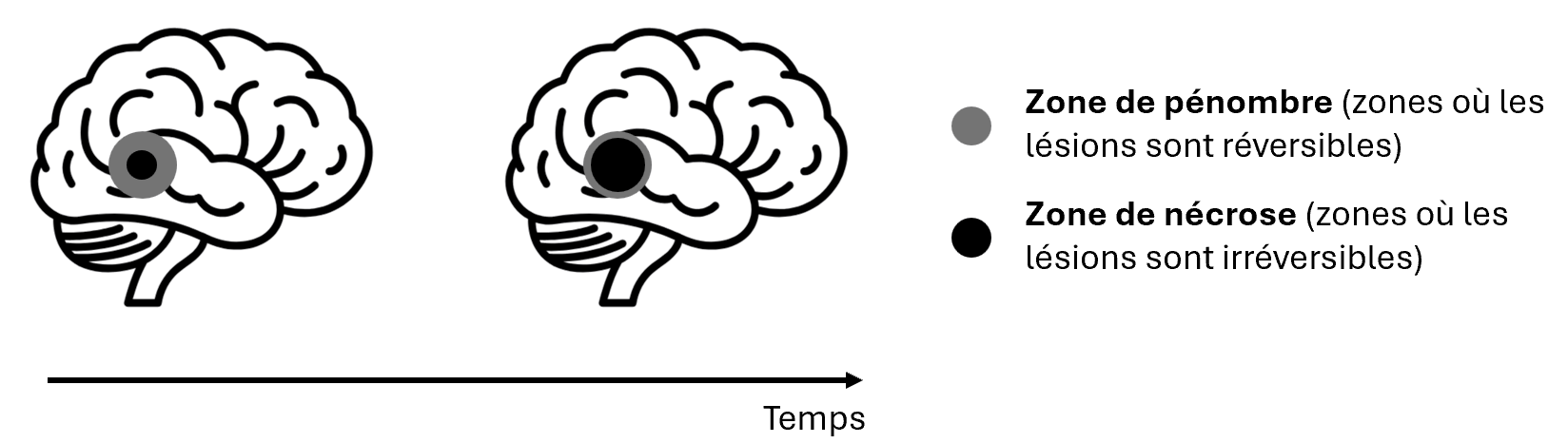
Une fois l’AVC avéré, il faut distinguer la zone cérébrale centrale de la zone périphérique. La zone centrale est l’espace nécrosé qui engendrera la majorité des séquelles neurologiques. La zone autour dite “périphérique” ou “zone de pénombre” est la zone avec des perturbations réversibles. Cette zone tissulaire a été privée de ses besoins de façon temporaire, permettant l’aspect réversible des séquelles du patient [14]. Ces zones sont présentées en Figure 2.
Figure 2 : Zones cérébrales de nécrose et de pénombre atteintes après l’apparition d’un AVC (Source : Auteur.e.s)
Dans le cas où l’afflux sanguin est rétabli dans la zone cérébrale lésée en moins d’une heure, on parle d’AIT, et non d’AVC. Les symptômes, parfois comparés à de simples malaises, ne doivent durer que quelques minutes dans le cas d’un AIT. La répétition de ces derniers et leur durée doivent toutefois être très contrôlées. En effet, le risque de survenue d’un AVC ischémique après un AIT est bien plus élevé qu’en temps normal. L’Institut National de la Santé et de la Recherche Médicale (INSERM) estime à 5% le risque de récidive d’AVC dans les 48 premières heures, et à 10% dans le mois qui suit [7].
3. Manifestations cliniques et facteurs de risque de l’AVC
3.1. Signes cliniques et symptômes de l’AVC
L’AVC est détectable de par différents symptômes tels que [9,15] :
- Faiblesse musculaire et engourdissements pouvant aller jusqu’à la paralysie :
- Engourdissement d’un membre supérieur : la paralysie du bras est le cas le plus fréquent
- Engourdissement d’un membre inférieur
- Déformation et paralysie du visage : lèvre tombante d’un côté par exemple
- Perte partielle ou totale de :
- La vision : oeil unique, perte d’une partie du champ visuel ou vision double
- La parole : troubles de l’élocution et difficultés à trouver ses mots
- Troubles cognitifs : manque de cohérence, difficulté à écouter et à comprendre un interlocuteur
- Maux de tête violents et inhabituels
3.2. Facteurs de risques de l’AVC
Bien que les facteurs de risque de l’AVC correspondent à ceux des maladies cardiovasculaires, l’identification de nouveaux facteurs plus spécifiques doit continuer à être explorée. L’AVC ne survient pas de manière aléatoire. Il est souvent le résultat d’une combinaison de facteurs de risques qui peuvent fragiliser les vaisseaux sanguins ou encore favoriser la formation de caillots dans les vaisseaux. Ces facteurs de risques peuvent être séparés en deux familles : les facteurs dits modifiables et les facteurs dits non modifiables.
Pour les facteurs dits non modifiables, ce sont les facteurs liés à l’hérédité, l’âge ou encore le sexe. Ils ne peuvent donc pas être contrôlés par l’individu. À propos de l’âge, la prévalence en 2022 de l’AVC était de 12% pour les personnes âgées de plus de 85 ans et au global de 2% de la population adulte [1]. En 2009, un rapport du Ministère de la Santé et des sports évoque le fait que le taux d’incidence de l’AVC est multiplié par 2 tous les 10 ans après 55 ans. Ainsi, plus de 50% des AVC surviennent chez les personnes de plus de 75 ans [3]. En plus de l’âge, le sexe est aussi un facteur non modifiable. L’AVC est la première cause de décès chez la femme [8]. Cependant, les études montrent que les hommes ont plus de risque de faire un AVC que la femme. En effet, les femmes représentent 46,8% des cas d’AVC contre 53,2% pour les hommes [1]. Pour finir sur les facteurs dits non modifiables, les antécédents familiaux sont aussi à prendre en compte. En effet, le risque augmente si un parent proche a déjà fait un AVC avant 45 ans [2].
Il existe des facteurs dits modifiables, ce sont les facteurs liés au mode de vie des personnes. Selon des études, 90% des AVC sont associés à un des 10 facteurs de risque modifiables de l’AVC [16]. Les différents facteurs modifiables sont les suivants :
- L’hypertension artérielle : facteur de risque principal. Cela correspond au fait que les parois des artères sont soumises à des pressions élevées du débit sanguin. Il va donc y avoir une fragilisation des artères suite au débit élevé présent. Cela correspond à une valeur systolique égale ou supérieure à 140 mmHg et/ou une valeur diastolique égale ou supérieure à 90 mmHg lors de mesures répétées [17].
- Le diabète : il correspond à un taux de sucre supérieur à 1,26 g/l à jeun lors de 2 mesures [2]. S’il est mal contrôlé, alors il y a une altération des parois des artères et il y a l’apparition d’athérosclérose (formation de plaque d’athérome au niveau des artères et donc entraînant un durcissement de ces dernières) ce qui augmente le risque d’AVC.
- L’hyper-cholestérolémie : cela correspond à un taux élevé de cholestérol (Low-density lipoproteins ou LDL cholesterol). Le LDL est considéré comme du “mauvais cholestérol” puisqu’il s’accumule au niveau des parois des artères. Cela crée donc un ralentissement du débit de la circulation sanguine car il y a une diminution du diamètre des artères. On parle toujours d’athérosclérose.
- Le tabagisme : il altère l’apport en oxygène des parois vasculaires, cela favorise donc l’athérosclérose. Il y a donc un rétrécissement des artères. Le tabac multiplie par 2 le risque d’AVC [2].
- La mesure du tour de taille : si le tour de taille est disproportionné par rapport à la taille de la personne, cela peut être un facteur aggravant.
- L’alcool : la consommation d’alcool peut augmenter la tension artérielle et donc accentuer le risque de faire un AVC.
- L’obésité : l’excès de poids augmente également la tension artérielle, privilégie la présence de LDL cholestérol, mais aussi le diabète. C’est donc un facteur aggravant d’AVC.
- La sédentarité : si il y a une absence d’exercice physique régulier, cela augmente le risque de maladie coronarienne, l’hypertension ou encore l’obésité. Il est donc nécessaire d’avoir une activité physique régulière.
- Les maladies cardiaques : les troubles cardiaques sont des facteurs modifiables.
- Le stress chronique : il accélère le rythme cardiaque et donc cela influence aussi la tension artérielle. Le stress peut aussi amener à consommer du tabac ou à diminuer son activité physique.
Ainsi, plusieurs facteurs sont à l’origine des AVC. Une partie des facteurs ne peut pas être modifiée, comme l’âge, le sexe ou encore l’hérédité. Cependant, une grande partie des AVC repose sur des facteurs liés au mode de vie, et donc modifiables. C’est donc sur ces facteurs qu’il faut agir, en réalisant par exemple de la prévention. C’est un axe prioritaire de la santé publique. Il faut réussir à faire de la prévention ciblée. Si certains facteurs de risques ne sont pas sous le contrôle du patient, tels que sa prédisposition génétique ou le développement de la pathologie sans causes identifiables, d’autres facteurs sont modifiables par l’amélioration de son rythme et de ses conditions de vie.
4. Prévention de l’AVC
Avec un AVC toutes les 4 minutes enregistré en France, la prévention est essentielle et constitue un enjeu de santé publique [7]. En effet, comme vu précédemment, une grande partie des AVC pourrait être évitée en mettant en place de la prévention adaptée.
Cette prévention est dite primaire, car le but est d’agir pour éviter la survenue d’un AVC. Il est possible d’agir sur les facteurs de risques modifiables, vus dans la partie précédente. Il faut changer les habitudes de vie des individus, mais également avoir un suivi médical régulier. Pour ce faire, la France a mis en place un plan d’actions national “Accidents Vasculaires Cérébraux 2010-2014” [18]. Ce plan a permis de structurer l’organisation nationale et régionale sur la prise en charge rapide des AVC. Une des actions du plan était justement d’inclure le développement de la prévention de l’AVC, d’informer la population sur l’AVC. Au-delà de ce plan d’actions, des habitudes de vie permettent de réduire le risque de survenue d’AVC :
- Une alimentation équilibrée (riche en fruits, légumes mais pauvre en sel, graisses saturées et en sucre raffiné) permet de diminuer les risques cardiovasculaires.
- Une activité physique régulière permet d’améliorer la tension artérielle, le poids mais aussi la glycémie. L’Organisation Mondiale de la Santé (OMS) recommande de réaliser 150 minutes d'activité physique par semaine pour les personnes âgées entre 18 et 64 ans. Cela correspond donc à 30 minutes d’activité physique par jour et cela doit être fait 5 fois par semaine [19].
- Une visite médicale régulière permet de réduire les risques d’AVC. En effet, en allant régulièrement chez le médecin, il est possible d’avoir un suivi et donc de dépister une maladie chronique comme l’hypertension ou encore le diabète. Un échange avec un professionnel de santé permet d'habituer nos modes de vie.
Pour finir, le 29 octobre correspond à la Journée Mondiale de l’AVC. Cette journée a pour but d’informer le plus grand nombre de personnes sur les risques de l’AVC et les signes pour le détecter. À l’occasion de cette date, beaucoup d’actions d’information et de prévention sont donc mises en place partout en France. L’association France AVC d’Île-de-France publie notamment des affiches à destination du grand public pour proposer des mesures préventives et diminuer le risque d’AVC.
5. Le diagnostic d’urgence de la pathologie
L’AVC est une urgence médicale dont le pronostic dépend d’une prise en charge rapide et coordonnée. Dès la suspicion, une hospitalisation immédiate en UNV s’impose. Le diagnostic repose sur deux piliers complémentaires : l’évaluation clinique des fonctions neurologiques et la confirmation par l’imagerie médicale.
5.1. Identification précoce des signes d’AVC
Avant même l’arrivée à l’hôpital, l’identification précoce des signes d’un AVC par l’entourage joue un rôle déterminant. Le test FAST (Face, Arm, Speech, Time) ou VITE en français (Visage paralysé, Impossible de bouger un membre, Trouble de la parole, Éviter le pire en composant le 15), constitue un outil simple et rapide pour repérer les symptômes caractéristiques [20] :
- Face (visage) : le visage paraît-il asymétrique ? Demander à la personne de sourire
- Arm (bras) : un bras reste-t-il pendant ? Demander à la personne de lever les deux bras en ayant les yeux fermés
- Speech (parole) : la parole est-elle confuse ou incohérente ? Lui faire répéter une phrase simple
- Time (temps) : si un de ces signes est présent, appeler immédiatement les secours
L’AVC se manifeste en effet par des symptômes brutaux et soudains, tels qu’une paralysie partielle, des troubles du langage ou une perte de vision. Il s’agit d’une urgence médicale absolue, pendant laquelle chaque minute compte : plus la prise en charge est tardive, plus les risques de séquelles irréversibles (paralysie, troubles cognitifs, aphasie) ou de décès augmentent. Une intervention rapide permet, au contraire, d’améliorer considérablement le pronostic fonctionnel du patient.
Un des éléments essentiels du diagnostic de l’AVC est la considération du genre du patient. En effet, les symptômes classiques de l’AVC évoqués précédemment (asymétrie du visage, bras pendant, etc.) sont particulièrement adaptés à l’homme, mais bien moins à la femme. Cela explique que la mortalité soit plus importante pour les femmes que pour les hommes. En effet, chez ces dernières, la fibrillation auriculaire multiplierait par 2 les risques d’AVC par rapport à l’homme. Les périodes de grossesse et de ménopause augmentent également le risque de survenue d’AVC, tout comme la prise de traitements hormonaux notamment à base d’oestrogènes [8]. De façon générale, il est à noter que les femmes ont des douleurs plus fréquentes que les hommes, notamment dues aux cycles menstruels. La conséquence est que lors des périodes pendant lesquelles des céphalées ou encore des maux de ventre sont ressentis, les nombreux signes de l’AVC sont alors “masqués”. L’INSERM souligne de ce fait que l’appel aux secours est plus long chez les femmes que chez les hommes, ce qui a des conséquences irréversibles dans le cas de l’AVC [21].
5.2. Diagnostic du type d’AVC et prise en charge
L’imagerie médicale occupe une place centrale dans la prise en charge de l’AVC. Dès la phase diagnostique, elle permet de confirmer la nature de l’accident, d’en distinguer le type, ischémique ou hémorragique, et d’orienter la stratégie thérapeutique. L’imagerie cérébrale et vasculaire constitue la première étape de la prise en charge. Elle doit être disponible en permanence, 24h/24 et 7j/7, afin de garantir une intervention rapide et efficace [22].
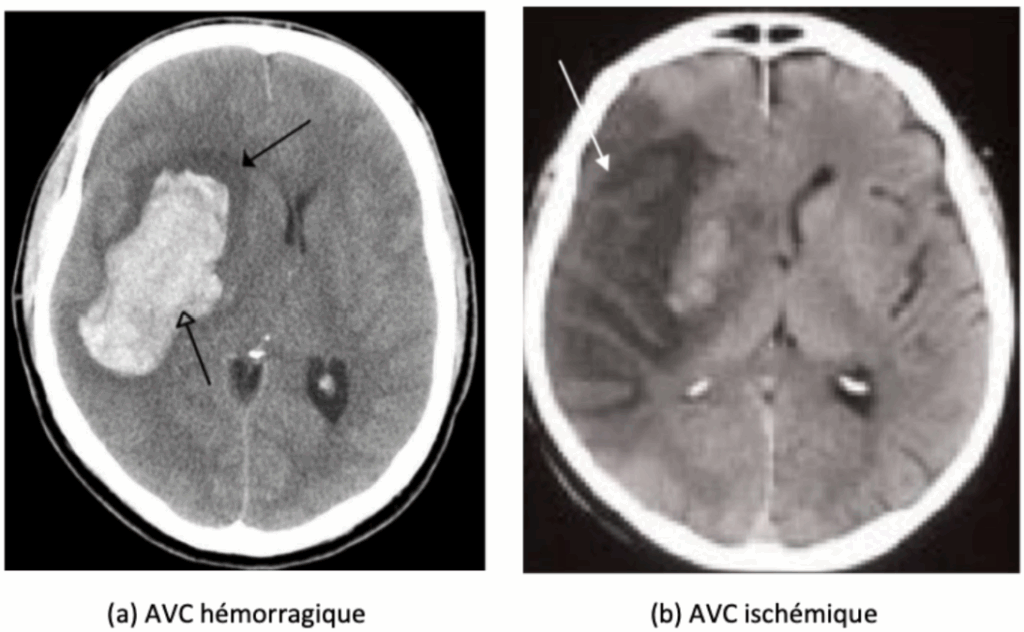
Lorsqu’un AVC est suspecté, le premier examen réalisé est généralement un scanner cérébral sans injection (tomodensitométrie - TDM) [23], lorsque l’Imagerie à Résonance Magnétique (IRM) n’est pas possible. Rapide et largement accessible, il permet avant tout de détecter une éventuelle hémorragie intracrânienne, qui apparaît sous forme d’une zone hyperdense (blanche) comme le montre la Figure 3.
Figure 3 : Aspect au scanner des AVC ischémique et hémorragique (Source : Léa PIETERS, Université de Lille 2, 2017) [24]
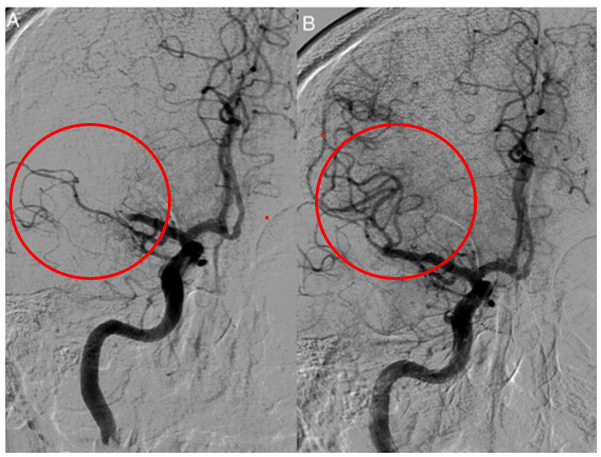
Si une hémorragie est mise en évidence, le diagnostic d’AVC hémorragique est posé et une prise en charge spécifique est initiée. Si aucun saignement n’est visible, l’hypothèse d’un AVC ischémique aigu est privilégiée. Dans ce cas, une angiographie par scanner (angio-TDM) peut être réalisée pour visualiser les artères cérébrales et repérer une occlusion d’un gros vaisseau (Figure 4).
Figure 4 : Angiographie carotidienne avant et après thrombectomie par cathéter dans un accident vasculaire cérébral aigu de la circulation antérieure.
(A) Occlusion thrombotique de l’artère cérébrale moyenne à l’admission.
(B) Artère cérébrale moyenne largement perméable (presque normale) après thrombectomie (Source : P. Widimsky et al.) [25]
L’injection d’un produit de contraste permet de dresser une cartographie précise du réseau vasculaire. L’imagerie vasculaire complète ce bilan en explorant les artères intracrâniennes et cervicales afin de localiser une sténose, une dissection ou une occlusion.
Bien que le scanner soit plus utilisé du fait de l’indisponibilité de l’IRM, cette dernière est considérée comme la technique de référence pour détecter les lésions ischémiques précoces et évaluer la perfusion cérébrale [22]. Les séquences de diffusion (diffusion-weighted imaging ou DWI) permettent de repérer très tôt les zones infarciées. Les séquences de perfusion distinguent le tissu nécrosé du tissu encore viable, orientant la décision de thrombolyse ou de thrombectomie mécanique.
Les séquences FLAIR (fluid-attenuated inversion recovery) et T2* apportent des informations complémentaires : datation des lésions, détection de micro-saignements ou de thrombus artériels [23, 26].
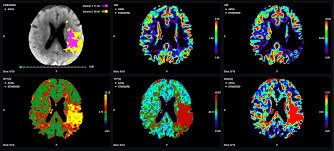
L’analyse de la perfusion cérébrale, réalisée par scanner ou IRM, est enrichie par des logiciels spécialisés (comme OLEA Sphere) qui génèrent des cartes colorées représentant :
- Le débit sanguin cérébral, ou Cerebral Blood Flow (CBF), qui correspond à la quantité de sang circulant dans une région donnée.
- Le volume sanguin cérébral, ou Cerebral Blood Volume (CBV), qui indique la quantité totale de sang présente dans le tissu.
- Le temps de transit moyen et le Tmax qui mesurent le temps nécessaire au sang pour traverser la zone étudiée.
Ces cartes (Figure 5) permettent de différencier le noyau infarci irréversiblement détruit de la pénombre ischémique encore récupérable. Cette approche a fait évoluer la notion de « fenêtre temporelle » vers celle d’horloge tissulaire : ce n’est plus le temps écoulé depuis les symptômes qui guide la décision thérapeutique, mais l’état du tissu cérébral lui-même [27].
Figure 5 : Cartes de perfusion issues d’un scanner de perfusion ou angioscanner (Source : olea medical, 2023) [28]
6. Traitements et parcours de soins actuels de l’AVC
Au-delà de son rôle diagnostique, l’imagerie est aujourd’hui pleinement intégrée dans la stratégie thérapeutique de l’AVC. Les techniques de neuroradiologie interventionnelle, encadrées depuis 2022 par un cadre réglementaire spécifique, permettent la réalisation de gestes endovasculaires tels que la thrombolyse ou la thrombectomie mécanique, sous contrôle radiologique. Ces interventions nécessitent une collaboration étroite au sein de centres spécialisés entre neurologues, radiologues, neuroradiologues et réanimateurs. La télémédecine et la téléradiologie renforcent ce dispositif en offrant un accès à l’expertise neurovasculaire même dans les établissements dépourvus d’unités spécialisées [22].
C’est dans ce contexte que s’inscrivent les traitements actuels de l’AVC, organisés autour de deux grandes phases : la phase aiguë, qui vise à traiter l’urgence et limiter les lésions cérébrales, et la prévention secondaire, destinée à réduire le risque de récidive et les complications à long terme.
6.1. Traitement de la phase aiguë : agir dans l’urgence
La phase aiguë constitue une course contre la montre : chaque minute de retard entraîne la destruction de millions de neurones. Dans le cas d’un AVC ischémique, qui est le plus fréquent, l’objectif est de restaurer la circulation sanguine le plus rapidement possible dans la zone cérébrale privée d’oxygène. Plusieurs options thérapeutiques sont disponibles :
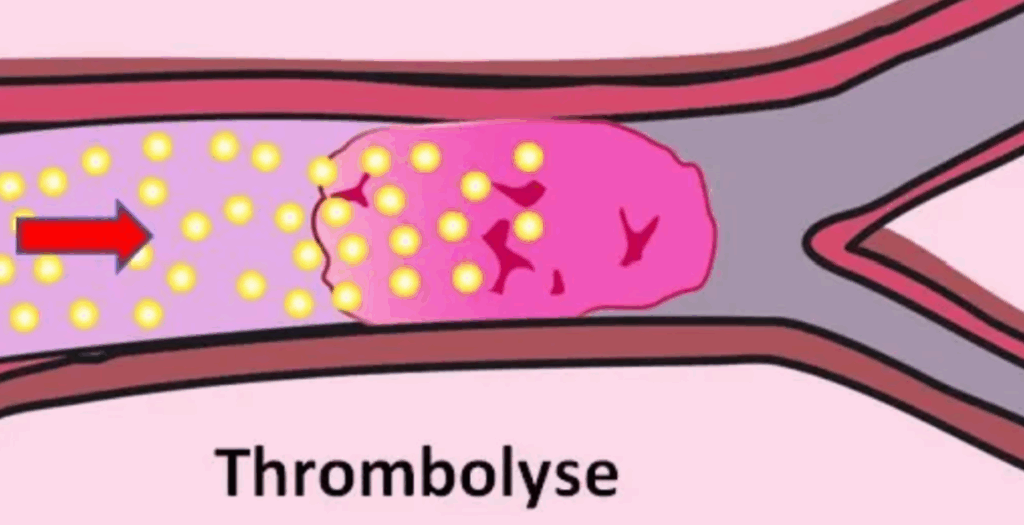
- La thrombolyse intraveineuse (IV) : administration par perfusion d’un médicament thrombolytique (tel que l’altéplase) permettant de dissoudre le caillot sanguin responsable de l’occlusion comme le montre la Figure 6. Ce traitement doit impérativement être réalisé dans un délai court, idéalement dans les 4h30 suivant l’apparition des symptômes [29]. Les nombreuses contre-indications limitent l’administration de ce traitement.
Figure 6 : Illustration d’une thrombolyse (Source : A. Aouadi, 2024) [30]
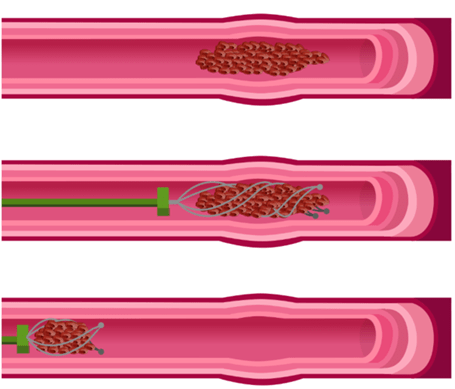
- La thrombectomie mécanique : intervention endovasculaire consistant à introduire sous contrôle radioscopique un cathéter (plusieurs voies possibles) et à le remonter jusqu’à l’artère cérébrale obstruée afin de retirer mécaniquement le caillot. Cette procédure, schématisée dans la Figure 7 et pratiquée dans des centres spécialisés, est particulièrement efficace lorsqu’elle est réalisée dans les 6 heures après le début des signes [29].
Figure 7 : Illustration de la procédure de thrombectomie mécanique (Source : Wikipedia, 2026) [31]
En revanche, pour un AVC hémorragique, la stratégie thérapeutique est différente : il s’agit de contrôler l’hémorragie et de réduire la pression intracrânienne. Le traitement peut inclure une intervention chirurgicale visant à réparer le vaisseau rompu, évacuer l’hématome ou drainer le sang accumulé (pose d’un drain ventriculaire externe). Le maintien des fonctions vitales et la stabilisation de la pression artérielle constituent alors les priorités absolues.
6.2. Limiter les risques de récidive et maximiser la récupération du patient après un AVC
Une fois la phase aiguë maîtrisée, l’objectif devient la prévention des récidives. En effet, le risque de récidive des patients ayant réalisé un AVC ou un AIT est estimé entre 30 et 43% à cinq ans [3]. La prévention pour éviter un nouvel AVC est appelée la prévention secondaire. Il faut donc pouvoir fournir une prise en charge et un suivi médical régulier aux patients à risque de récidive. Différents leviers sont mis en place selon le type d’AVC [32] :
- Pour l’AVC ischémique, il faut éviter qu’un vaisseau sanguin ne se bouche à nouveau. Pour ce faire, un traitement médicamenteux est administré au patient à base d’anticoagulants ou antiagrégants plaquettaire selon la cause initiale de thrombose.
- Pour l’AVC hémorragique, l’idée est d’éviter une nouvelle rupture de la paroi d’un vaisseau sanguin. Pour cela, un traitement médicamenteux est administré au patient à base d’antihypertenseurs. La prise d’anticoagulants est contre-indiquée pour ne pas favoriser le risque d'épanchement cérébral du sang.
Dans les deux types d’AVC, une attention particulière est accordée au contrôle et au suivi de la tension, du diabète, du cholestérol et du poids du patient. Le mode de vie du patient est bien entendu également contrôlé, avec une alimentation équilibrée, une gestion du stress optimisée et la pratique d’une activité physique. Ces éléments qui étaient précédemment considérés comme de la prévention primaire, sont appliqués avec rigueur après la survenue d’un AVC ou d’un AIT.
La seconde partie très importante de la prévention secondaire est la récupération du patient. C’est également un objectif de la prise en charge de l’AVC. En effet, même une fois le traitement mis en place et le patient stabilisé, ce dernier continue son parcours patient.
Ce parcours se poursuit notamment par de la rééducation. Elle vise à favoriser la récupération fonctionnelle et à réapprendre les gestes de la vie quotidienne. Selon les séquelles observées, différents professionnels interviennent comme le kinésithérapeute pour la motricité et la coordination, l’ergothérapeute pour la réadaptation aux activités quotidiennes ou encore l’orthophoniste pour la récupération du langage et de la déglutition. Cette rééducation débute dès les premières heures d’hospitalisation, se poursuit en centre spécialisé, puis à domicile. Elle améliore non seulement les capacités physiques, mais aussi la confiance et la qualité de vie du patient [33].
De plus, l’activité physique adaptée (APA) est souvent mise en place. Elle favorise le contrôle de la pression artérielle, stimule la plasticité cérébrale et contribue à réduire les séquelles motrices. Les activités proposées, comme la marche, le tennis de table, le karaté ou l’athlétisme, sont encadrées par des éducateurs spécialisés formés au sport-santé. Le médecin traitant peut prescrire ces activités en précisant les objectifs (récupération motrice, autonomie, contrôle du poids, bien-être psychologique) et les contre-indications éventuelles. De plus, certaines mutuelles, mairies ou départements peuvent participer financièrement aux frais liés à ces programmes. Les patients rapportent souvent des bénéfices physiques (meilleure endurance, motricité, équilibre) mais aussi psychosociaux, tels qu’une diminution de l’isolement, une meilleure estime de soi et un retour plus rapide à une vie active [33].
Ce premier chapitre permet de mettre en évidence les enjeux actuels de la prise en charge de l’AVC, en soulignant le besoin de rapidité ainsi que l’importance d’une organisation coordonnée entre les différents professionnels de santé. Il démontre les modalités de la prise en charge de l’AVC au sens large, allant des stratégies de prévention jusqu’au diagnostic et au traitement de ce dernier. Cette analyse du parcours patient actuel est importante pour comprendre l’intérêt des innovations biomédicales et organisationnelles, qui font l'objet du chapitre suivant.
II. Les perspectives d’améliorations de la prise en charge de l’AVC grâce aux innovations biomédicales
Plusieurs études cliniques ont démontré que le délai de revascularisation constitue l’un des principaux déterminants pronostiques lors d’un accident vasculaire cérébral ischémique aigü. La Figure 8 permet de mettre en avant l’efficacité relative d’un traitement en fonction du temps écoulé avant la revascularisation. On utilise pour cela “l’odds ratio” qui correspond au rapport entre la probabilité d’obtenir une issue favorable (absence ou réduction des séquelles) chez les patients traités et celle observée chez les non-traités.
Figure 8 : Efficacité des procédures de revascularisation en fonction du temps en cas d'accident vasculaire cérébral ischémique aigu (Source : Centre Hospitalier Universitaire Vaudois - Lausanne et Centre de rééducation et universitaire de Zurich, 2020) [34].
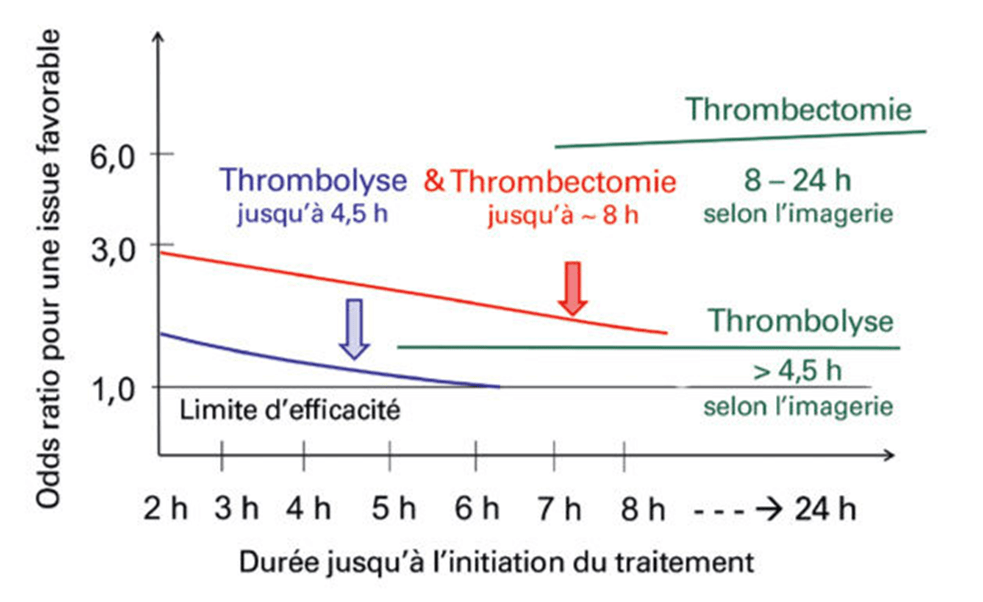
Ainsi, un odds ratio supérieur à 1 indique que le traitement permet d’éviter ou de réduire significativement les séquelles neurologiques post-AVC. La première heure suivant l’apparition des symptômes, ou “golden hour”, se caractérise par un odds ratio maximal pour l’ensemble des solutions thérapeutiques. C’est le cas de la thrombolyse dont la fenêtre thérapeutique optimale s’étend jusqu’à 4,5h. De même, la thrombectomie est particulièrement efficace dans un délai de 8h après l’AVC. On note qu’au sein même de ces fenêtres, l’efficacité thérapeutique décroit très rapidement.
Bien que basés sur plusieurs études, ces délais peuvent varier en fonction des cas. Ainsi, tous les patients ayant subi un AVC ischémique aigu invalidant dont les symptômes sont apparus il y a plus de 6 heures, mais moins de 24 heures au moment de la prise en charge, doivent être examinés rapidement pour évaluer leur admissibilité à une imagerie neurovasculaire. En fonction de l’atteinte tissulaire, l’intérêt d’une thrombolyse et/ou d’une thrombectomie tardive est évalué. Cependant, ces procédures personnalisées qui sont réalisées pour un odds ratio inférieur ou égal à 1 sont souvent associées à une probabilité d’atteinte fonctionnelle post-AVC élevée.
Afin d’assurer une prise en charge en urgence, une nouvelle organisation pilotée par les Autorités de Santé a ainsi été établie et mise en œuvre. La constitution de filières AVC régionales a été concomitante à celle des UNV qui jouent un rôle de référence pour les établissements de santé de proximité en intégrant :
- des lits en Unité de Soins Intensifs NeuroVasculaires (USINV),
- des lits d’hospitalisation classiques dédiés,
- une organisation permettant d'apporter une télé-expertise auprès des structures d’urgence de proximité
Le maillage territorial organisé en étoile autour des UNV reconnues par l’ARS (Mothership) intègre ainsi les établissements de santé selon un modèle de “drip” : diagnostic et thrombolyse intraveineuse dans un centre de proximité, and “ship” : transfert vers un centre expert pour une neurochirurgie. Ces circuits de prise en charge sont limités par des difficultés liées à la coordination des professionnels de santé entre les différentes étapes. De même, l’accès à une imagerie diagnostique, à une expertise neurovasculaire ou plus largement à des moyens thérapeutiques adaptés est problématique. Ainsi, en dépit de l’efficacité des procédures thérapeutiques actuelles, c’est l’accès aux soins qui est entravé pour une grande majorité des patients victimes d’AVC.
Dans ce contexte, des innovations biomédicales matérielles et organisationnelles sont en cours de développement et susceptibles de pallier ces limites.
1. Amener l'hôpital au patient grâce au projet ASPHALT
L’une des innovations les plus prometteuses consiste à amener les outils diagnostic et thérapeutiques au plus près des patients dans des Mobile Stroke Units (MSU) ou Unité Neurovasculaire Mobile (UNVM). Ce sont des ambulances avec une équipe spécialement formée à bord pour l’utilisation d’un scanner cérébral, d’un laboratoire biologique d’appoint et d’une solution de télémédecine reliée aux centres experts AVC. L’utilisation d’UNVM à Berlin et aux Etats-Unis a permis une réduction des délais de prise en charge des patients et une réduction du handicap par rapport aux parcours habituels. Les études ont notamment démontré une augmentation de 22% de l’accès à la thrombolyse passant de 79,5 % des patients éligibles à 97,1 %. Le temps médian pour l'initiation de la thrombolyse a également pu être raccourci en passant de 108 à 72 minutes.
Quant au critère principal, le pourcentage de patients retrouvant une vie normale trois mois après l'AVC, il a été augmenté de 24 % [35, 36].
Ces résultats ont conduit l’European Stroke Organisation (ESO) à suggérer de recourir à ce dispositif dont la rapidité de l’évaluation et du traitement préhospitalier permet une réduction significative des séquelles post-AVC. C’est dans cette dynamique que le Groupe Hospitalo-Universitaires (GHU) de Paris s’est doté d’une UNVM mutualisée avec le SAMU 75 et 9 autres hôpitaux parisiens participant. Cet investissement s’accompagne de la mise en place d’une étude visant à démontrer qu'une telle innovation permet d’améliorer la qualité de vie des patients pris en charge dans une zone géographique incluant de nombreux centres de TM (Paris intra-muros et petite couronne). Il s’agit du projet ASPHALT (Acute Stroke : prehospital versus in-hospitAL initiation of recanalization Therapy) qui est financé dans le cadre d’un programme de recherche médico-économique (PRME) de la DGOS à hauteur de 2,6 millions d'euros incluant le coût de l'UNV mobile d'environ 900 000 €. Cette dernière a été conçue sur mesure avec le concours d’équipementiers et d’entreprises de la Santé en intégrant les spécificités des routes et hôpitaux parisiens et les contraintes liées à la radioprotection.
L'objectif est de recruter 450 patients souffrant d’un AVC ischémique aigu sur trois ans pour juger du ratio coût-utilité à l’horizon vie entière en s’appuyant sur le critère clinique de handicap à 3 mois. L’étude est randomisée selon 2 bras de prise en charge : cheminement vers l'hôpital dans l'UNVM ou transport par véhicule de premier secours classique. Cette méthode doit permettre d’assurer un niveau de preuve scientifique suffisant pour comparer ces 2 parcours et conclure d’un avantage de l’UVNM pour la réduction des séquelles [37].
Le dispositif intègre un scanner 8 barrettes compact dédié à l’étude de l’encéphale, il est relié à un injecteur pour l’angiographie et alimenté par le moteur en intervention. Les médicaments, les pousses seringues électriques, le corpuls (défibrillateur/moniteur), la réserve de consommables pour la perfusion et le laboratoire biologique de première nécessité assurent une prise en charge adaptée, l’analyse sanguine délocalisée et la préparation de solutions thrombolytiques. En cabine, l’UNVM se distingue par la présence des retours corpuls et de l’injecteur (scanner), d’une caméra de surveillance patient et d’une console déportée pour les acquisitions. Un interphone permet également la communication avec le compartiment sanitaire qui inclut des sièges pour les 3 membres de l’équipe : l’ambulancier, le Manipulateur en Électroradiologie Médicale (MERM) et le médecin urgentiste ou neurologue.
Dès l’arrivée de l’UNVM sur site et la confirmation des symptômes cliniques, l’identité du patient est enregistrée et le protocole d’imagerie peut débuter. Il inclut un scout view pour le repérage et le placement des coupes, une acquisition sans produit de contraste pour éliminer la suspicion d’hématome et l'angioscanner pour le diagnostic de l’AVC. Ces acquisitions sont réalisées depuis la cabine blindée (3mm de Plomb) par le médecin et le manipulateur via la console déportée (ordinateur portable). Les images sont ensuite transmises sur un serveur PACS (Picture Archiving and Communication System) dédié pour la télé-interprétation. La surveillance du patient par le manipulateur et l’identification par le médecin d’un centre adapté pour la suite des soins sont réalisés en parallèle. Dans le cas d’un AVC ischémique sans contre-indication, la préparation et l’injection de l’Actilyse (thrombolyse) est réalisée par le médecin en amont du transfert. Les informations nécessaires à l’étude, telles que les données patients et le timing d’intervention, sont consignées sur la feuille eCRF (electronic Case Report Form).
La Figure 9 résume les différentes étapes de ce nouveau circuit de prise en charge :
Figure 9 : Logigramme du parcours patient avec l’UNVM pour la prise en charge de l’AVCi (ischémique) et AVCh (hémorragique) (Source : Auteur.e.s d’après l’APHP, 2023) [36]

Malgré le respect des procédures réglementaires de radioprotection (port des équipements de protection individuelle, dosimètre) et la réalisation des contrôles qualité, l’usage d’un scanner nécessite plusieurs autres dispositions. Le tableau (Figure 10) ci-dessous résume les principales contraintes et limites de ce dispositif.
Figure 10 : Tableau récapitulatif des contraintes et limites d’utilisation du projet ASPHALT (Source : Auteur.e.s)
| Contraintes | Limites |
| Des prises Maréchal sont nécessaires pour recharger les batteries hors intervention | Le scanner cérébral n’est pas prévu pour un usage sur véhicule roulant (vibrations, secousses, variations de température) |
| Les images envoyées sur le PACS pour télé-interprétation doivent être retransmises à l’UNV de transfert | La couverture réseau doit être compatible avec le transfert des acquisitions pour la télé interprétation et les échanges à distance |
| Une zone surveillée de 2m autour de la cabine sanitaire doit être établie (rubalise) lors des acquisitions pour assurer la radioprotection | En dépit d’un coût initial élevé, l’UNVM n’est pas mobilisable lorsque le patient se rend directement sur un site hospitalier |
| La zone de stationnement doit permettre au système de vérins hydrauliques couplés à un niveau électrique d’assurer l’horizontalité du dispositif pour réaliser les acquisitions | Le dispositif nécessite un réseau existant de centres experts pour la réalisation des actes techniques (neuroradiologie interventionnelle ou neurochirurgie) |
En optimisant le triage pré-hospitalier, en améliorant la coordination des soins et en réduisant les délais médians entre la survenue des symptômes et la thrombolyse, la thrombectomie mécanique ou la neurochirurgie grâce à une opération dès l’arrivée au centre, ce dispositif pourrait faire gagner jusqu'à une heure sur les circuits actuels de prise en charge. Cependant, sa mise en place nécessite un investissement élevé et des infrastructures modernes : couverture réseaux, centres experts, prises adaptées. Étant exclusivement réservé à la prise en charge de l’AVC, son déploiement doit également être justifié par un nombre d'actes suffisant. Suite à un lancement au cours de l’année 2024 et sans analyse intermédiaire planifiée, les premiers résultats de l'étude sont attendus “début 2027" d’après les responsables [36].
2. Recherche d'un centre expert pour une prise en charge adaptée : Télé-AVC
En complément des UNVM comme celle du projet ASPHALT, la télémédecine se développe et est apparue comme une innovation structurelle majeure pour améliorer l’accès à l’expertise neurovasculaire. Face aux difficultés d’accès aux centres spécialisés déficitaires sur le territoire et dont la répartition souffre d’inégalités, l'usage de la télémédecine à travers le Télé-AVC s'avère particulièrement pertinent. S’inscrivant dans le cadre de la loi « Hôpital, patients, santé et territoires » du 21/07/2009 et définit par le décret du 19/10/2010, le champ de la télémédecine concernant les AVC, ou télé-AVC, fait aujourd’hui partie intégrante de l’organisation de la filière de prise en charge des AVC et implique l’utilisation d’outils numériques associés à des processus organisationnels. Le télé-AVC constitue une pratique particulièrement déployée à travers l’ensemble du territoire depuis la mise en place du Plan national « AVC 2010-2014 » et regroupe l’ensemble des moyens nécessaires au diagnostic clinique, à l’imagerie, aux décisions thérapeutiques, en urgence, lors du suivi des patients et dans le cadre de réunions de concertation pluridisciplinaire [38].
Le concept du télé-AVC repose ainsi sur la mise en relation entre le département des urgences de proximité où le patient est accueilli et l’UNV de référence du territoire. En proposant un accès équitable à l’expertise médicale neurologique à tous les patients, dans l’urgence ou dans le suivi, quel que soit le lieu de vie ou de prise en charge, le Télé-AVC est apparu comme une solution viable pour les hôpitaux périphériques et/ou sous dotés. Ce dispositif nécessite la mise en commun de toutes les compétences nécessaires dans le champ des pathologies neurovasculaires, notamment neurologiques et radiologiques et s’intègre généralement dans une organisation globale, notamment avec un réseau de télémédecine régional lorsque celui-ci existe. D’autres spécialités peuvent être nécessaires telles que la chirurgie vasculaire, la médecine physique et de réadaptation, et éventuellement la pédiatrie. À ce titre, le terme « télé-AVC » se retrouve tout au long de la prise en charge du patient, de la phase hyperaiguë à la réadaptation, au suivi, et à la prévention secondaire et tertiaire, et se réfère à différents actes de télémédecine. Dans le cas de la prise en charge en phase aiguë, le principe est le suivant :
- Le service des urgences de proximité reçoit un patient présentant les symptômes d’un AVC. Un prélèvement pour bilan sanguin est réalisé et son consentement pour la télé-AVC recueilli.
- Après un examen d’imagerie médicale, les acquisitions sont routées vers une plateforme dédiée et le médecin urgentiste peut solliciter l’avis d’un neurologue situé sur un site de recours à distance pour une télé-expertise.
- Le neurologue accède aux éléments partagés (images IRM/scanner, résultats de biologie) transmis par l’établissement demandeur (télé-radiologie) et échange en temps réel avec le patient et le médecin urgentiste afin de poser son diagnostic, c’est la phase de télé-consultation. Les outils de visioconférence (caméras mobiles) sont indispensables pour permettre l’échange avec le patient (anamnèse et examen clinique standardisé).
- La décision thérapeutique (thrombolyse, thrombectomie, neurochirurgie) ainsi que la procédure de prise en charge (transfert vers un centre spécialisé) sont établis conjointement entre le médecin urgentiste et le neurologue, on parle de télé-assistance donnant lieu à une télé-thrombolyse par exemple.
- À l’issue de l’intervention clinique, les paramètres permettant de contrôler l’état clinique du patient (pression artérielle, saturation en oxygène, température, bilan biologique, Électrocardiogramme …) sont enregistrés, c’est la télé-surveillance.
La Figure 11 permet de faire un récapitulatif du processus de télé-AVC.
Figure 11 : Schéma du principe de fonctionnement du processus télé-AVC (Source : Dr. BUTTAZ, groupe TéléAVC Artois Hainaut, 2009) [39]
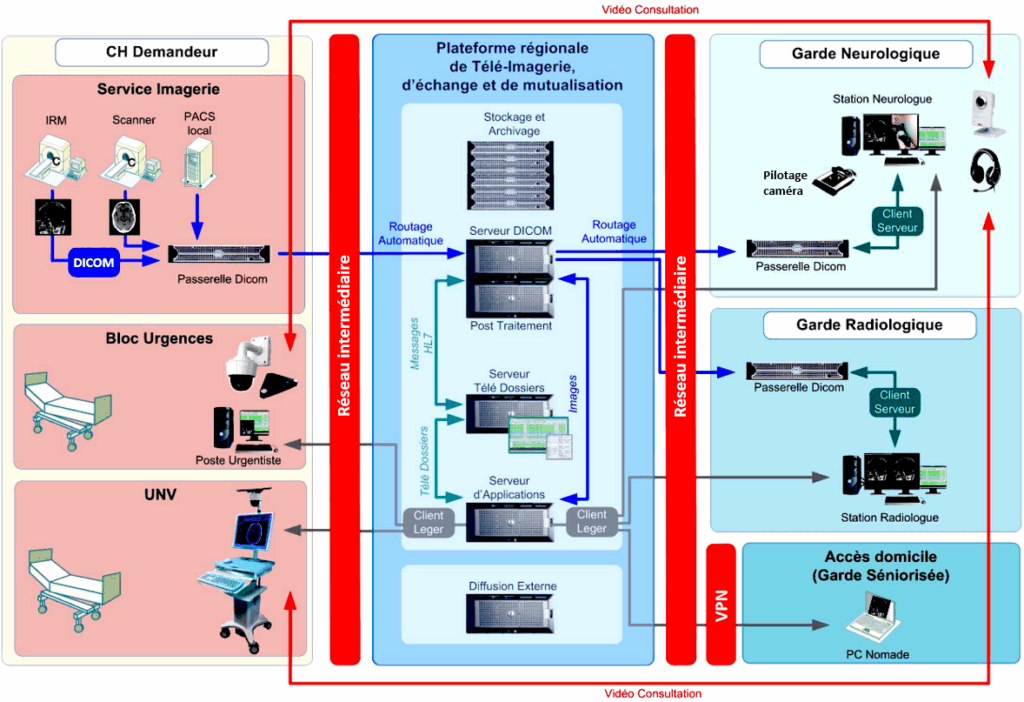
Lors de la phase hyperaiguë, la télé-AVC peut ainsi être mobilisé pour :
- L’évaluation par le médecin régulateur et/ou le médecin neurovasculaire directement dans l’ambulance pour aider au tri et à l’orientation préhospitalière des patients
- La prise en charge dans un établissement sans UNV
- La décision de transfert inter-établissement pour thrombectomie mécanique ou intervention neurochirurgicale dans le centre de recours, après analyse en urgence des données cliniques et radiologiques
Cependant, la mise en place d’une prise en charge à distance de l’AVC présente plusieurs contraintes techniques liées aux modalités d’échanges des données. Les flux vidéos nécessaires pour permettre le pilotage à distance par l’expert requièrent des débits de transmission élevés pouvant être complexes à gérer. Les échanges sonores doivent non seulement permettre une communication compréhensible pour le patient et les professionnels, mais aussi être enregistrés pour garantir la traçabilité et la qualité des décisions cliniques. S’agissant de données de grade médical, la question de la sécurité des communications, du stockage et de la gestion des accès est essentielle. De même, l’ergonomie et la rapidité des échanges doivent permettre un usage simple et à un accès à l’information en temps-réel. En outre, malgré le gain de chance pour le patient mis en évidence par plusieurs études, la télé-AVC en tant que service global n’est pas prise en charge par la Sécurité Sociale. En effet, seuls les actes individuels de télé-expertise et de télé-consultation le sont. De même, il n’existe actuellement aucun modèle général de financement des moyens indispensables à sa mise en œuvre opérationnelle : acquisition des stations de télémédecine, logiciels de visualisation des acquisitions, mise à disposition des ressources humaines (neurologues en astreinte, radiologues et personnel technique). Les structures existantes sont ainsi financées par l’ARS dans certains cas ou par l’établissement offrant le service ce qui constitue un frein majeur à la généralisation du dispositif. Enfin, son adoption peut aussi ajouter une contrainte sur les équipes soignantes en se cumulant à leurs activités quotidiennes.
Malgré les inégalités territoriales, les initiatives liées au télé-AVC s'intègrent progressivement à l’amélioration de la prise en charge des AVC. Sur les 60 réseaux déclarés par les ARS, on en recense actuellement 35 équipés et fonctionnels incluant 60 centres requis et 200 centres requérants. La dynamique positive de déploiement initiée par le plan AVC 2010-2014 fait aujourd’hui face à des problématiques structurelles et financières [40]. Une insertion systématique requiert une formation préalable des professionnels de santé aux pratiques de télémédecine. Plus globalement, leur sensibilisation aux nouveaux outils numériques, sur lesquels repose le télé-AVC ou le projet iAVC, devrait permettre de faciliter leur adoption.
3. Transfert interhospitalier du patient et géolocalisation médicale sécurisée : projet iAVC
Comme vu précédemment, le télé-AVC permet d’accélérer le diagnostic à distance. Cependant, il reste tout de même un problème dans le parcours patient : le transfert inter-hospitalier. En effet, une fois le patient orienté vers un centre expert pour une thrombectomie mécanique par exemple, les équipes soignantes receveuses ne connaissent pas précisément son horaire d'arrivée. Cela entraîne donc des pertes de temps critiques et complique l’organisation d’une prise en charge optimisée. C’est ainsi que le projet iAVC (Figure 12) est né, proposant une innovation technologique et organisationnelle basée sur la coordination en temps réel des différents acteurs impliqués dans la prise en charge de l’AVC.
Figure 12 : Logo de la startup iAVC (Source : iAVC)

Fondée en 2021 au sein de l’incubateur Eurasanté de Lille par Pierre-Olivier BUSSIÈRE et Adrien ROUSSEAUX, la startup iAVC est partie d’un constat simple : il est actuellement possible de suivre en temps réel la livraison d’un repas à domicile, mais il n’est pas possible de suivre la localisation d’un patient victime d’un AVC pendant son transfert hospitalier. Ainsi, il est fondamental de mettre en place une solution pour diminuer les pertes de temps et réduire les flous existant sur la chaîne de soin. Pour rappel, le cerveau perd environ 2 millions de neurones par minute en cas d’AVC [7]. De plus, la prise en charge implique une chaîne complexe d’acteurs (voir Figure 1). Ainsi, la coordination en temps réel est complexe entre les différents intervenants mais également pour gérer les ressources hospitalières comme le bloc opératoire ou l’IRM. Or, les équipes médicales ne peuvent connaître l’heure exacte d’arrivée du patient. Il y a donc une préparation trop tardive du personnel et du matériel, causant une perte de temps dans la prise en charge. Ou à l'inverse, une préparation trop rapide de tout le personnel et du matériel, entraînant une attente passive et inutile. C’est ainsi que la startup iAVC a développé une nouvelle application : ROMAIN.
ROMAIN est une solution mobile de géolocalisation en temps réel du patient pendant son transfert inter-hospitalier ou également en pré-hospitalier (en cours d’étude). Un bracelet connecté est mis en place au niveau de la cheville du patient. Via un système sécurisé tout au long de son transfert, il est possible d’avoir la géolocalisation du patient (que ce soit pour un transfert terrestre mais aussi héliporté). Cela permet donc aux équipes médicales de prévoir avec précision l’arrivée de ce dernier (Figure 13).
Figure 13 : Présentation du bracelet et de l’application ROMAIN (Source : iAVC)
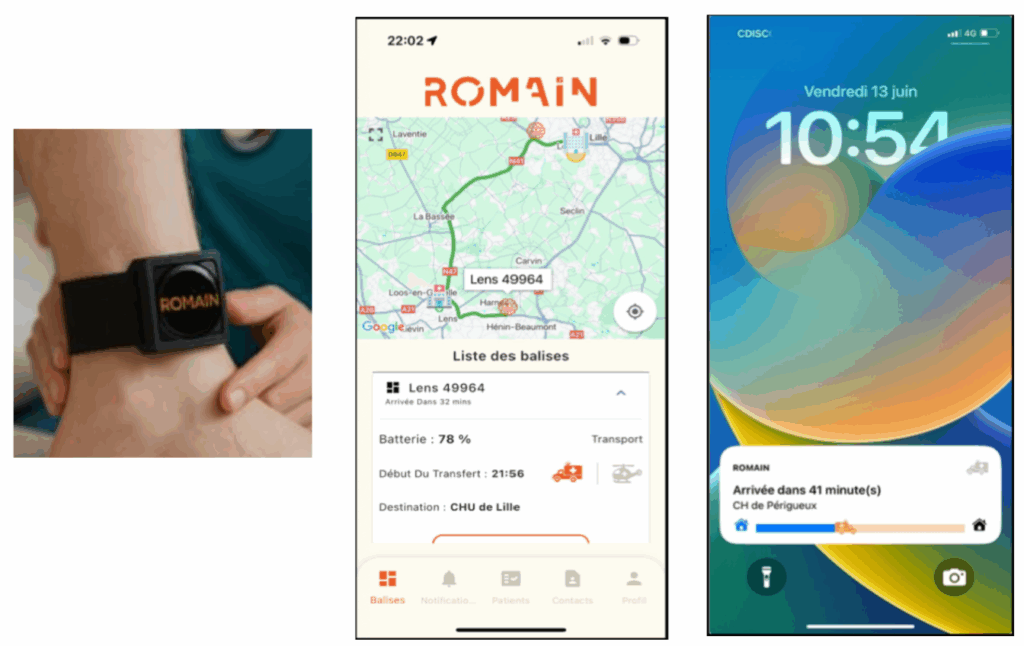
Plusieurs fonctionnalités sont actuellement disponibles ou en cours de développement :
- Notifier automatiquement les professionnels concernés via des alertes. Ces dernières sont transmises aux personnels en service et d’astreinte uniquement grâce à un calendrier personnalisé pour chaque intervenant.
- Partage sécurisé des données via un hébergement conforme aux normes de santé (Hébergeur de Données de Santé ou HDS, et Règlement Général sur la Protection des Données ou RGPD)
- Intégrer progressivement le dossier patient informatisé dans l’application pour avoir automatiquement l’horodatage de chaque étape de la prise en charge du patient : du départ du premier hôpital à l’arrivée dans le deuxième hôpital, en passant par les imageries et le bloc opératoire.
Ainsi, l’objectif principal de ROMAIN est bien d’optimiser la chaîne organisationnelle des professionnels de santé dans la prise en charge de l’AVC. Le but étant de réduire les délais d’intervention, notamment en intégrant la notion de “P to P”, c’est-à-dire “Picture to Puncture” (temps entre l’imagerie cérébrale confirmant l’AVC et la thrombectomie). Mais d’autres bénéfices sont attendus :
- Réduire le temps d’attente des équipes médicales et la durée de leur mobilisation
- Diminuer le nombre d'appels téléphoniques pouvant avoir lieu entre le SAMU et les établissements grâce à la visualisation en temps réel des informations sur l’application
- Optimiser le flux de patients et anticiper les besoins matériels
- Mieux évaluer les temps de prise en charge
Le projet iAVC a depuis 2024 été déployé en phase pilote au Centre Hospitalier Universitaire (CHU) de Lille, en partenariat avec le SAMU 59, sous la supervision d’un comité éthique et scientifique. Les premiers résultats portent essentiellement sur l’acceptabilité du dispositif : sur 125 patients transférés, environ 96% ont pu être équipés d’un bracelet connecté, ce qui montre que les équipes soignantes réussissent à intégrer le système dans leur pratique de prise en charge. Toutefois, à ce stade, ces chiffres ne renseignent pas sur l’impact réel de la solution ROMAIN sur les délais de prise en charge ou sur l’organisation des soins. Ils témoignent uniquement d’un bon taux d’utilisation. Depuis juillet 2025, le CHU de Bordeaux dispose également de la solution ROMAIN. Du reste, l’implantation du système à Nancy et à Reims est en cours d’exploration. Ce déploiement témoigne d’un intérêt croissant des hôpitaux à adopter ce dispositif dans leur pratique. Cependant, des données supplémentaires doivent parvenir pour évaluer le bénéfice pour le patient et pour l’amélioration de l’organisation de la prise en charge de l’AVC.
Au-delà des transferts inter-hospitaliers, iAVC a comme objectif d’élargir son champ d’application en incluant les transferts pré-hospitaliers. L’outil souhaite être intégré directement dans les services informatiques des hôpitaux pour avoir accès à une retransmission des données du bracelet directement dans le dossier patient pour avoir une traçabilité.
Le projet bénéficie actuellement du dispositif Article 51 de la sécurité sociale, permettant de promouvoir l’innovation en santé en fournissant un mode de financement inédit. Le projet doit donc démontrer une pertinence et un réel intérêt dans la prise en charge sanitaire. Une fois démontré, le projet doit aller s’inscrire dans le droit commun et pouvoir obtenir ainsi une convention avec l’Assurance Maladie pour obtenir le remboursement du produit [41]. Dans le cadre du projet iAVC, il s’agit de prouver que la solution permet d’améliorer la coordination des équipes et que cela réduit la mortalité et les séquelles pour les patients, mais également que les frais associés pour le système de santé sont soutenables.
Malgré son potentiel, la solution ROMAIN présente des limites, notamment quant à l'utilisation d’un bracelet géolocalisé. En effet, selon le type de transport ou l’environnement du patient, la couverture réseau pourrait réduire la fiabilité de la géolocalisation. De plus, il est nécessaire de faire accepter la solution par l’ensemble du personnel soignant, qui doit donc adapter ses pratiques de soins, modifier ses habitudes mais également suivre une formation. La startup a déjà évoqué l’implantation du système dans l’ensemble des ambulances. Pour le moment, cela n’est pas possible car il y a justement un refus de certaines personnes qui y voient ici un moyen de suivre tout le temps les ambulances, même quand ce n’est pas un patient faisant un AVC. Et cela pourrait poser un problème quand l’ambulance est par exemple en pause. iAVC s’est donc adapté en mettant le bracelet directement sur les patients, et non sur l’ambulance. Mais un travail d’acceptation reste tout de même à mettre en place. Par ailleurs, la question de la sécurité des données de santé reste à vérifier. Le système ROMAIN héberge les données conformément aux normes HDS et RGPD. Mais dans l’optique d’un développement de l’application, il faudra toujours conserver cette confidentialité notamment si les données sont envoyées vers le dossier patient de l’hôpital. Ainsi, le projet est novateur mais des éléments restent à vérifier avant un déploiement sur l’ensemble du territoire français.
Pour conclure, le projet iAVC représente une innovation biomédicale dans la prise en charge de l’AVC en proposant le bracelet et l’application ROMAIN permettant de géolocaliser les patients. Il intègre le numérique et la notion de géolocalisation médicale sécurisée pour permettre d’agir sur l’un des facteurs aggravant de l’AVC : le délai trop long de prise en charge du patient. Toutefois, son efficacité devra être confirmée au fur et à mesure de sa mise en place via des données cliniques.
4. Développement de la thrombectomie mécanique de proximité et impacts sur la prise en charge de l'AVC
L’organisation de la thrombectomie mécanique en France a connu une évolution majeure depuis 2015, sous l’impulsion de la SFNR et de la DGOS. Les publications de cinq grandes études internationales ont démontré l’efficacité de la thrombectomie dans le traitement de l’AVC ischémique aigu à occlusion de gros vaisseaux, entraînant une refonte du maillage territorial pour permettre l'égalité d'accès aux soins de la population.
Les décrets n° 2022-21 et n° 2022-22 de janvier 2022 [42], relatifs aux conditions techniques de fonctionnement de l'activité interventionnelle sous imagerie médicale en neuroradiologie, définissent précisément les obligations de moyens applicables aux établissements autorisés à pratiquer la thrombectomie mécanique et vient remplacer l’ancien arrêté du 15 mars 2010 relatif à la prise en charge des patients victimes d’un accident vasculaire cérébral. Le texte impose la présence sur site d’une unité de soins intensifs disposant d’une expertise neurovasculaire et d’une unité de réanimation, toutes deux accessibles 24h/24 et 7 j/7. L’établissement doit également garantir l’accès permanent à un scanner et une IRM, ainsi qu’à des examens de biologie médicale et aux produits sanguins nécessaires.
Sur le plan technique, le décret exige la mise à disposition d’une salle d’angiographie numérisée interventionnelle répondant aux normes d’anesthésie et d’asepsie d’un bloc opératoire et permettant la visualisation du parenchyme cérébral (anatomie et tissus). Les conditions d’autorisation incluent aussi un seuil minimal d’activité dans l’objectif d’avoir des équipes opérationnelles habituées au geste de thrombectomie mécanique.
Enfin, le personnel médical doit inclure des praticiens formés et expérimentés en neuroradiologie interventionnelle, en nombre suffisant pour assurer la permanence et la continuité des soins. Le texte n’impose toutefois pas de quota chiffré d’effectifs paramédicaux, laissant aux établissements la responsabilité d’adapter leurs ressources humaines aux exigences de sécurité et de disponibilité.
Initialement concentrée dans quelques grands centres universitaires, la pratique s’est progressivement étendue grâce à une politique d’ouverture de centres de thrombectomie de proximité, visant à réduire les délais d’accès à la reperfusion. Sous l’impulsion de la première génération de médecins radiologues interventionnels rigoureusement formés pendant 1 an, et en étroite collaboration avec les agences régionales de santé, de nouveaux sites ont ouvert dès 2017-2018, souvent dans un cadre dérogatoire. Ces sites sont par exemple situés dans les villes de : Pau, Bayonne, Annecy, Valence, Valenciennes, Boulogne, Mantes-la-Jolie, Aulnay, Meaux, Corbeil-Essonnes, etc. Ces structures présentaient déjà un plateau technique d’angiographie et une expérience en neuroradiologie interventionnelle, facilitant leur adaptation rapide au parcours de prise en charge de l’AVC.
Le succès de ces centres a permis l’extension du dispositif à l’échelle nationale, avec 52 centres actifs, garantissant désormais un délai d’accès inférieur à une heure pour la quasi-totalité du territoire. Les bénéfices de la thrombectomie de proximité sont multiples. Le principal est la réduction du délai de reperfusion, facteur déterminant du pronostic neurologique (« time is brain »). Cette proximité permet également une amélioration de la coordination interhospitalière, en rapprochant la neuroradiologie interventionnelle des services d’urgence et des UNV. En parallèle, la mutualisation des plateaux techniques, comme à Bastia, où la salle d’intervention est partagée avec la cardiologie, optimise les ressources matérielles et humaines tout en maintenant la réactivité pour les urgences vitales (AVC et infarctus du myocarde).
L’ouverture de nouveaux centres étant par le volume minimal d’activité, la pérennité du dispositif repose sur la consolidation des équipes existantes, l’évaluation des zones encore sous-dotées et l’amélioration du circuit préhospitalier et interhospitalier, souvent pénalisée par une expertise inégale en imagerie et un manque de priorisation des urgences neurologiques.
Le CHU de Bordeaux constitue un exemple abouti d’optimisation du parcours patient interhospitalier dans la prise en charge de l’AVC aigu. L’établissement a été le premier en France à installer une salle d’angiographie biplan directement intégrée au sein du bloc des urgences, à proximité immédiate du service d’imagerie d’urgence (Figure 14). Ce positionnement stratégique permet de supprimer les transferts inter-services entre les urgences, la radiologie et la neuroradiologie interventionnelle, réduisant ainsi de plusieurs dizaines de minutes le délai entre l’arrivée du patient et la réalisation d’une thrombectomie mécanique. Dans une pathologie où chaque minute représente des millions de neurones perdus, cette approche organisationnelle constitue un progrès majeur.
La salle a été conçue comme un plateau interventionnel partagé, pouvant accueillir l’ensemble des actes de radiologie vasculaire urgente (notamment les hémorragies et pathologies aortiques), mais son activité est dédiée à près de 90 % à la thrombectomie mécanique. Ce choix traduit une priorisation claire de la filière neurovasculaire et la volonté d’assurer une disponibilité quasi permanente pour l’AVC ischémique. L’intégration spatiale des urgences, de l’imagerie et de la salle interventionnelle crée une unité fonctionnelle complète autour du patient, depuis le diagnostic initial jusqu’à la revascularisation.
Figure 14 : Les docteurs Xavier Barreau et Eva Jambon au sein de la salle d’imagerie interventionnelle désormais intégrée aux urgences de l’hôpital Pellegrin : une première en France. Crédit photo : Thierry David/SO (Source : Sud ouest, 2025) [43]
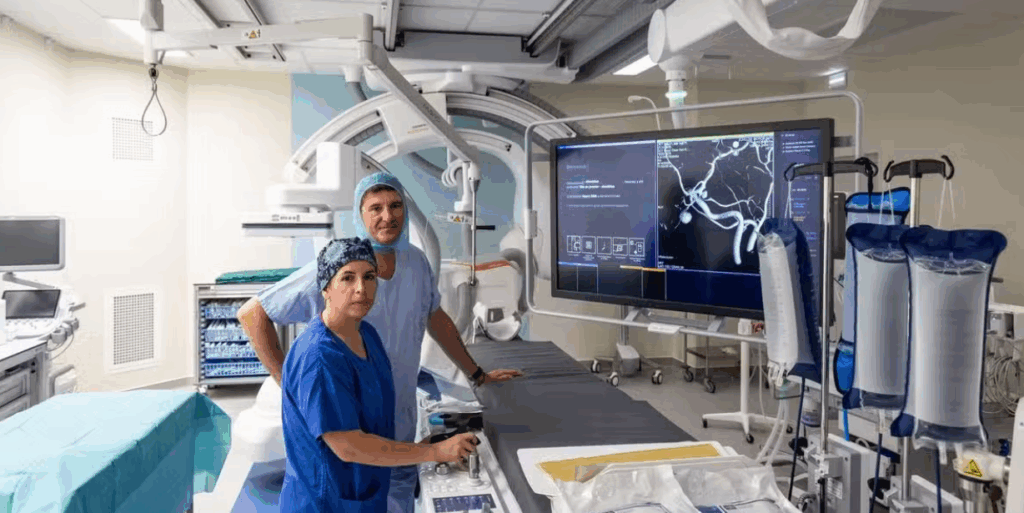
Cette organisation, unique en France au moment de sa mise en place, illustre la tendance actuelle vers des modèles d’intervention intégrés, où la logistique et l’architecture hospitalière deviennent des leviers déterminants d’efficacité clinique. Le projet bordelais démontre qu’une réorganisation physique du plateau technique peut être tout aussi décisive que l’innovation technologique pour améliorer les délais de reperfusion et, in fine, le pronostic fonctionnel des patients victimes d’un AVC.
Malgré les progrès significatifs de la thrombectomie de proximité en France depuis 2015, plusieurs limites persistent et méritent un regard critique. La formation et les ressources humaines restent des obstacles majeurs . Le recrutement et la formation des neuroradiologues interventionnels, avec un cursus strict d’un an et un volume minimal de 60 thrombectomies par centre, limitent l’ouverture de nouveaux sites et peuvent générer une saturation dans les centres existants. Les effectifs paramédicaux ne sont pas réglementés, entraînant une variabilité de la qualité et de la continuité des soins selon les établissements.
Des inégalités territoriales subsistent également. Certaines zones rurales ou périphériques restent moins bien desservies malgré l’expansion à 52 centres. Le circuit préhospitalier n’est pas uniformisé et la priorisation des AVC dans les urgences polyvalentes reste imparfaite ralentissant parfois la prise en charge. La complexité organisationnelle constitue un autre défi : la coordination entre urgences, imagerie et salle d’angiographie exige une fluidité maximale difficile à maintenir en cas de saturation ou d’indisponibilité du personnel et du matériel. Le partage des salles avec d’autres interventions urgentes, bien que nécessaire, peut générer des conflits de priorité et limiter l’accessibilité immédiate lorsque l’activité dédiée à la thrombectomie approche 90 %. Enfin, la pérennité et le suivi du dispositif dépendent de la consolidation des équipes, de la formation continue et de l’évaluation régulière des zones sous-dotées.
5. Robeauté : un micro-robot qui pourrait révolutionner la neurochirurgie
À plus long terme, certaines innovations pourraient transformer la prise en charge neurologique. En effet, dans le cadre du traitement de l’AVC, le dispositif en cours d’étude par Robeauté ouvre des perspectives inédites (Figure 15).
Figure 15 : Représentation de différentes configurations du microrobot Robeauté en fonction de l’objectif clinique : dépôt d’électrode (Micro-sensor), visualisation des structures (Micro-camera), administration de traitements (Drug Delivery) (Source : Sorbonne Université, 2022) [44]

La start-up française est actuellement en train de développer un micro-robot neurochirurgical de la taille d’un grain de riz en phase d’essai pré-clinique. Il est conçu pour naviguer au sein des tissus cérébraux via des orifices minimes afin de délivrer des traitements, implanter des électrodes ou réaliser des biopsies avec une précision optimale [45]. Grâce à un système de propulsion miniaturisé, un guidage 3D à distance par IRM cérébral et un tracking en temps réel par ultrasons, ce microrobot peut emprunter des trajectoires non linéaires, ce qui lui permet d’atteindre des zones profondes ou complexes que la chirurgie traditionnelle ne peut approcher sans risque élevé [44]. Outre les tumeurs, Robeauté envisage d’étendre l’application de cette technologie aux pathologies neurologiques comme les maladies neurodégénératives ou les séquelles d’AVC, en explorant la possibilité d’une délivrance ultra-ciblée de traitements directement dans le tissu cérébral lésé. Moins invasif que les solutions actuelles et avec des 1er essais cliniques sur des patients prévus fin 2026, ce dispositif pourrait notamment intervenir pour traiter les tissus atteints en évitant d’endommager les tissus sains.
Cependant, cette innovation peut soulever plusieurs défis majeurs. La navigation d’un dispositif robotique au sein du tissu cérébral exige une grande précision, car la moindre déviation pourrait endommager des zones fonctionnelles essentielles. De plus, le passage de prototypes précliniques à une utilisation humaine impose de garantir la biocompatibilité, la sécurité du dispositif, son devenir après intervention, ainsi que la fiabilité de la délivrance du traitement.
Plus globalement, le développement de nouvelles technologies miniaturisées pourrait permettre d’intervenir sur l’ensemble des étapes de la prise en charge de l’AVC. En effet, d’autres projets s'intéressent notamment à l’administration d’agents thrombolytiques au plus proche de la zone obstruée à l’aide de micro robots capables de se déplacer au sein même des vaisseaux sanguins. En plus de la veille technologique, l’étude des méthodes et structurations internationales est également primordiale.
6. Comparaison internationale de la structuration du parcours AVC
À l’échelle internationale, les modèles d’organisation de la thrombectomie mécanique diffèrent sensiblement selon les systèmes de santé et la densité territoriale. Aux États-Unis, la prise en charge repose sur un réseau hiérarchisé de Compréhensive Stroke Centers (CSC) et de Primary Stroke Centers (PSC), coordonnés par des protocoles standardisés (drip and ship ou mothership). La rapidité d’accès est favorisée par un recours massif à la téléexpertise neurologique et à des systèmes de tri préhospitalier algorithmiques utilisant des échelles de gravité. Toutefois, la taille du territoire américain impose souvent des transferts longs, compensés par la généralisation des ambulances mobiles de type Mobile Stroke Unit (MSU), dotées de scanners embarqués et d’équipes formées à la thrombolyse préhospitalière. Ces unités permettent d’administrer la thrombolyse en moyenne 30 à 40 minutes plus tôt, réduisant la mortalité et améliorant le pronostic fonctionnel, bien que leur coût limite leur diffusion en dehors des grandes métropoles.
En Allemagne, le modèle est particulièrement innovant grâce à une intégration poussée de la télémédecine et à un réseau dense d’unités neurovasculaire. Le programme Telemedical Project for Integrative Stroke Care (TEMPiS) relie plus de 20 hôpitaux communautaires à des centres experts par télé-imagerie et téléconsultation 24h/24, permettant une thrombolyse sécurisée dans des établissements non spécialisés et un tri plus rapide pour les thrombectomies [46]. L’Allemagne a aussi été pionnière dans le déploiement des Mobile Stroke Unit (MSU), démontrant leur faisabilité et leur impact clinique dès 2012 à Berlin.
Le modèle français, en comparaison, s’est développé plus tardivement mais avec une forte structuration réglementaire et un objectif clair d’équité territoriale. Les centres de thrombectomie de proximité offrent une alternative réaliste aux MSU, mieux adaptée à la géographie française, en garantissant un accès à moins d’une heure sans nécessiter d’infrastructure mobile coûteuse. Ce modèle repose sur la mutualisation des plateaux techniques, la formation homogène des équipes et le développement de la téléthrombolyse, permettant aux hôpitaux non experts d’être intégrés au parcours de soins.
Enfin, certains pays nordiques, notamment la Finlande et le Danemark, se distinguent par une logistique d’urgence centralisée : un seul centre de thrombectomie par région, mais des hélicoptères médicalisés dédiés aux AVC, assurant un transfert direct depuis le site d’appels. Ces stratégies, bien que coûteuses, atteignent des délais de reperfusion comparables aux meilleurs centres américains.
Ce dernier chapitre démontre les perspectives d’évolution de la prise en charge de l’AVC, qu’il s’agisse d’innovations en cours d’intégration sur le terrain ou à venir. Toutefois, il est important de rappeler que leur mise en place reste inégale sur le territoire français, et très hétérogène à l’international. Les contraintes de déploiement sont plurifactorielles et naissent de difficultés structurelles, financières, technologiques ou encore liées au personnel soignant réticent à l’adoption de nouvelles méthodes par exemple. Le tableau récapitulatif de l’ensemble des solutions présentées est disponible Figure 16 :
Figure 16 : Tableau récapitulatif des innovations biomédicales pour la prise en charge de l’AVC (Source : Auteur.e.s)
| Innovation | État du déploiement en France | Champ d’action | Champ d'application |
| UNVM (ASPHALT) | 1 étude médico-économique en cours en île-de-France | Imagerie diagnostique sur site, Télé-interprétation, Télé-thrombolyse | Diagnostic, Thrombolyse, Transfert domicile-UNV |
| Télé-AVC | +250 établissements participants répartis sur l’ensemble du territoire | Télé-interprétation, Télé-consultation, Télé-thrombolyse | Diagnostic, Décision thérapeutique, Choix du centre de Transfert |
| iAVC | 2 CHU équipés, 2 CHU en cours d’étude | Géolocalisation du patient en temps-réel | Suivi du transfert inter-hospitalier |
| Centres de Thrombectomie | 52 centres actifs | Traitement en phase aiguë | Neuroradiologie interventionnelle |
| Robeauté | Phase pré-clinique | Traitement en phase subaiguë | Administration de médicaments, Dépôt d'électrodes |
De ce tableau récapitulatif des innovations, nous avons pu envisager un schéma global envisageable pour la prise en charge de l’AVC, présent dans la Figure 17.
Figure 17 : Schéma global de la prise en charge de l’AVC (Source : Auteur.e.s)

Conclusion
L’AVC est une pathologie qui voit aujourd’hui de nombreuses innovations biomédicales naître afin de réduire autant que possible les délais de prise en charge. Si certains patients sont admis directement dans un centre expert lors d’une suspicion d’AVC, la majorité des cas impliquent un à plusieurs transferts hospitaliers pour trouver une structure adaptée. Malgré les plans dédiés à l’AVC, les contraintes démographiques et économiques limitent l’accessibilité aux soins.
Ce projet a donc étudié des solutions compatibles avec l’urgence de la phase hyper aiguë, afin de réduire le taux de mortalité et les séquelles liées. En rapprochant l’imagerie au patient, l’UNVM permet un triage préhospitalier efficace et permet un transfert direct vers le centre adapté. Les résultats du projet ASPHALT suggèrent un intérêt particulier pour les zones sous-dotées (déserts médicaux) afin d’initier au plus tôt la thrombolyse et éviter de multiplier les transferts inutiles. Cependant, l’investissement initial exigé pourrait restreindre son usage aux grandes agglomérations disposant des moyens financiers suffisants. Enfin, les travaux sur l’IRM portable ultra-bas champ spécialisé pour l’imagerie du cerveau pourraient enlever les contraintes du scanner et améliorer le diagnostic. De plus, la télé-AVC, associant télé-expertise et téléconsultation, offre une expertise neurologique aux structures de proximité, tandis que des outils de géolocalisation (comme le bracelet ROMAIN de la Startup iAVC) permet d’améliorer la coordination des transferts inter-hospitaliers. Le déploiement de nouveaux centres experts de l’AVC et leur intégration au maillage régional doit pouvoir garantir une meilleure couverture territoriale pour réduire les délais de transport. Enfin, la mise en place d’une salle d’imagerie interventionnelle au sein même du service des urgences permet un gain de temps sur la dernière phase intra-hospitalière. Ces innovations s’intègrent directement aux circuits existants et offrent des gains de temps significatifs tout en maîtrisant les coûts.
L’articulation de ces différentes solutions pourrait répondre aux besoins des patients et ainsi réduire l’impact sanitaire et économique de l’AVC chiffré à 4,5 milliards d’euros pour l’année 2022 par la cour des comptes [47]. Pour finir, la réussite de ces innovations repose sur une coordination des équipes médico-techniques pluridisciplinaires pour voir émerger des solutions performantes et répondant au mieux aux exigences des praticiens. Les actions nationales de sensibilisation et de prévention sur les facteurs de risque de l’AVC, ses symptômes et la conduite à tenir en cas de leur survenue constituent également un axe important à développer. Bien menées, elles devraient notamment permettre de garantir la reconnaissance du besoin urgent de services médicaux sur des publics ciblés afin d’assurer la délivrance de soins adaptés dans les meilleurs délais.