IDS254 - Chirurgie 4.0 : Intégration des salles multimodalités et des robots chirurgicaux au bloc opératoire
Les projets ou stages publiés auxquels vous accédez sont des rapports d'étudiants et doivent être pris comme tels. Il peuvent donc comporter des imperfections ou des imprécisions que tout lecteur doit admettre et donc supporter. Il ont été réalisés pendant les périodes de formation et constituent avant-tout des travaux de compilation bibliographique, d'initiation et d'analyse sur des thématiques associées aux concepts, méthodes, outils et expériences sur les démarches qualité dans les organisations ou sur les technologies en santé.
Si, malgré nos précautions, vous avez des raisons de contester ce droit de diffusion libre, merci de nous en faire part (master@utc.fr), nous nous efforcerons d'y apporter une réponse rapide. L'objectif de la présentation des travaux sur le web est de permettre l'accès à l'information et d'augmenter ainsi la qualité des échanges professionnels.
Nous ne faisons aucun usage commercial des travaux de projet ou de stage publiés, par conséquent les citations des informations et l'emploi des outils mis à disposition sont totalement libres. Dans ce cas, nous vous demandons de respecter les règles d'éthique en citant explicitement et complètement vos sources bibliographiques.
Bonne lecture...
Auteurs





Contacts
- DELATTRE Eloïse : eloise.delattre59@gmail.com
- FRAYCHINAUD Etienne : etienne.fraychinaud@gmail.com
- NZIMI Fabiola : valnzims@gmail.com
- QURAISHI Aamir : quraishiaamir7@gmail.com
- ROSSETTI Alexandre : alex.ros2206@gmail.com
Citation
A rappeler pour tout usage : ROSSETTI Alexandre, FRAYCHINAUD Etienne, DELATTRE Eloïse, QURAISHI Aamir, NZIMI Fabiola « Chirurgie 4.0 : Intégration du numérique au bloc opératoire », Université de Technologie de Compiègne (France), Master Ingénierie de la Santé, Mémoire de Projet, https://travaux.master.utc.fr/, réf n° IDS254, janvier 2025, https://doi.org/10.34746/ids254, https://travaux.master.utc.fr/formations-master/ingenierie-de-la-sante/ids254/
Résumé
Le bloc opératoire évolue vers la chirurgie 4.0, une transformation inspirée par l’Industrie 4.0 et reposant sur des technologies telles que l’intelligence artificielle, l’Internet des objets médicaux (IoMT), les robots chirurgicaux, l’imagerie avancée et les jumeaux numériques. Ces outils modernisent le bloc opératoire, offrant des soins plus sûrs et plus efficaces tout en améliorant l'expérience des professionnels de santé.
Les salles multimodalité et les robots chirurgicaux révolutionnent la pratique en augmentant la précision des interventions, réduisant les complications post opératoires et optimisant la gestion des cas complexes. Toutefois, leur mise en œuvre présente des défis importants, notamment l’adaptation des infrastructures, la sécurisation des données médicales, l’intégration interopérable des dispositifs connectés et le respect de cadres réglementaires stricts..
Abstract
The Operating rooms are advancing toward Surgery 4.0, a transformation inspired by Industry 4.0 and driven by technologies such as Artificial Intelligence, the Internet of Medical Things (IoMT), surgical robots, advanced imaging, and digital twins. These innovations modernize operating rooms, delivering safer and more precise healthcare while enhancing the experience of healthcare professionals.
Multimodal rooms and surgical robots are revolutionizing surgical practice by increasing precision in interventions, reducing postoperative complications, and optimizing the management of complex cases. However, their implementation poses
challenges, including adapting infrastructures, securing medical data, ensuring interoperability of connected medical devices, and adhering to strict regulations.
Téléchargements


Glossaire
Mini-invasive : Technique chirurgicale qui réduit au maximum la taille des incisions nécessaires pour effectuer une intervention, limitant ainsi les traumatismes aux tissus et favorisant une récupération rapide.
Micro-invasive : Une évolution des techniques mini-invasives, impliquant des instruments encore plus fins et des incisions presque imperceptibles, souvent utilisées dans des interventions spécialisées comme la neurochirurgie.
VLAN (Virtual Local Area Network) : Réseau local virtuel permettant de segmenter un réseau informatique physique en plusieurs réseaux logiques distincts, augmentant la sécurité et l'efficacité de la gestion des données dans des environnements complexes tels que les hôpitaux.
EAI (Enterprise Application Integration) : Technologie ou ensemble de processus permettant d'intégrer et d'harmoniser les flux de données entre différentes applications utilisées dans une organisation.
Norme HL7 (Health Level Seven) : Norme internationale destinée à faciliter l'échange électronique de données de santé entre différents systèmes d'information.
Norme DICOM (Digital Imaging and Communications in Medicine) : Standard international pour gérer, stocker, transmettre et partager des images médicales, essentiel pour les dispositifs d'imagerie comme les scanners et arceaux.
Bastion : Dispositif ou système de sécurité informatique utilisé pour protéger les communications et l'accès à des équipements critiques, comme les robots chirurgicaux, en établissant des connexions chiffrées et sécurisées.
IoMT (Internet of Medical Things) : Réseau d'objets connectés dédiés à la santé, permettant de collecter, transmettre et analyser des données en temps réel pour optimiser les soins.
HDS (Hébergeur de Données de Santé) : Organisme agréé en charge de la sécurisation et de l'hébergement des données médicales, assurant leur disponibilité même en cas de panne ou d'attaque.
Mémoire Complet
Chirurgie 4.0 : Intégration du numérique au bloc opératoire
Introduction
Le domaine de la santé entre dans une ère de transformation : celle de la chirurgie 4.0. Inspirée par les concepts de l’Industrie 4.0, cette évolution repose sur des technologies telles que l’intelligence artificielle (IA), l’Internet des objets médicaux (IoMT), les robots chirurgicaux, l’imagerie avancée et les jumeaux numériques. Ces outils modernisent le bloc opératoire, créent des environnements connectés et intelligents pour améliorer la qualité et la sécurité des soins [20].
L’Industrie 4.0 a marqué une rupture en intégrant des systèmes interconnectés capables d’optimiser les processus en temps réel. Les blocs opératoires suivent également ce même principe : planification assistée par IA, modélisation 3D en temps réel et interventions robotisées [20] (cf : figure 1).
Figure 1 - Schéma sur l'évolution chirurgical (source : auteurs)
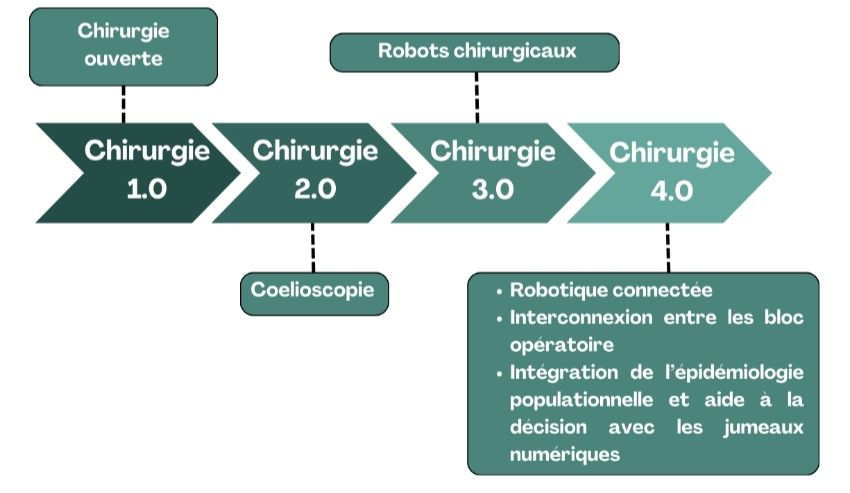
Les chirurgiens pourront alors alimenter les données opératoires et leurs résultats dans les modèles informatiques et alimenter les data des logiciels embarquant l'intelligence artificielle.
Cette transformation ne se limite pas aux innovations techniques. Les services biomédicaux jouent un rôle clé dans l’installation, la maintenance, et la formation des utilisateurs. Ils doivent également relever des défis complexes, comme la cybersécurité et l’interopérabilité des dispositifs, tout en garantissant une gestion financière durable.
Pour les patients, les bénéfices sont significatifs : interventions moins invasives, meilleure récupération, et réduction des complications post-opératoires. Les chirurgiens, quant à eux, bénéficient d’outils qui améliorent leur confort, leur précision
et leur sécurité.
Ce mémoire propose une étude sur l'intégration des salles multimodalité et des robots chirurgicaux dans le bloc opératoire, en mettant en exergue les défis d'installation qu'ils représentent. Il commence par une présentation de l'évolution du bloc opératoire, suivie d'une analyse générale des salles multimodalité et des robots chirurgicaux, pour ensuite aborder les enjeux liés à leur implémentation et les solutions envisageables pour surmonter ces défis.
I. L’intégration du 4.0 au bloc opératoire
Avant d’aborder le fonctionnement et l’intégration des salles multimodalités et des robots chirurgicaux au bloc opératoire. Il est d’abord nécessaire de définir celui-ci et de comprendre son évolution au cours du temps et en quoi cela est nécessaire.
Selon L'Académie Nationale de Médecine, le bloc opératoire est finalement “une enceinte dédiée à des actes invasifs à visée diagnostique et/ou thérapeutique effectués soit à ciel ouvert, soit par fonction et par voie endoscopique, qu’il s’agisse d’actes programmés, ambulatoires ou urgents”. [32]
1. Le bloc opératoire classique
Historiquement, les blocs opératoires étaient organisés autour de besoins simples : fournir un environnement stérile et des outils essentiels pour permettre des interventions chirurgicales sûres. Les équipements se limitaient à ce que représente
la figure 2 :
- La table d'opération réglable : Autrefois fixe et simple, la table d'opération est aujourd'hui conçue pour être entièrement ajustable, ce qui permet de positionner le patient avec précision et de s'adapter aux besoins spécifiques de chaque intervention.
- Les scialytiques avancées : Remplaçant les sources de lumière basiques, les lampes modernes fournissent un éclairage LED intense, ajustable et sans ombre, indispensable pour une visibilité parfaite de la zone opératoire.
- L’équipement d'anesthésie : Avant, l'anesthésie était donnée de façon assez simple et parfois imprécise. Aujourd'hui, les machines modernes permettent de doser l'anesthésie avec précision tout en surveillant en permanence les signes vitaux du patient.
- Les systèmes de monitoring des constantes vitales : Aujourd'hui, ils sont essentiels pour assurer la sécurité du patient. Ils permettent de surveiller en temps réel des informations comme la fréquence cardiaque, la tension artérielle et d'autres données vitales.
- Le matériel chirurgical spécialisé : Les instruments de base d'autrefois ont évolué pour devenir des outils beaucoup plus précis, comme les systèmes d'endoscopie, adaptés à des interventions spécifiques.
- L’environnement stérile et ergonomique : Les progrès dans les matériaux de construction (sols, murs, plafonds) et la gestion de l'air stérile (flux laminaire) minimisent les risques d'infections.
Figure 2 - Bloc Opératoire classique a CH des Quatres Villes [28]

Cependant, ces environnements montrent leurs limites dans des interventions nécessitant une grande précision ou dans des contextes où l’optimisation des ressources est indispensable. L’absence d’automatisation ou de systèmes avancés de guidage augmente la fatigue des équipes et peut compromettre la qualité des soins. Ces contraintes se traduisent par : une durée opératoire prolongée, une difficulté à gérer les interventions complexes et un risque d'erreurs accru dans
certaines procédures délicates.
2. Les défis majeurs des blocs opératoires traditionnels
Dans leur configuration actuelle, les blocs opératoires classiques peinent à répondre aux besoins croissants des établissements de santé et des équipes médicales. Ces défis se manifestent principalement à travers :
- Un accès limité aux données en temps réel : L’absence d’interconnexion entre les équipements rend difficile une prise de décision rapide et éclairée.
- Une charge de travail accrue pour le personnel : Les équipes soignantes doivent gérer manuellement des tâches répétitives, amplifiant leur fatigue, notamment lors d’interventions longues.
- Une évolution nécessaire vers les nouvelles pratiques chirurgicales : Les procédures mini-invasives ou guidées par imagerie nécessitent des technologies de pointe qui ne sont pas disponibles dans les blocs classiques.
Ces limitations, bien que gérables pour des interventions standard, deviennent problématiques lorsque les exigences en précision, rapidité et sécurité augmentent.
3. La transition vers un bloc opératoire 4.0
Pour commencer, la gestion du bloc opératoire est un élément majeur pour garantir une bonne prise en charge des patients et d’améliorer l’organisation des différentes salles d’opération.
Pour cela, l’information des blocs opératoires devient une solution afin d’optimiser le fonctionnement des différentes unités. En effet, une évolution considérable de la gestion des équipes médicales avec l'implantation de nouveaux logiciels et l'arrivée des technologies numériques optimise l’organisation du bloc et le suivi du parcours patient.
Face à l’évolution constante des besoins en chirurgie, l'introduction des nouvelles technologies au bloc opératoire est devenue bénéfique pour les patients et les soignants. Des dispositifs comme l’imagerie avancée et les robots chirurgicaux ne se contentent pas de combler les limites des pratiques traditionnelles, ils permettent de faire évoluer la chirurgie traditionnelle en répondant à certaines problématiques et favorisent une chirurgie de moins en moins invasive pour améliorer la prise en charge
du patient.
Bien que les dispositifs médicaux classiques restent toujours utilisés au bloc opératoire, leur évolution sera nécessaire pour répondre aux défis des pratiques chirurgicales en constante évolution. La chirurgie 4.0 vise à optimiser le parcours de soins du patient et tendre vers des interventions mini-invasives grâce à la combinaison entre les données per-opératoires et les données obtenues lors de l’intervention chirurgicale. L'évolution de cette démarche mène vers une chirurgie personnalisée.
Cependant, ces technologies sont des dispositifs complexes et coûteux. Grâce de nombreuses recherches et des différents retours d'expérience obtenus, il a été décidé de se concentrer spécifiquement sur les salles multimodalités et les robots chirurgicaux. En effet, ces technologies permettent d’illustrer les différentes problématiques d’implémentation existantes.
II. Salle multimodalité
Les salles multimodalités intègrent plusieurs technologies d’imagerie avancée en un seul environnement, répondant aux besoins grandissant concernant la précision et l’efficacité des actes chirurgicaux. Elles permettent la fusion d’image entre des différentes modalités d’imagerie pour une vision plus complète et précise.
Selon un communiqué de presse du CHU Besançon, « la salle multimodale de radiologie interventionnelle intègre, dans un environnement opératoire, un scanner interventionnel et un arceau d’angiographie, dont la combinaison confère au geste
chirurgical une précision inégalée. » [27]
Historiquement, ce sont des salles de radiologie interventionnelle qui ont évolué pour permettre la réalisation de gestes chirurgicaux. Aujourd'hui, ces salles sont très polyvalentes et permettent de traiter de nombreuses pathologies. En termes d’organisation, un manipulateur radio est toujours présent avec le chirurgien.
Figure 3 - Solution Nexaris™ par Siemens Healthineers [9]
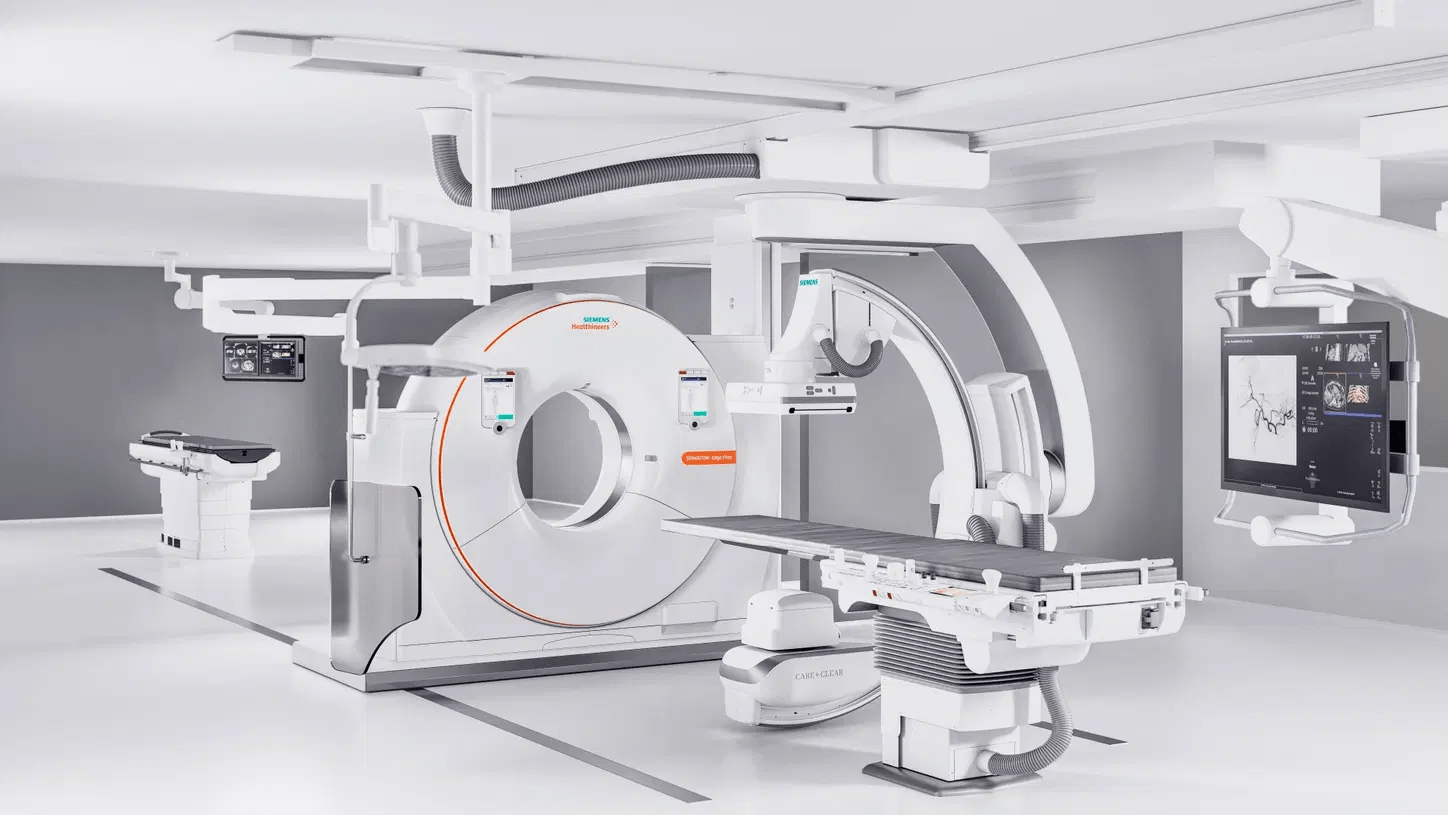
Ces salles intègrent des équipements avancés, tels qu’un arceau de bloc fixe créé pour la fusion d’images, combiné avec un scanner interventionnel comme présenté en figure 3.
Les salles multimodalités sont, aujourd’hui, conçues de manière modulaire, avec des solutions innovantes comme des systèmes de traitement d’air adaptés aux différentes normes ISO. Cette modularité permet également d’intégrer des technologies avancées, telles que des robots chirurgicaux, ou de s’ajuster à des exigences spécifiques pour certaines pathologies complexes.
Ces salles regroupent plusieurs technologies fonctionnant ensemble pour répondre aux différents besoins des médecins et des patients tout en garantissant leur sécurité.
Grâce à la fusion d’image, cette structure permet d’améliorer la visualisation en temps réel des zones anatomiques et permet aux professionnels de santé de réaliser des procédures de plus en plus complexes.
Le fonctionnement des deux dispositifs cités précédemment sera présenté en mettant en évidence leurs spécificités et leur complémentarité au sein de la salle multimodalité.
1. Composants principaux
a. Arceaux de bloc opératoire
Les arceaux de bloc opératoire (figure 4) sont des dispositifs d'imagerie utilisés pour obtenir des images radiologiques pendant une intervention chirurgicale. Leur capacité à capturer des images en temps réel en font un outil essentiel pour les chirurgiens.
Les arceaux de bloc opératoire offrent une combinaison unique de mobilité, de précision et de polyvalence, répondant parfaitement aux exigences des blocs opératoires modernes. En salle d'angiographie, on utilise un arceau de radiologie fixe qui fournit des images 2D dynamiques et en temps réel pendant l’intervention.
De plus, contrairement aux scanners, l'arceau de bloc opératoire émet des niveaux de rayonnement réduits, garantissant une sécurité optimale pour les patients et le personnel médical.
Aujourd’hui les fabricants leaders sur le marché de l’imagerie, comme Philips, proposent des plateformes telles que Azurion, conçues dans le but de minimiser autant que possible l’exposition aux rayonnements, ici DoseWise, et ce tout en garantissant une bonne qualité d’image. [12]
Figure 4 - Arceau fixe Philips
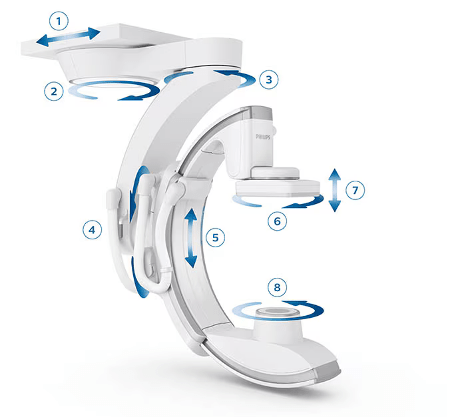
b. Scanner interventionnelle
Le scanner médical utilise un faisceau de rayons X émis par un tube rotatif autour du patient. Les rayons traversent le corps et sont capturés par des détecteurs qui envoient les données à un ordinateur. Celui-ci reconstruit des images 3D détaillées des organes, tissus et os. Contrairement aux radiographies traditionnelles, le scanner offre des coupes transversales précises, permettant de visualiser les anomalies avec une résolution élevée. Grâce à une acquisition rapide d’images multi-coupes, cette technologie réduit l'exposition aux rayons X tout en améliorant l'efficacité des examens. En facilitant la détection des lésions, des tumeurs ou des fractures complexes, elle garantit également un diagnostic précis.
Une des applications courantes de l’arceau est l’embolisation, dans le cadre de maladie tumorales par exemple. La figure 5 illustre la détection automatisée des artères prostatiques en 3D lors d’une embolisation. Dans ce cas l’utilisation de la fluoroscopie seule ne suffit pas. Il est nécessaire d’effectuer des injections de produits de contraste répétées qui permettront de mieux repérer les lésions. Les acquisitions 3D obtenues à l’aide du scanner facilitent davantage le repérage des différentes lésions et la navigation endovasculaire. La fusion d’image permet ensuite d’obtenir une cartographie complète offrant la possibilité de contrôler les images 3D en temps réel.
Figure 5 - Fusion d'images d'un scanner allié à un arceau [17]

2. L'association d'un Scanner à un Arceau de Bloc
L’association d’un scanner et d’un arceau de bloc opératoire est devenue indispensable dans les salles multimodales pour les interventions chirurgicales complexes.
Elle permet d'associer les deux types d’imagerie, préopératoire avec le scanner et de fusionner cette image à celle obtenue en temps réel via l’arceau de bloc comme présenté en figure 4. Néanmoins, il est aussi possible d’utiliser le scanner au cours de l’intervention. [17]
Cette multimodalité permet de réduire considérablement les doses de rayons X administrés au patient, mais aussi de limiter l’injection de produit de contraste, nocifs pour les reins. En effet, une meilleure visualisation de la zone à traiter permet au médecin de mieux s’orienter. Il est également important de noter que les images préopératoire du scanner permettent de faire du post traitement et d'isoler numériquement certaine artère et veine abîmée.
L’arceau peut être utilisé en continu pour des images rapides en temps réel. Le scanner, quant à lui, est utilisé à des étapes stratégiques pour produire des images précises et détaillées. Cette approche réduit le besoin d’organiser d’autres interventions, évitant ainsi au patient de se déplacer en salle de radiologie pour effectuer un scanner. Enfin, elle permet de prendre des décisions éclairées lors de l’intervention, et ce tout en optimisant le temps de la chirurgie.
a. Des applications cliniques diverses
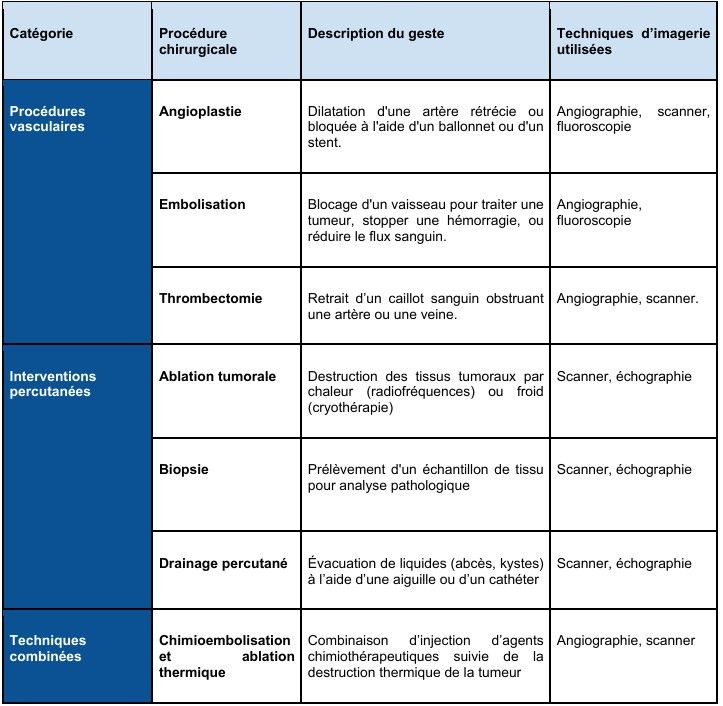
Les procédures cliniques par abord vasculaire ou percutanée sont de plus en plus courantes en médecine interventionnelle. Elles permettent d'effectuer des traitements diagnostiques et thérapeutiques avec une grande précision tout en minimisant les risques pour les patients, grâce à l'utilisation de techniques mini-invasives. Pour optimiser ces interventions, plusieurs modalités d'imagerie, telles que la fluoroscopie, l'angioscopie et le scanner, jouent un rôle clé. Ces technologies permettent de guider les médecins en temps réel et de visualiser avec une grande précision les zones à traiter. Le tableau présenté en annexe 1 apporte un aperçu des principales procédures cliniques dans ces domaines, ainsi que les techniques d'imagerie associées.
Les salles multimodales trouvent également leur utilité lors d’examens cardiaques, notamment grâce aux caractéristiques techniques avancées des scanners modernes, comme les détecteurs de haute précision. Ces techniques fournissent des images détaillées, et facilitent des diagnostics cardiovasculaires précis et des traitements ciblés.
b. Exemples de Fabricants
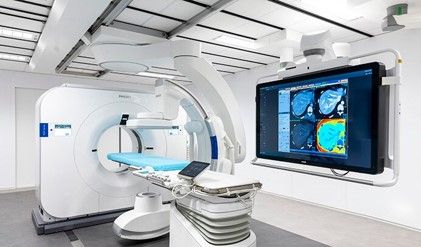
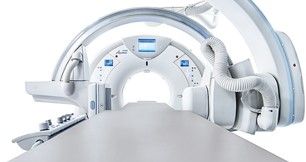
Les constructeurs comme Siemens Healthineers, Canon Medical Systems et Philips (cf : figure 6 et 7 ) sont des leaders dans la fabrication d'équipements pour les salles de multimodalité. Leurs systèmes intègrent l'imagerie en temps réel, la navigation chirurgicale et des logiciels de gestion de données médicales.
Figure 6 - Philips Azurion plus Scanner Spectrale[10] Figure 7 - Canon Hybride Système D'angiographie
c. Investissement
Les salles multimodalités sont des systèmes complexes à installer, car elles nécessitent des dispositifs médicaux relativement coûteux. Par exemple, la création d’une salle de radiologie interventionnelle s’élève à 1 858 500 € TTC. À cela s’ajoutent des équipements tels qu’un scanner spectral (1 294 665,85 € TTC) et la réorganisation du bloc opératoire (1 106 231,80 € TTC), selon le CHU de Besançon [27].
III. Robots Chirurgicaux : Entre Innovation et Expertise Humaine
Depuis leur intégration dans les blocs opératoires à la fin des années 1980, les robots chirurgicaux ont transformé la prise en charge de millions de patients, offrant des interventions plus rapides, précises et sûres. Partout dans le monde, notamment en France, ces technologies repoussent les limites avec des applications dans des domaines variés comme : la chirurgie optique, de la colonne vertébrale, du système digestif, des reins et de la prostate.
La chirurgie robotique se divise en trois sous-catégories selon le degré d’interaction avec le chirurgien : supervisée, télé-chirurgicale et à contrôle partagé, ces deux dernières étant les plus répandues. [36],[24]
1. Les Robots à Contrôle Partagé : Une Nouvelle Ère pour la Chirurgie
Pour commencer, les systèmes de contrôle partagé impliquent une collaboration étroite entre le robot et le chirurgien, où ce dernier dirige l’opération et le robot assure une manipulation précise et stable de l’instrument. L’un des robots les plus répandus sur le marché est la gamme ROSA, développée par Zimmer-Biomet. Elle inclut le ROSA One Brain, dédié à la neurochirurgie mini-invasive, et la gamme ROSA Robotics pour les interventions orthopédiques. [13],[3]
Le ROSA One Brain assiste plusieurs procédures cérébrales, telles que la stéréoélectroencéphalographie (SEEG) et la stimulation cérébrale profonde (DBS). Cette technologie apporte sa contribution dans le traitement des maladies dégénératives, des tumeurs ou encore des déformations de la colonne vertébrale. Elle facilite la planification et l'exécution des actes chirurgicaux complexes, incluant une perceuse de précision pour intervenir au niveau du crâne. [4]
a. Le Fonctionnement de la ROSA Brain ONE
La planification des opérations est une étape importante avec ce robot. En effet, grâce à un logiciel adapté, des cartes 3D, comme présenté en figure 8 , sont obtenues à partir de données d’imagerie médicale, tels que le scanner ou l’IRM, de l’organe à opérer. Cela permet au chirurgien de développer une stratégie chirurgicale efficace et optimisée. Ce robot joue finalement un rôle similaire au GPS afin d’éviter les structures critiques du cerveau. [4]
Figure 8 - Logiciel Préopératoire du Robot - Rosa ONE [4]
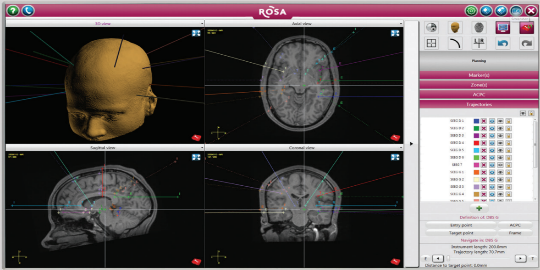
Avant que l’opération ne commence, le robot utilise ses lasers et capteurs pour analyser la position et l’anatomie du patient. L’écran fixé au robot, permet au chirurgien d’observer les nouvelles images obtenues et de les comparer avec les images préopératoires. Une phase de calibration est également nécessaire afin d’aligner le robot avec le patient. Finalement, pendant l’opération, le robot assite le chirurgien en guidant ses instruments, qui sont eux-mêmes visualisés en temps réel sur les images du patient. [4]
Les études montrent que le ROSA One Brain (cf : figure 9) peut accélérer plusieurs procédures neurochirurgicales. Par exemple, une étude menée par Gonzalez-Martinez et al. a démontré que les procédures SEEG assistées par robotique étaient en moyenne 3 heures et 42 minutes plus rapides. [4]
Figure 9 - Robot Rosa ONE Brain [4]

En termes de coût, un robot de la gamme ROSA, comme le ROSA One Brain, représente un investissement significatif pour les hôpitaux, avec un prix de base à partir de 300 000 euros, auquel s'ajoutent les équipements et services, portant le coût total à environ 500 000 euros. [15], [11]
b. Le Mako de Stryker : Une révolution dans la robotique orthopédique
Le MAKO SmartRobotics de Stryker (cf. : figure 10), largement utilisé en chirurgie orthopédique pour la pose de prothèses, s’impose comme l’un des systèmes robotiques leaders sur le marché, avec plus de 1 000 000 de procédures réalisées dans le monde jusqu’en 2023.
Figure 10 - Robot Mako SmartRobotics de Stryker [5]

Par exemple, depuis son installation au printemps 2021, ce robot a déjà été utilisé pour traiter près de 1 000 patients à l’Hôpital Lyon Sud, illustrant son adoption croissante à l’échelle locale. [5],[21]
Il se distingue par l’intégration de trois composants clés : une planification 3D basée sur la tomodensitométrie (cf : figure 11), une technologie haptique AccuStop et une plateforme de données interactives, permettant de présenter directement aux patients les résultats pour les chirurgies du genou partiel, total, et de la hanche totale. Chaque type de procédure bénéficie d’un logiciel de pré-planification adapté, optimisant ainsi la précision et l’efficacité des interventions. [5]
Figure 11 - Logical Préplanification de Stryker après le CT Scan [5]
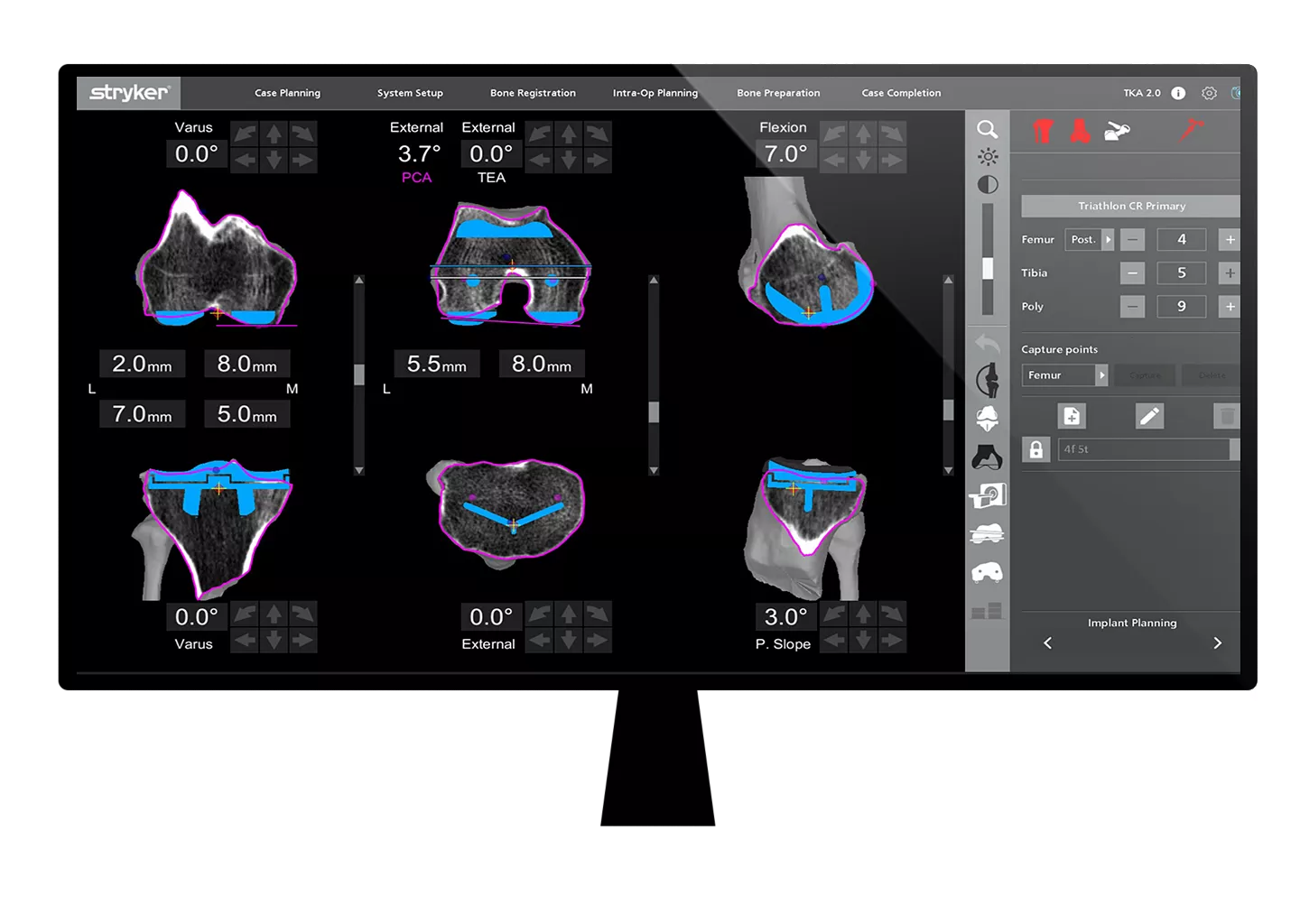
Stryker a récemment lancé le Total Knee 2.0, conçu pour améliorer l’expérience et l’efficacité des chirurgiens en arthroplastie du genou. Cette technologie intègre un planning 3D avec un nouveau tensiomètre numérique pour évaluer la stabilité du genou en cours d'opération (cf. figure 11). Le prix de ce robot dépasse 1 million USD et, comparé à son concurrent, le ROSA One, il offre une précision supérieure grâce à son bras robotique et au feedback haptique, selon une étude de Walgrave et Oussedik (2022). [10],[33]
a. VELYS : La Révolution Orthopédique Sans Pré-Scan
Le VELYS™ Robotic-Assisted Solution (cf : figure 12), développé par DePuy Synthes, une division de Johnson & Johnson, a été conçu pour améliorer la précision chirurgicale grâce à une technologie sans tomodensitométrie, optimisant ainsi le placement des implants. Depuis son lancement en 2017, le Mako Total Knee de Stryker a atteint 27 installations en France, tandis que le VELYS™, introduit plus récemment, compte déjà 3 unités installées depuis juin 2024, illustrant une adoption rapide et un intérêt croissant pour cette nouvelle technologie. [18]
Le robot VELYS™ intègre plusieurs technologies avancées qui simplifient le processus chirurgical tout en améliorant la précision et l’efficacité, sans nécessiter de pré-scanners. Les deux technologies clés qui sont responsables pour l’imagerie sont L’ADAPTIVE TRACKING™ et le PROADJUST™. La première utilise une caméra haute vitesse combinée à des réflecteurs optiques PURESIGHT™. [1]
Figure 12 - Système VELYS™ de Johnson & Johnson [18]

Ensemble, ces outils ajustent et contrôlent en temps réel le plan de résection, garantissant des résultats précis et cohérents. Le PROADJUST™ va faciliter la planification chirurgicale grâce à une interface claire et intuitive. Sur une seule page, le chirurgien peut ajuster rapidement les paramètres pourpersonnaliser l'alignement et l'équilibre en fonction des tissus mous du patient (cf : figure 13). [1]
Figure 13 - Logiciel de Planification avec technologie PROADJUST™ [18]

Il y a également deux autres technologies comme le NATURAL CONTROL™ qui assure le maintien du plan de coupe de la scie, permettant au chirurgien de réaliser des coupes précises avec un contrôle direct, sans l'utilisation de blocs de coupe traditionnels. ACCUBALANCE™ Graph fournit des données sur la stabilité des tissus mous pendant toute l'amplitude du mouvement, aidant le chirurgien à visualiser et anticiper la stabilité articulaire avant de procéder aux coupes osseuses. [1]
2. La chirurgie à portée de clic : l’incroyable avancée de la téléchirurgie
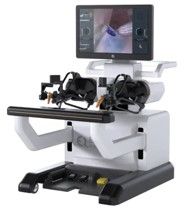
L’évolution de la robotique a permis de réaliser des avancées majeures dans le domaine médical, notamment avec l'avènement de la téléchirurgie. Elle est définie comme un geste chirurgical à distance assisté par ordinateur. C’est une modalité qui appartient à la télémédecine. Les plateformes de téléchirurgie permettent de reproduire, guider, assister et même d’améliorer les gestes des chirurgiens à distance. Les robots télémanipulateurs Zeus et Da Vinci (cf : figure 7 et 8) ont été les premiers à introduire une distance entre le chirurgien et le patient. [34],[36]
a. Fonctionnement général des robots de téléchirurgie
Le chirurgien est assis sur une console et va pouvoir contrôler le robot à distance par l’intermédiaire de joysticks et de commandes aux pieds. Les bras du robot sont positionnés dans les cavités du patient dans le cas d’opération laparoscopique. L'installation différera selon l’application clinique. Entre les deux entités, un câblage réseau permet la transmission des informations du chirurgien vers le patient (commandes des bras articulés et des instruments) et du patient vers le chirurgien (informations vidéo). Ils sont capables de combiner différents dispositifs au sein d’une même plateforme. En associant différentséquipements d’imagerie, d’instrumentation chirurgicales, de prothèses et d'ancillaires, ils utilisent habituellement des endoscopes, des exoscopes et des coeilioscopes. (Caméra introduite dans le corps pour éviter une chirurgie avec une large exposition des tissus) (cf : Figure 14). [34],[36]
Figure 14 - Schéma des étapes de la téléchirurgie [34]
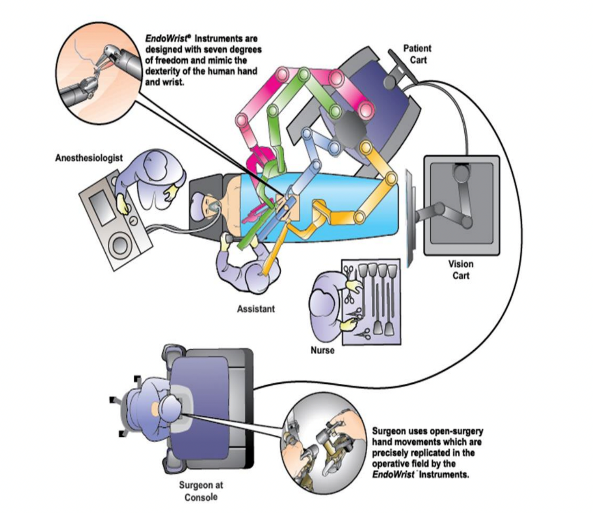
En comparaison au robot à contrôle partagé, les robots de téléchirurgie sont directement équipés d’un système vidéo d’endoscopie ce qui permet d’opérer et de visualiser en temps réel les tissus du patient en 3D. La distance à l’heure actuelle entre le patient et le chirurgien est de quelques mètres. Mais, différentes expériences ont déjà eu lieu, notamment la plus célèbre « l’opération Lindbergh » qui a permis la réalisation d’une cholécystectomie chez une patiente à Strasbourg, par le professeur Jacques Marescaux à New York ce qui à mobiliser de nombreuses ressources informatiques et réseau. [34],[36]
b. Avantages et applications cliniques
Grâce à ces technologies, les mouvements du chirurgien sont reproduits avec plus de précision et de manière plus efficace tout en permettant une chirurgie micro invasive. Le temps opératoire est alors considérablement réduit. Ce type de geste est impossible pour l’homme à reproduire en une seule étape. Cela permet notamment au chirurgien de ne plus souffrir de la fatigue de gestes opératoire et de grandement diminuer l’impact négatif du geste chirurgical pour le patient. (Élimination des tremblements). Les infections et les douleurs sont alors réduites ainsi que la durée d’hospitalisation. Ils sont surtout utilisés en chirurgie dite du « mou », comme la chirurgie digestive, la chirurgie gynécologique, l’urologie ou encore la chirurgie thoracique. [7]
c. Système à port unique
Les robots à port unique permettent de réaliser une intervention mini invasive par une seule incision ou un seul point d’entrée dans le corps. Ils sont utilisés pour des chirurgies complexes avec un accès restreint. Ils sont utilisés en chirurgie digestive, urologique, gynécologique et thoracique. [2]
Exemple : Le Robot Da Vinci SP
Figure 15 - Le Robot Da Vinci SP [19]

Ce robot dispose d’un seul bras équipé de trois instruments multiarticulés et d’un endoscope (cf : figure 15 et 16). [19]
Ce type de robot est particulièrement intéressant pour les chirurgies complexes qui nécessitent des accès chirurgicaux alternatifs et plus étroits. Comme c’est le cas pour les interventions trans-orales. Le bras unique élimine les problématiques de collisions externes, l'entrechoquement des bras et optimise l’espace. [19]
Figure 16 - Instruments du Robot DaVinci [19]

- Prix d’acquisition : 2,5 à 3 millions d’euros.
- Coût des consommables : 2000 à 3000 euros par intervention.
- Coût de la maintenance : 150 000 euros par an.
- Applications cliniques : Chirurgie viscérale, urologique [19]
d. Système multiport
Un robot multiport implique plusieurs incisions pour introduire les instruments dans le corps du patient. C’est le système le plus polyvalent et le plus utilisé lors de chirurgie complexes. Chaque incision sert de point d’entrée pour un outil spécifique. Du gaz est habituellement introduit dans la cavité à explorer (Laparoscopie). Ces systèmes offrent un meilleur contrôle par rapport aux systèmes à port unique. Ce type de robot comporte habituellement 3 à 4 bras robotisés [2]. On peut citer le robot Da Vinci intuitive surgical leader sur le marché ainsi que le robot Hugo RAS de chez Medtronic.
Exemple : Le Da Vinci X et Da Vinci XI.
Le système Da Vinci X se compose d’une console de chirurgie, d’un endoscope, de pince de résection, de pince bipolaire de préhension, de pince d’agrafage et de pince de cautérisation. Il permet d’actionner les différentes fonctionnalités des instruments au pied avec des pédales et de naviguer avec les manettes de la console [2].
Ce robot est également équipé d'une deuxième console qui peut être utilisée soit en chirurgie, pour permettre à un deuxième chirurgien d’assister le premier, soit pour de la formation. En dehors des interventions chirurgicales, le chirurgien peut s’entraîner sur cette console grâce au logiciel da Vinci OS4, en travaillant sur des modèles numériques. De plus, les deux praticiens peuvent partager une vue en 3D de l’opération, offrant ainsi des opportunités avancées d’apprentissage et d’enseignement. [2]
Le Da Vinci XI, modèle le plus haut de gamme, offre des fonctionnalités avancées indisponible sur le modèle X. Notamment un accès anatomique élargi, la technologie Integrated Table Motion (permettant d’ajuster la table d’opération et le positionnement du patient en temps réel) ainsi qu’une potence rotative. Il possède également de nombreuses améliorations ergonomiques, telles qu’une installation automatisée, des réglages peropératoires optimisés, et un accès au patient facilité. En effet, la taille et le positionnement des bras du robot peuvent parfois gêner les équipes médicales pour intervenir auprès du patient. Les bras du Da Vinci XI sont plus fins et multi articulés ce qui améliore leur maniabilité. [2]
- Application clinique : Chirurgie laparoscopique.
- Prix : 1,5 à 2,5 millions d’euros, selon le modèle.
- Coût par intervention : 2000 euros de consommables.
- Coût de la maintenance : 150 000 euros, par télémaintenance.
- Coût : Stérilisation de l’optique à froid (équipement à 115 000 euros) et des bras robotisés.
Figure 17 - Les Systèmes DaVinci [2] Figure 18 - Robot chirurgical ZEUS.[8]


e. Système endoluminale
A la différence des autres systèmes, un système endoluminal permet d’effectuer des interventions chirurgicales mini-invasives à l'intérieur des structures tubulaires naturelle du corps humain, comme les vaisseaux sanguins, l'œsophage, l'intestin, les voies urinaires, les poumons. Cependant il est limité aux zones accessibles par les voies naturelles. Son avantage est qu’Il est extrêmement mini invasif et ne nécessite aucune incision pour introduire les instruments. Ils sont équipés d’un endoscope flexible. Ce type de robot peut se coupler avec des chariots d’arceau chirurgicaux pour coupler plusieurs systèmes d’imagerie. [34]
Application clinique :
- Trans oral : Résection sous-muqueuse, Myotomie, Gastroplastie, fundoplication gastrique, Amygdalectomie, Laryngectomie
- Trans ombilicale : Cholécystectomie, Appendicectomie, Laparoscopie diagnostique, Cystectomie, Néphrectomie, Pyéloplastie. TransAnal : Dissection sous muqueuse, Résection rectum.
- Trans vaginale : Hystérectomie, Ovariectomie, Cholécystectomie, Ablation kyste ovarien.
Prix d'acquisition : 50 000 à 500 000 euros selon les modèles et les fabricants.
Exemple : Robot ION - Intuitive surgical
Figure 19 - Robot Endoquest Robotics [25]
Le Robot Ion d’Intuitive Surgical comporte une aiguille de biopsie et de sonde ainsi que d’un cathéter ionique pour brûler les tumeurs. Il est donc plus adapté en chirurgie oncologique. [2]
Exemple : Robot Endoquest robotics
Figure 20 - Robot Endoquest Robotics [25]

Ce robot polyvalent est conçu pour réaliser une grande variété d’interventions en passant par les orifices naturels. Ce système permet une chirurgie à incision unique, réduisant le traumatisme pour le patient et favorisant des temps de guérison plus rapides. Il est équipé d’une gamme complète d’instruments flexibles offrant 7 degrés de liberté, reproduisant avec précision les mouvements naturels de la main du chirurgien, pour une manipulation optimale et une intervention plus précise (figure 18 et 19). [25]
3. Limites et problématiques d’implémentation spécifique aux robots chirurgicaux.
La stérilisation :
Ce genre de dispositif est réutilisable il faut prévoir une stérilisation à froid avec une machine spécifique sterrad. Ce qui engendre un coût supplémentaire de 90 000 euros. Cependant il faut adapter les paniers et les chariots de stérilisation car les bras et les outils chirurgicaux sont considérables en taille.
Consommables : Coûts supplémentaires en moyenne de 3000 euros de consommables liés à la chirurgie.
Le choix d'acquisition :
Concernant l’achat il est parfois préférable de choisir une location plutôt qu’un investissement car ce sont des technologies qui évoluent et une location sur 7 ans comme pour les machines de radiologie (scanner, IRM) va permettre d'étaler le coût et de rentabiliser les coûts. Si les fonds d'investissement le permettent, il est possible de faire un investissement.
La maintenance :
La télémaintenance et la maintenance engendrent un coût de 150 000 euros par an. Il est important de pouvoir former certains techniciens pour éviter des coûts supplémentaires dans des réparations simples. On met en place un VPN et système bastion pour protéger l’accès informatique de la machine.
La Formation :
La formation sur les robots nécessite une obligation d’un programme d’habilitation. Le chirurgien doit réaliser 40 séances de simulation et avec coefficient de réussite moyen à atteindre. La formation initiale se fait habituellement en interne grâce à la double console dont une console spécifique à la simulation. Par la suite les chirurgiens vont suivre des modules de formation complémentaire à l'IRCAD à Strasbourg ou dans d’autres centres spécialisés.
IV. De l'hôpital à l'écosystème : Implémentation de la chirurgie 4.0
Avec l'émergence de la chirurgie 4.0, l'intégration de dispositifs médicaux avancés tels que vu précédemment est devenue une priorité pour de nombreux établissements de santé.
Au cours du travail, les caractéristiques techniques des robots chirurgicaux et des salles de multimodalités ont déjà été explorées. Cette étude a permis de mieux comprendre leur fonctionnement, leurs composants essentiels ainsi que les technologies sous-jacentes, telles que les systèmes de navigation chirurgicale, l'imagerie en temps réel, la fusion d’image pré et peropératoire et la robotique assistée. Cependant, l'aspect purement technique ne suffit pas à garantir le succès de leur utilisation en milieu hospitalier.
L’implémentation efficace de ces dispositifs complexes repose sur une approche systémique qui dépasse les performances techniques. L'adaptation de l'infrastructure hospitalière, la gestion des flux chirurgicaux, la maintenance préventive et corrective, la formation des utilisateurs et le respect des normes réglementaires sont autant de facteurs clés pour assurer un déploiement efficace et durable. L’ingénieur biomédical joue un rôle central dans ce processus, intervenant à chaque étape pour garantir le bon fonctionnement des équipements, leur conformité aux normes et leur intégration dans les protocoles médicaux existants.
Dans cette partie, l'accent est mis sur les éléments essentiels à optimiser pour assurer une implémentation réussie des robots chirurgicaux et des dispositifs multimodaux au bloc opératoire en milieu hospitalier. Les défis majeurs seront analysés en mettant en avant trois aspects fondamentaux : les dimensions techniques, les facteurs organisationnels et les exigences réglementaires. Cette approche offrira une vision complète et structurée des étapes à suivre pour transformer les blocs opératoires traditionnels en environnements chirurgicaux 4.0.
Il est important de comprendre que ces recommandations sont issues de nos entretiens avec des professionnels et de nos compétences biomédicales. Cependant, suivant les établissements et leur organisation les problématiques ne sont pas les mêmes et les moyens mis en œuvre devront s’adapter à la structure et à l’organisation des équipes. Les recommandations présentées sont des moyens jugés pertinents à partager dans l’objectif d’informer les professionnels hospitaliers, qu’ils soient biomédicaux.
1.Aspect technique
a.Infrastructure Hospitalière Nécessaire
Lors de plusieurs échanges avec des ingénieurs biomédicaux, il a été constaté que les dispositifs médicaux présentés, tels que les robots chirurgicaux, les scanners et les arceaux chirurgicaux, sont des équipements complexes et lourds pouvant dépasser la tonne avec une répartition au mètre carré importante. Leur intégration en milieu hospitalier nécessite des capacités techniques spécifiques au sein des blocs opératoires.
Par conséquent, leur implantation en milieu hospitalier nécessite une évaluation préalable approfondie de la structure du bâtiment. Cette évaluation doit comprendre des études de sol menées par des ingénieurs en génie civil et des experts en ingénierie biomédicale, afin de vérifier que la structure peut supporter de telles charges sans nuire à la sécurité des patients et du personnel médical.
Si la structure du bâtiment s'avère insuffisante, des travaux d'aménagement sont indispensables avant l'installation des équipements. Ces travaux peuvent inclure le renforcement du sol, la redistribution des charges et la stabilisation des fondations.
Une solution utilisée pour renforcer les structures hospitalières consiste à mettre en place des plats en carbone (figure 21) , également appelés plaques ou renforts en fibre de carbone. Ces éléments, légers mais extrêmement résistants, sont fixés directement sur le béton à l'aide de résines époxy haute performance. Leur rôle est de répartir les charges de manière uniforme et de renforcer la capacité portante des sols, plafonds ou murs, sans ajouter de poids excessif à l'infrastructure existante. Parfois en fonction des configurations hospitalières il sera préférable de passer par le dessous ou le dessus.
Figure 21 - Exemple du Plat Carbone [30]

Sur l'image ci-dessus, une application typique des plats de carbone dans le renforcement d'une structure peut être observée. Les plats sont disposés en quadrillage sous le plafond, formant un réseau régulier. Cette configuration permet de réduire les contraintes locales et d'assurer une stabilité accrue sur l'ensemble de la surface. [30]
- Conditions minimales de surface et de hauteur
Pour assurer l'intégration optimale de nos équipements médicaux certaines conditions minimales de surface et de hauteur doivent être respectées :
- Hauteur sous plafond minimale : 2,90 mètres.
Cette hauteur est essentielle pour permettre l'installation de bras articulés, de supports de dispositifs médicaux et de systèmes de ventilation, tout en assurant la sécurité des interventions chirurgicales. - Surface minimale des espaces techniques :
Figure 22 - Graphique des surfaces autour du bloc opératoire - source auteur.e.s

Ce coût peut représenter en moyenne plus de 800 000 euros.
b. Organisation de la structure du bloc opératoire
Les pratiques médicales associées aux nouveaux dispositifs médicaux évoluent rapidement. Ces évolutions imposent une réflexion à long terme sur les changements lors de la construction ou de la rénovation des blocs opératoires. Plutôt que de concevoir ces espaces sur une période de cinq ans, il est essentiel d'adopter une vision stratégique sur vingt ans. Cela permet d'anticiper les évolutions technologiques et organisationnelles tout en précisant les besoins en rénovations coûteuses à court terme.
Pour répondre à ces défis, le déploiement de salles opératoires modulaires constitue une solution pertinente. Ces salles, conçues pour être flexibles et reconfigurables, permettent d'adapter les espaces en fonction des besoins spécifiques. Par exemple, les cloisons amovibles, comme présenté dans la figure 23 peuvent être utilisées pour réorganiser les flux de travail ou créer des zones dédiées à des équipements lourds. Cette modularité est également bénéfique pour répondre à la diversité d’utilisation de la salle en fonction des spécialités, aux évolutions des pratiques chirurgicales ou à des situations exceptionnelles, telles qu'un afflux de patients massifs. De plus, les infrastructures électriques, les réseaux informatiques et les systèmes de câblage modulaires facilitent l'intégration des nouvelles technologies. [14]
Figure 23 - Salle Modulaire Vide [14]

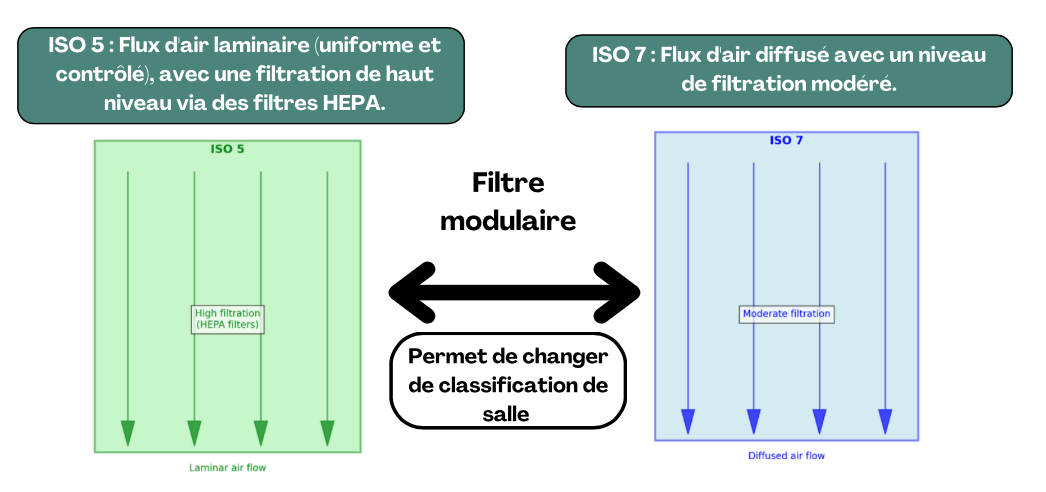
En parallèle, la gestion de la ventilation dans les blocs opératoires est un aspect nécessaire. Les normes ISO définissent les classifications de la qualité de l'air. Il existe ISO 7 pour une salle opératoire standard et ISO 5 pour des interventions nécessitant un environnement stérile renforcé.
Comme illustré en figure 24, la principale différence réside dans les flux d'air et les niveaux de filtration. Des systèmes de ventilation modulables permettent de passer d'une classification ISO à une autre sans travaux majeurs. Cela offre une flexibilité pour les hôpitaux même si cette solution est plus coûteuse. Ces systèmes, équipés de filtres modulaires, permettent de modifier la qualité de l'air sans entreprendre de travaux lourds. Cette flexibilité est un atout majeur pour les hôpitaux cherchant à optimiser leurs infrastructures tout en respectant les normes de sécurité.
Figure 24 - Graphique Comparent ISO 5 et ISO 7 - source auteur.e.s
2.Gestion de Projet d'Implémentation
La mise en place de dispositifs médicaux complexes, tels que les robots chirurgicaux et les systèmes de multimodalité, nécessite une gestion de projet rigoureuse et structurée. L'un des premiers aspects à considérer est de mettre en place un comité de pilotage constitué de l'entièreté des parties prenantes du projet (ingénieur biomédical, DSI, service technique, les personnels soignant, services qualité, services hygiènes, services RH et direction des soins). Un cahier des charges processus est nécessaire avec une mise en comparaison des offres. Ensuite, il est nécessaire d’avoir une planification, qui comprend l'élaboration d'un budget détaillé et d'un échéancier précis. Le budget doit couvrir l'acquisition des équipements, les travaux d'aménagement nécessaires, la formation du personnel, ainsi que les coûts de maintenance. En parallèle, l'échéancier permet de définir les différentes étapes clés du projet, telles que l'analyse des besoins, la sélection des fournisseurs, l'installation, et la validation des dispositifs avant leur mise en service.
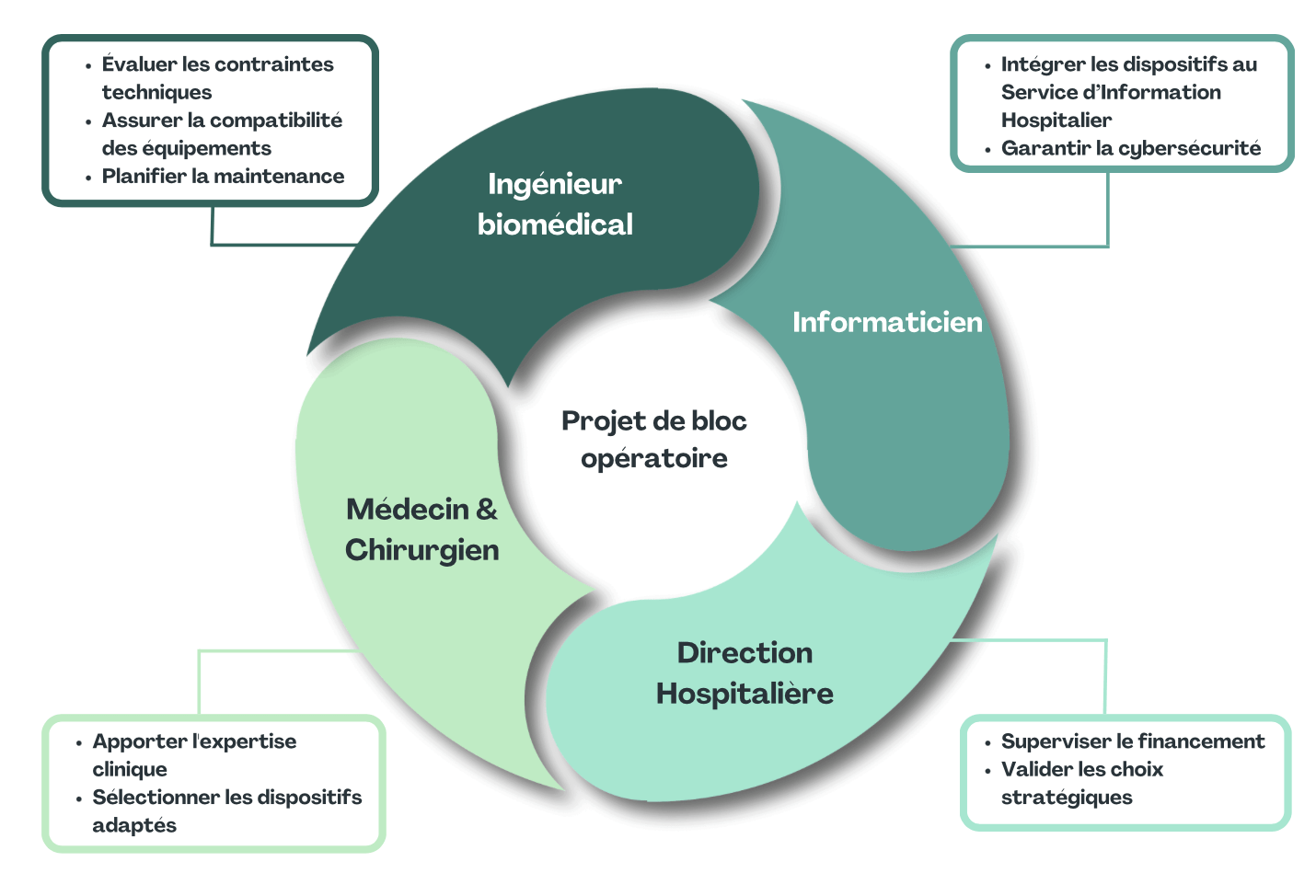
La réussite du projet repose également sur la coordination efficace de multiples acteurs. Ces interactions sont synthétisées dans le schéma ci-dessous qui illustre la coordination essentielle pour mener à bien le projet :
Figure 25 - Graphique avec les différents acteurs dans le bloc opératoire - Source Auteur.e.s
Enfin, il est important de prendre en compte que les protocoles, le placement du personnel et les flux opératoires des différents services vont devoir être modifiés pour pouvoir s’adapter à la technologie créant ainsi des problématiques de temps et organisationnelle.
3.Sécurité des Données Médicales
La transformation numérique des blocs opératoires, avec l'introduction de dispositifs médicaux connectés, a accru les préoccupations liées à la sécurité des données médicales. Ces dispositifs collectent et traitent des informations sensibles, telles que les dossiers médicaux des patients ou les données d'imagerie, qui doivent être protégées pour éviter toute fuite ou utilisation abusive.
La cybersécurité des appareils connectés est une priorité pour prévenir les attaques malveillantes qui pourraient perturber les opérations hospitalières. Cela inclut la mise en place de telles mesures que le chiffrement des données lors de leur transmission et stockage, l'utilisation de pare-feu et de réseaux segmentés, ainsi que des mises à jour régulières des logiciels pour corriger les éventuelles failles de sécurité. Les audits de sécurité périodiques permettent également de détecter et de combler les vulnérabilités avant qu'elles ne soient exploitées.
En outre, la protection des données sensibles doit respecter les exigences du Règlement Général sur la Protection des Données (RGPD). Cela implique la pseudonymisation ou l'anonymisation des informations personnelles, la mise en place de systèmes d'authentification renforcés, et des contrôles stricts pour limiter l'accès aux seules personnes autorisées. Les hôpitaux doivent également disposer de plans de gestion des incidents pour réagir rapidement en cas de violation des données.
Lors des visites et des différentes interviews réalisées, plusieurs points critiques liés à la cybersécurité en milieu hospitalier ont été identifiés. L’un des aspects récurrents observés est l’utilisation fréquente de clés USB dans les blocs opératoires, ce qui soulève plusieurs problèmes potentiels de sécurité.
La dépendance technologique à un support physique aussi petit pose plusieurs questions. Une clé USB peut facilement être perdue, volée ou endommagée, ce qui compromettrait l'accès à des données critiques, comme des paramètres d'équipements, des logiciels de contrôle ou même des dossiers médicaux. Cette vulnérabilité peut engendrer de sérieux risques opérationnels et interruptions de service en cas de panne.
Les clés USB sont des vecteurs de contamination numérique bien connus. Leur utilisation répétée sur différents dispositifs médicaux ou postes informatiques peut favoriser l’introduction de malwares, virus ou ransomwares dans le système d’information hospitalier (SIH). Si aucune politique de sécurité stricte n'est mise en place, ces menaces pourraient facilement se propager dans l’ensemble du réseau hospitalier, perturbant les opérations médicales essentielles.
Pour lutter contre ce problème, il existe quelques solutions qui pourraient être mises en place et qui nécessitent une collaboration entre les fournisseurs de robots chirurgicaux et la Direction des Systèmes d'Information (DSI). L'une de ces solutions consiste à créer un réseau VLAN dédié, reliant les différents dispositifs, notamment ceux utilisés dans le bloc opératoire avec les consoles des médecins dans leur bureau. Ce qui permettrait de pousser les planifications opératoires directement vers les robots. [23]
L'intégration des équipements médicaux connectés dans les blocs opératoires 4.0 exige une gestion rigoureuse de la protection des données sensibles. Pour assurer leur sécurité, les informations générées en continu par ces dispositifs sont enregistrées à deux niveaux : sur un concentrateur interne à l'hôpital et sur un Hébergeur de Données de Santé (HDS) (cf : figure 26) agréé extérieur de l’établissement avec un échange unidirectionnel (il s’agit d’une boite noire qui récupère en continue des données médical). Cette double garantie permet la sauvegarde et la préservation des données même en cas de panne réseau ou de cyberattaque. De plus, les flux de données sont configurés en unidirectionnel, protégeant à toute intrusion ou retour potentiel vers les systèmes critiques de l'hôpital. [26]
Figure 26 - Schéma de HDS [26]

En cas de coupure réseau ou d'infection informatique, les appareils situés à l'extérieur de l'hôpital prennent le relais. Ils continuent de collecter les données et de les stocker temporairement. Une fois la connexion rétablie, ces postes transmettent les informations sécurisées vers les serveurs de l'établissement. Cette architecture assure une continuité du flux de données tout en minimisant les interruptions potentielles liées aux incidents techniques ou aux cybermenaces. Tous ces protocoles sont mis en œuvre afin de garantir un plan de reprise d’activité le plus efficace possible.
Pour sécuriser les interventions à distance, notamment dans le cadre de la télémaintenance, un système de bastion associé à un VPN est mis en place. Ce dispositif établit un tunnel chiffré et sécurisé, garantissant l'intégrité des communications entre les équipes techniques et les équipements médicaux. En particulier les risques d'intrusion extérieure, cette solution permet de maintenir un haut niveau de sécurité tout en assurant la maintenance proactive des systèmes connectés.
4.Interopérabilité et Gestion des Flux de Données
L'intégration des équipements médicaux connectés dans les blocs opératoires 4.0 repose sur une interopérabilité optimale entre les différents systèmes de gestion hospitaliers. Pour y parvenir, l'utilisation d'un EAI (Enterprise Application Integration) jouant le rôle de concentrateur de production de données est essentiel (cf : figure 27). Cet EAI centralise tous les flux de données générés par les dispositifs médicaux et les redistribue vers les logiciels hospitaliers compatibles, garantissant une communication fluide et sans rupture. [31]
Figure 27 - Example des Applications d'un EAI [31]
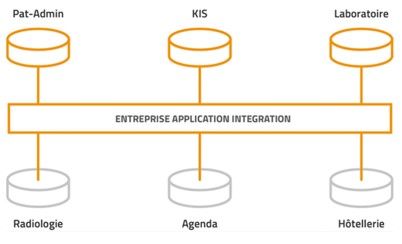
Une passerelle spécialisée, telle qu’un VLAN (figure 28) peut être utilisée pour assurer la conversion et la transmission des données médicales dans les formats appropriés. Des entreprises comme Orange avec leur solution EnevaCom se distinguent par leur expertise dans ce domaine, assurant une gestion efficace et sécurisée des flux critiques, indispensable au bon fonctionnement des infrastructures de santé. [23]
En matière de sécurité informatique, l'implication du responsable de la sécurité des systèmes d'information (RSSI) est primordiale. Il doit superviser et appliquer rigoureusement les protocoles de protection des données à chaque étape du traitement de l'information. Pour renforcer encore davantage la sécurité, l'hébergement des données cliniques sur un Hébergeur de Données de Santé (HDS) agréé est recommandé. Ce dernier agit comme une réplique sécurisée du concentrateur principal, assurant une sauvegarde continue et conforme aux normes réglementaires en vigueur.
Figure 28- Système des VLANs [23]

5. Autorisations et Réglementations en Santé
L'intégration des dispositifs médicaux de pointe dans les établissements de santé est strictement encadrée par des autorisations délivrées par les Agences Régionales de Santé (ARS), conformément aux directives définies par le Programme Régional de Santé (PRS). Ce programme établit la politique de santé publique au niveau régional et fixe le nombre d'autorisations nécessaires pour diverses activités médicales, notamment dans des domaines sensibles comme l'imagerie médicale et la chirurgie robotique.
En matière d'imagerie médicale, certains équipements, tels que les scanners, ne doivent obligatoirement plus d'autorisation spécifique de l'ARS. Cependant, leur installation dans une salle multimodaledoit toujours être déclarée auprès de cette autorité pour garantir leur utilisation conforme aux normes de santé publique. De plus, tous les dispositifs émettant des radiations ionisantes, comme les scanners et certains systèmes d'imagerie interventionnelle, sont soumis à une déclaration obligatoire auprès de l’Autorité de Sûreté Nucléaire (ASN). Cette exigence vise à respecter les normes de radioprotection et de sécurité, tant pour les patients que pour le personnel médical.
En ce qui concerne les technologies chirurgicales avancées, telles que l’implantation de robots chirurgicaux, les ARS doivent délivrer des autorisations de capacité d’implantation. Cette régulation est nécessaire pour éviter un phénomène de « chirurgie publique à deux vitesses », où seuls les centres hospitaliers les mieux financés pourraient subir ces équipements coûteux. Si aucune régulation n'était mise en place, certains établissements publics moins bien dotés seraient privés de technologies modernes, poussant les patients à se tourner vers des structures privées, souvent plus coûteuses.
Pour cette raison, les actes de chirurgie robotique ne bénéficient pas de tarification spécifique à l'acte jusqu’à 2019 près de 300 000 actes dans le système de remboursement de la Sécurité sociale. Cela évite que les établissements privés, qui ont davantage de moyens pour s'équiper de robots chirurgicaux, ne concentrent toutes les interventions chirurgicales robotisées. Si cette situation survenait, elle entraînerait un déséquilibre important : les patients privilégieraient massivement les cliniques privées, ce qui augmenterait considérablement les dépenses de l'État pour rembourser ces actes périodiques. En maintenant une tarification unique et universelle, l'État prévient cette dérive tout en favorisant une meilleure répartition des interventions entre les établissements publics et privés.
Ainsi, l'application stricte des procédures administratives et des normes de sécurité garantit une utilisation réglementée et équitable des équipements médicaux de pointe, tout en préservant un système de santé inclusif et accessible à tous. Cette régulation permet également de maintenir un équilibre économique en limitant les coûts pour la Sécurité sociale et en favorisant un accès équitable aux technologies médicales de dernière génération.
Conclusion
L’intégration des technologies au bloc opératoire marque une avancée considérable dans les pratiques chirurgicales. En combinant les salles multimodalité, les robots chirurgicaux et autres technologies émergentes comme les jumeaux numériques ou la réalité virtuelle, la chirurgie 4.0 apporte de nombreux avantages dans la prise en charge des patients.
En effet, ce mémoire a démontré que ces innovations offrent une précision accrue, une forte réduction des risques opératoires ainsi que des interventions de moins en moins invasives permettant ainsi une meilleure récupération pour le patient et garantissant à la fois sa sécurité et son confort. Pour les chirurgiens, la chirurgie 4.0 leur permet une meilleure planification des procédures chirurgicales, une assistance en temps réel et une optimisation des gestes chirurgicaux complexes.
Malgré ces nombreux avantages, il est important de noter que l’implémentation de ces technologies nécessite la mise en place d’infrastructures spécifiques et adaptées, une formation continue et personnalisée des collaborateurs ainsi que du personnel biomédical.
En ce qui concerne la cybersécurité, ce rapport a démontré que celle-ci s’impose comme un point majeur à ne pas négliger. En effet, les dispositifs médicaux devenant de plus en plus interconnectés et intégrés aux systèmes d’informations hospitaliers, protéger les données de santé des patients et la prévention contre les cyberattaques doivent être des priorités pour l’ensemble du personnel.
Pour tirer parti l’ensemble des bénéfices qui sont offerts par la chirurgie, une démarche stratégique correctement coordonnée est nécessaire. Cela implique de développer plusieurs procédures et protocoles robustes, compris et appliqués par tous qui permettront de renforcer la formation des équipes et de garantir la conformité de ces outils aux normes de sécurité qui leur sont applicables. Finalement la chirurgie 4.0 représente une véritable évolution technologique transformant le bloc opératoire en un écosystème intelligent, fiable et centré sur la collaboration entre humain et machine.
Annexes
Annexe 1 – les différents procédures réalisé dans une salle multimodalité avec les techniques d’imagerie [22]