IDS294 – Scanner Spectral à Comptage Photonique
DOI mémoire
https://doi.org/10.34746/ids294Catégories
Les projets ou stages publiés auxquels vous accédez sont des rapports d'étudiants et doivent être pris comme tels. Il peuvent donc comporter des imperfections ou des imprécisions que tout lecteur doit admettre et donc supporter. Il ont été réalisés pendant les périodes de formation et constituent avant-tout des travaux de compilation bibliographique, d'initiation et d'analyse sur des thématiques associées aux concepts, méthodes, outils et expériences sur les démarches qualité dans les organisations ou sur les technologies en santé.
Si, malgré nos précautions, vous avez des raisons de contester ce droit de diffusion libre, merci de nous en faire part (master@utc.fr), nous nous efforcerons d'y apporter une réponse rapide. L'objectif de la présentation des travaux sur le web est de permettre l'accès à l'information et d'augmenter ainsi la qualité des échanges professionnels.
Nous ne faisons aucun usage commercial des travaux de projet ou de stage publiés, par conséquent les citations des informations et l'emploi des outils mis à disposition sont totalement libres. Dans ce cas, nous vous demandons de respecter les règles d'éthique en citant explicitement et complètement vos sources bibliographiques.
Bonne lecture...
Auteurs




Contacts
- Adrien CHARDON : adrien.chardon@outlook.fr
- Yanis GHOUAR : yanis.ghouar@tutamail.com
- Afrilande Donnella HEZAGIRA : hezagiradonnellaafrilande@gmail.com
- Nicolas JOUVET : nicolasjouvet@gmail.com
Citation
À rappeler pour tout usage : A. CHARDON, Y. GHOUAR, A-D. HEZAGIRA, N. JOUVET, « Scanner spectral à comptage photonique », Université de Technologie de Compiègne (France), Master Ingénierie de la Santé, Parcours des Technologies Biomédicales et Territoires Santé, Mémoire de Projet, https://travaux.master.utc.fr/, réf n° IDS294, janvier 2026, https://travaux.master.utc.fr/formations-master/ingenierie-de-la-sante/ids294/, https://doi.org/10.34746/ids294
Avant-Propos
Afin de faciliter la lecture en ligne, certains contenus additionnels n'ont pas été inclus. La version téléchargeable constitue le document de référence intégral et contient l'ensemble des annexes nécessaires à l'approfondissement des analyses présentées.
Résumé
L’imagerie scanner repose sur la production de rayons X, leur interaction avec les tissus biologiques et leur détection afin de former des images tomodensitométriques utilisées en pratique clinique. Les scanners conventionnels, puis l’imagerie spectrale, ont permis des avancées notables en améliorant la caractérisation tissulaire et la différenciation des matériaux grâce à l’analyse énergétique, mais ces technologies restent limitées par les détecteurs à intégration d’énergie qui entraînent un bruit électronique, une superposition des informations spectrales et une forte exposition des patients. Face à ces limites, le scanner à comptage photonique s’impose comme une évolution majeure, reposant sur la détection directe et individuelle des photons X avec une mesure précise de leur énergie, permettant une imagerie véritablement multi-énergétique. Cette technologie offre une amélioration significative de la résolution spatiale, une meilleure caractérisation des tissus, une réduction importante de la dose de rayonnements ionisants et une diminution du volume de produit de contraste administré. Elle ouvre des perspectives cliniques importantes, en particulier en radio-pédiatrie, en cancérologie digestive et en imagerie cardiovasculaire, tout en s’intégrant dans des environnements de travail et des workflows adaptés grâce à des outils de reconstruction avancés. Malgré des contraintes médico-économiques, réglementaires et techniques liées à son installation et à sa complexité, le scanner à comptage photonique représente une avancée vers une imagerie plus précise et plus sûre.
Abstract
Computed tomography imaging is based on the production of X-rays, their interaction with biological tissues, and their detection in order to generate tomographic images used in clinical practice. Conventional CT scanners, followed by spectral imaging, have enabled significant advances, particularly by improving tissue characterization and material differentiation through energy analysis ; however, these technologies remain limited by energy-integrating detectors defaults : electronic noise, spectral information overlap, and important dose requirement. In response to these limitations, photon-counting CT has emerged as a major technological evolution, relying on the direct and individual detection of X-ray photons with precise energy measurement, enabling truly multi-energy imaging. This technology provides a significant improvement in spatial resolution, enhanced tissue characterization, a substantial reduction in ionizing radiation dose, and a decrease in the amount of administered contrast medium. It opens important clinical perspectives, particularly in pediatric radiology, digestive oncology, and cardiovascular imaging, while integrating into adapted working environments and workflows through advanced reconstruction tools. Despite medico-economic, regulatory, and technical constraints related to its installation and complexity, photon-counting CT represents a major step toward more precise and safer medical imaging.
Téléchargements


Liste des abréviations
- ALARA : AS Low As Reasonably Achievable
- ANSM : Agence Nationale de Sécurité du Médicament et des produits de santé
- ASIC : Application-Specific Integrated Circuit
- ASN : Autorité de Sûreté Nucléaire
- AEC : Automatic Exposure Control
- CAD-RADS : Coronary Artery Disease – Reporting and Data System
- CCAM : Classification Commune des Actes Médicaux
- CT : Computed Tomography
- CTDI : Computed Tomography Dose Index
- DLP : Dose Length Product
- DQE : Detective Quantum Efficiency
- DSDE : Dual Source Dual Energy
- DSSE : Dual Source Single Energy
- DECT : Dual-Enegy CT
- EID : Energy-Integrating Detector
- HU : Hounsfield Unit
- IQR : Iterative Quantum Reconstruction
- PCD : Photon-Counting Detector
- PCD-CT : Photon-Counting Detector Computed Tomography
- PACS : Picture Archiving and Communication System
- RX : Rayons X
- SNR : Signal-to-Noise Ratio
- SPCCT : Spectral Photon-Counting Computed Tomography
- SPP : Spectral Post Processing
- TAP : Thoraco-Abdomino-Pelvien
- TDM : Tomodensitométrie
- TNC : True Non Contrast
- VMI : Virtual Monoenergetic Imaging
- VNC : Virtual Non Contrast
Scanner spectral à comptage photonique
Introduction
Depuis la découverte des rayons X et l’invention de la radiologie, l'imagerie médicale permet l’étude in-vivo et de manière non invasive du corps humain. Avec le développement de technologies d’acquisition anatomique de plus en plus précises, elle occupe actuellement une place incontournable dans la prise en charge diagnostique et thérapeutique des patients. Parmi les différentes modalités, le scanner constitue l’un des examens les plus pratiqués en raison de sa rapidité et de sa polyvalence. Chaque année en France plusieurs millions d’actes sont ainsi réalisés : 7,3 millions recensés en 2020 [1]. Cette large adoption met en évidence les atouts du scanner conventionnel qui n’est cependant pas exempt de limites techniques et cliniques qui justifient la recherche de solutions technologiques innovantes.
En effet, ce dernier présente plusieurs inconvénients notamment une résolution spatiale maximale (de l’ordre de 0,5 mm) ne permettant pas d’analyser finement certaines structures telles que la lumière coronarienne ou la morphologie des plaques calciques. Le contraste entre les différents tissus, et particulièrement mous, est souvent insuffisant. En effet, les acquisitions n’étant pas tissu-spécifiques, plusieurs types tissulaires présentent des valeurs d’atténuation proches ce qui limite la sensibilité pour certaines pathologies par rapport à l’IRM qui est plus discriminante pour de nombreux organes. Chez certains patients obèses ou lors de scans à faible dose de rayons X, des artéfacts et une diminution du rapport Signal-sur-Bruit (Signal-to-Noise Ratio ou SNR) peuvent apparaître, principalement en raison de l’augmentation du bruit quantique auquel peut s’ajouter le bruit électronique du système lorsque le flux de photons devient très faible. Aussi, la quantification absolue de l’agent de contraste injecté n’est pas possible puisqu’elle résulte de l’atténuation globale mesurée qui combine celle du produit de contraste et des tissus et varie selon l’énergie du faisceau de rayons X. De plus, les agents de contraste iodés usuels posent plusieurs défis : néphrotoxicité, clairance rapide et une non-spécificité biologique qui empêche la détection et le suivi des inflammations ou le biomarquage tumoral notamment. Enfin, l’usage du scanner pour le dépistage de masse ou les contrôles répétés est restreint puisqu’il implique une exposition aux rayonnements ionisants non négligeable et quantifiable par la dose efficace (indicateur dosimétrique de l’exposition des populations aux rayonnements ionisants). Les doses efficaces moyennes en scanographie varient ainsi entre 2 mSv (scanner cérébral sans injection de produit de contraste) et 18,5 mSv (scanner thoraco-abdomino-pelvien ou TAP). À titre comparatif, en radiologie conventionnelle, ces doses sont beaucoup plus faibles et comprises entre 0,05 mSv (radiographie thoracique) et 3 mSv sur certaines radiographies en incluant la scopie de centrage [2]. Ainsi, bien que représentant moins de 15% des modalités de radiologie, les actes de scanographie sont à l'origine des trois quarts des rayonnements ionisants auxquels s'exposent les patients [3], ce qui soulève un enjeu majeur de radioprotection.
C’est dans ce contexte qu’une nouvelle génération de scanner spectral à comptage photonique émerge. Capable de mesurer l’énergie de chaque photon incident, elle promet non seulement une amélioration de la résolution spatiale et du contraste mais également une réduction du bruit, garantissant ainsi une meilleure discrimination des tissus tout en réduisant les volumes de produits de contraste injectés et les doses de rayons X envoyées au patient. Récente, le déploiement de cette technologie en France est encore très limité avec une dizaine d’équipements installés (exclusivement des variantes de la gamme Naeotom Alpha de Siemens Healthineers) parmi les quelque huit-cents scanners conventionnels en service au sein des structures publiques et privées à but non lucratif [1].
Les enjeux autour d’une nouvelle génération de scanners
L’imagerie médicale connaît un essor technologique avec le scanner spectral à comptage photonique. Du point de vue du patient, il promet d'offrir plusieurs bénéfices significatifs. Le principal réside dans l’amélioration de sa fonction diagnostique, la réduction de l’exposition aux rayons X est également primordiale puisqu’elle diminue le risque de pathologies somatiques radio-induites. Par ailleurs, la qualité des images obtenues devrait permettre des diagnostics plus précoces et plus précis : le scanner aurait ainsi contribué à réduire de 54% les coronarographies invasives chez les patients à haut risque [4]. La dose de produit de contraste injecté devrait également diminuer comme vu dans les examens d’angioscanographie où la dose a été réduite jusqu’à 47% et de 38% dans le diagnostic d’embolie pulmonaire [5] [6].
Du côté du constructeur, le développement du scanner à comptage photonique nécessite des investissements massifs en recherche pour l’étude de nouveaux matériaux et de circuits intégrés compatibles avec le traitement de grandes quantités de données. La fiabilité et la précision des détecteurs sont essentielles pour garantir des images de haute qualité, elles sont encadrées par des normes et une réglementation stricte accompagnées de contrôles qualité rigoureux. Sur le plan commercial, l’enjeu réside également dans la compétitivité afin de proposer un scanner innovant capable de séduire les établissements hospitaliers en répondant à leurs besoins [6].
Pour le médecin, le scanner à comptage photonique peut constituer un outil révolutionnaire. La capacité à obtenir des images plus détaillées et à discriminer plus finement les tissus améliore la précision des diagnostics et peut influencer directement les décisions thérapeutiques. Cette technologie facilite la détection précoce de zones séquellaires complexes, et permet un suivi plus précis de l’évolution des traitements. Cependant, l’introduction de ce scanner implique aussi de nombreux défis : les radiologues doivent se former à l’interprétation des images générées, qui peuvent être plus complexes à étudier que celles des scanners classiques, et adapter leurs protocoles pour tirer pleinement parti de cette technologie. Cela nécessite du temps, des ressources pédagogiques et une collaboration étroite avec les équipes techniques pour intégrer ces innovations dans la pratique quotidienne [6] [7].
Au vu de tous ces enjeux, il convient de se poser la question suivante : Quels sont les apports cliniques et techniques du scanner spectral à comptage photonique en imagerie médicale ? Est-ce pour le constructeur juste un moyen de garder une longueur d’avance sur ses concurrents ? Les Établissement de Santé s'équipent-ils de cette technologie dans un souci d’image de l'établissement sans réel apport clinique ?
Ce projet a pour objet de proposer une vision claire sur cette technologie émergente et de servir de support de réflexion pour déterminer si les améliorations apportées justifient son adoption dans les centres de santé.
I. Principes physiques et technologiques du scanner conventionnel et spectral
L’exploration de l’anatomie repose sur plusieurs modalités d’imagerie médicale, conçues pour répondre à des objectifs cliniques et diagnostiques variés. Celles-ci se répartissent en trois catégories : l'imagerie "topographique" qui représente la surface du corps, l'imagerie par projection qui montre l'interaction de radiations dans les tissus selon des directions connues et l'imagerie tomographique qui est une représentation bidimensionnelle en coupe de la distribution spatiale des interactions locales des rayons X avec les tissus à travers le corps humain. C’est sur cette dernière que repose la Tomodensitométrie (TDM) qui permet au scanner ou Computed-Tomography (CT) de mesurer les propriétés des tissus en tout point du corps.
1. Présentation de la tomodensitométrie
1.1. Bases physiques de la production des rayons X
La production des ondes électromagnétiques de haute fréquence (rayons X) est assurée par un dispositif appelé tube radiogène, constitué principalement d’une cathode et d’une anode enfermées dans une enveloppe sous vide. Lorsque le tube est alimenté, un courant électrique chauffe un filament situé dans la cathode et provoque l’émission d’électrons par effet thermoïonique. Ces électrons sont ensuite accélérés à grande vitesse vers l’anode grâce à une différence de potentiel appliquée entre les deux électrodes et fixant l’énergie maximale du faisceau. Le courant (typiquement entre 50 et 500 mA) est régulé par le générateur et détermine la quantité de photons générés tandis que la tension appliquée fixe leur énergie. En effet, une tension d’accélération de 150 kV produit des photons X d’énergie maximale 150 keV. L'énergie moyenne du spectre est largement inférieure du fait de la filtration des photons de basse énergie peu pénétrants (dose inutile à la constitution de l’image radiologique) et de la nature des interactions présentées en Figure 1. Une tension d’acquisition faible réduit la dose et augmente le contraste mais également le bruit. En pratique clinique, le mAs ou charge, défini comme le produit du courant à la cathode (mA) par la durée de son application (s), est aussi contrôlé car il conditionne le bruit et la dose délivrée au patient. On note que la quasi-totalité de l’énergie transférée lors de l’impact est dissipée sous forme de chaleur, si bien que moins d’1% seulement se transforme en rayons X exploitables. Pour cette raison, l’anode est conçue pour résister à de hautes températures (jusqu’à 2.5k °C), souvent sous forme d’anode rotative à dissipation thermique [8].
Le rayonnement X est obtenu par l’interaction des électrons avec une cible anodique généralement en Tungstène et provient de deux origines distinctes :
- Le rayonnement de freinage continu (Bremsstrahlung), provient de l’interaction (accélération, freinage ou changement de direction) d’un électron avec le champ électrique du noyau atomique via l’attraction coulombienne. On a alors une conversion de l’énergie cinétique en rayonnement électromagnétique.
- Le rayonnement caractéristique discret, émis lorsqu’un électron incident expulse un électron interne de l’anode, la réorganisation des couches électroniques entraîne alors la libération d’un photon d’énergie définie (fluorescence).
Figure 1. Spectre d'émission d'un tube à rayons X avec une tension d'accélération de 150 kV. [9]
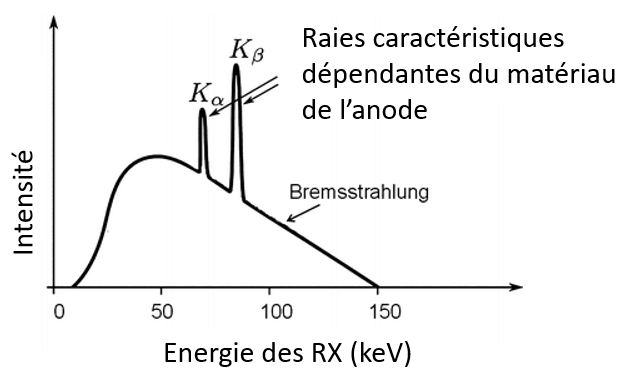
Le spectre obtenu pour un tube est donc le cumul d’un continuum et de raies définies (spectre polychromatique). En scanographie, la gamme d’énergie des rayons X utilisée va de 40 keV et jusqu’à 190 keV dans certains cas. Une fois produits, des filtres primaires absorbent les photons les moins énergétiques (généralement inférieurs à 20 keV [10]). La fenêtre de sortie et le collimateur primaire (diaphragme) assurent ensuite respectivement l'émission des rayons X puis la définition de la forme et des dimensions du faisceau pour limiter la divergence (adaptation aux largeurs d’exploration et aux épaisseurs de coupes désirées) et réduire l’exposition inutile du patient [11]. En effet, dans le corps humain, les photons de basse énergie sont absorbés par les premiers centimètres de tissu et ne sont donc pas exploitables. Les photons X peuvent à présent interagir avec les structures anatomiques que l’on souhaite explorer.
1.2. Interaction des rayons X avec les tissus biologiques
La tomodensitométrie repose sur l’association du spectre énergétique au coefficient d’atténuation linéaire à chaque tissu. Au sein des tissus traversés, les RX interagissent avec la matière selon 2 principaux types d’interactions.
Dans le cas de l’effet photoélectrique, le photon incident interagit avec un électron de cœur (généralement issu des couches électroniques K et L de l’atome) en lui cédant l’intégralité de son énergie et entraînant son éjection (photoélectron). L’atome se retrouve ionisé et va se désexciter soit par libération d’un électron (processus non radiatif Auger-Meitner), soit par réarrangement de son nuage électronique provoquant l’émission d’un photon de fluorescence. Cet effet est prédominant aux faibles énergies (<50 keV) et directement proportionnel à la densité du tissu, il contribue donc au contraste qui est recherché pour produire l’image.
Lors d’une interaction par effet Compton, le photon incident est dévié de sa trajectoire initiale suite à une collision avec un électron de valence qui est alors expulsé en récupérant une partie de son énergie. Le photon atténué et dévié est alors détectable dans une zone différente du lieu d'interaction, l’information spatiale est altérée et le bruit généré augmente. On note que les septa (fines lames de Plomb) de la grille anti-diffusante (ou collimation secondaire) placée avant la détection réduisent l’impact de ces rayonnements diffusés sur la qualité de l’image.
Ces interactions modifient l’intensité et l’énergie des photons qui arrivent au détecteur. La diffusion Rayleigh, qui correspond à la déviation des photons primaires, est très minoritaire et s’effectue sans perte d’énergie mais peut entraîner la formation d’un léger voile diffus sur les acquisitions (bruit). [11] [12]
Selon leur numéro atomique, leur densité (composition chimique) et l’énergie des RX incidents, les tissus traversés sont représentés en plusieurs nuances de gris correspondant aux unités Hounsfield attribuées à chaque pixel. Les os sont ainsi plus visibles que les tissus pulmonaires par exemple (contraste). Enfin, le coefficient d’atténuation des tissus humains étant inversement proportionnel à l’énergie des RX, le contraste est maximal à bas keV (mais le bruit également). Cette notion est importante pour assurer la qualité des acquisitions tout en respectant le principe ALARA (AS Low As Reasonably Achievable) pour minimiser la dose délivrée aux patients. Suite à leurs interactions au sein des tissus du patient, les photons X doivent ensuite être détectés pour produire une image.
1.3. Principe du détecteur à intégration d’énergie
Les détecteurs des scanners conventionnels fonctionnent sur le principe d’intégration d'énergie (Energy Integrating Detectors ou EID) et reposent sur des cristaux scintillateurs (souvent du Gadolinium Oxy-Sulphide ou une céramique dopée) qui convertissent les rayons X en photons visibles. Cette étape est permise par l’absorption des photons X par les électrons du détecteur qui entraîne l’émission de photons de scintillation (lumière visible). Ces derniers sont ensuite détectés par des photodiodes assemblées en matrices de photodétecteurs. Elles convertissent l’énergie déposée en signaux électriques proportionnels à l’intensité des photons reçus. Le phénomène de conversion photons X - photons lumineux étant diffus, des septa optiques réfléchissantes sont utilisées pour limiter le cross-talk entre les cristaux scintillants adjacents en confinant la lumière de chaque élément comme présenté Figure 2.
Enfin, L’épaisseur du détecteur doit garantir l'interaction des photons incidents au sein des cristaux pour éviter l’exposition du patient sans détection subséquente (dose inutile). Cette notion est définie par le paramètre de Detective Quantum Efficiency (DQE) ou efficacité quantique de détection qui correspond à la probabilité qu’un photon absorbé engendre un signal électrique exploitable.
Figure 2. Représentation schématique du détecteur à integration d’énergie. [13]
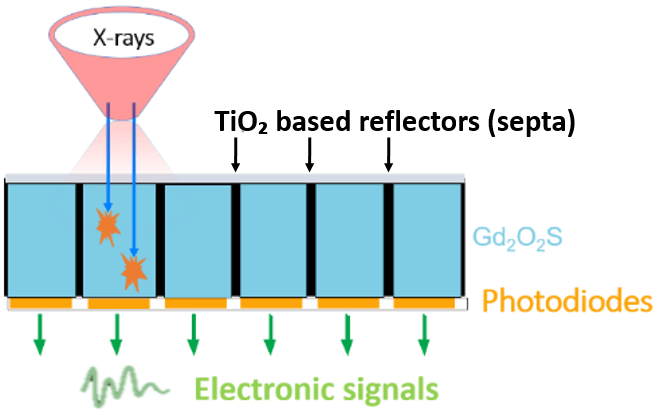
En réduisant la surface effective du détecteur (fill-factor) à cause des zones inexploitables (dead-zone) qui affectent son efficacité géométrique, cette architecture doit compenser la perte de signal par une augmentation de la dose. On identifie plusieurs limites intrinsèques des EID [14] :
- La présence de septa et la dispersion isotrope des photons lumineux au sein d’un même scintillateur limitent la résolution spatiale.
- Les EID intègrent la lumière émise sur une courte période et produisent un signal proportionnel à la somme des énergies des photons incidents. De ce fait, les photons de basse énergie (porteurs d’une grande partie de l’information de contraste) sont proportionnellement moins valorisés (sous-pondérés) dans le signal final, ce qui réduit la sensibilité au contraste et empêche l’imagerie spectrale intrinsèque.
- L’étape d’intégration des signaux et l’électronique associée introduisent un bruit (électronique et de lecture) qui limite la qualité d’image à bas keV. Les EID ne peuvent pas complètement éliminer ce bruit intrinsèque.
Suite à leur production, leurs interactions avec les tissus d’intérêt et leur détection, les signaux recueillis doivent finalement être traités pour permettre la formation de l’image finale.
1.4. Reconstruction de l’image à partir des acquisitions
Le principe de formation de l’image repose sur la mesure de l’atténuation moyenne d’un spectre d'émission dont l’énergie maximale est définie en amont de l’examen. Après le détection des photons X et la production des signaux électriques par conversion indirecte, ces derniers sont amplifiés et numérisés par des convertisseurs analogique‑numérique puis organisés en sinogrammes (ensemble de projections pour chaque angle d’acquisition). La mesure de l’atténuation pour chaque angle permet d’établir des profils d’atténuation qui servent de données brutes pour la reconstruction tomographique.
La conversion des données de projection en image repose sur des algorithmes mathématiques de reconstruction. L’image reconstruite est représentée sous forme d’une matrice numérique bidimensionnelle, généralement de 512×512 pixels pour les coupes axiales en routine clinique, et jusqu’à 2048×2048 sur des scanners haut de gamme pour augmenter la résolution spatiale. Chaque pixel reçoit une valeur de coefficient d’atténuation exprimée en unités Hounsfield (HU), qui reflète la densité locale du tissu. La correspondance entre la valeur numérique d’un pixel et l’affichage en niveaux de gris est gérée par une Look‑Up Table (LUT) qui mappe les valeurs HU aux niveaux de gris affichés, tandis que les paramètres de fenêtrage ajustent la gamme de valeurs HU visibles pour optimiser le contraste selon le type de tissu ciblé. La reconstruction des images peut être réalisée soit par des méthodes itératives telles que l’Iterative Quantum Reconstruction (IQR), consistant à comparer l’image reconstruite aux données de projection mesurées et à ajuster l’image à chaque itération en fonction des écarts observés, soit par rétroprojection filtrée, qui repose sur une reconstruction directe selon une séquence unique d’opérations mathématiques (matrice de convolution ou kernel) [11] [15]. La reconstruction, réalisée par une unité spécialisée (Image Reconstruction System ou IRS), nécessite une importante puissance de calcul et une durée variant entre quelques secondes en rétroprojection filtrée à plusieurs minutes pour les méthodes itératives.
Ainsi, les RX sont quotidiennement utilisés en imagerie médicale pour acquérir des radiographies bidimensionnelles (2D) ou reconstruire des tomodensitométries tridimensionnelles (volumique ou 3D) par empilement des coupes. On parle alors d’unités élémentaires volumiques ou voxels qui sont obtenus par reconstructions multi-planaires (multiplanar reconstruction ou MPR).
Finalement, au cours des dernières années, la tomodensitométrie conventionnelle a connu plusieurs évolutions visant à améliorer les soins médicaux. Ces avancées technologiques ont été appliquées à l'acquisition en réduisant les temps de rotation du tube, en augmentant les plages de tension (kV) et de courant (mA) disponibles et en utilisant une filtration supplémentaire, à la détection en réduisant la taille des cristaux ou encore à la reconstruction avec des algorithmes plus performants. Ces améliorations ont permis de réduire la dose administrée au patient tout en améliorant la qualité de l'image grâce à la réduction du bruit et/ou à l'amélioration de la résolution spatiale et du contraste.
Depuis moins de 20 ans, une autre avancée majeure a été permise par le développement de plateformes de TDM à double énergie, basées sur l'acquisition ou la détection de deux spectres de rayons X à basse et haute énergie, permettant d'évaluer séparément la contribution de l'effet photoélectrique (composition chimique) et de l'effet Compton (densité). L'information spectrale peut alors être utilisée pour générer de nouveaux types d'images qui facilitent la détection et la caractérisation des lésions.
2. Installation complète d’une salle et modèles de scanner
Le scanner utilise un tube motorisé en rotation continue (1 à 4 tours/s) dans un anneau circulaire statique ou gantry, la table sur laquelle est allongé le patient se déplace pour permettre une étude localisée ou corps entier en fonction du protocole d’acquisition. Le pitch ou pas, rapport entre la distance parcourue par la table pendant une rotation du tube et la largeur totale du faisceau de rayons X, est un paramètre important de la durée d’acquisition. En effet, un pitch > 1 (étiré) réduit le temps d’acquisition et la dose délivrée mais augmente le bruit et le risque d'artéfacts de reconstruction. À l’inverse, un pitch < 1 (chevauché) améliore la qualité des images mais rallonge la durée des acquisitions et la dose associée [16].
En complément du scanner, de la table d’examen et de la station de reconstruction des acquisitions, de nombreux autres éléments sont présents dans la salle pour assurer le fonctionnement et la sécurité des examens. On retrouve tout d’abord une armoire pour l’alimentation électrique et pour la climatisation à air ou liquide. Un injecteur peut également être présent pour l’administration des produits de contraste généralement par voie intraveineuse. On note que ce sont les produits de contraste iodés (PCI) qui sont actuellement les plus utilisés pour leur numéro atomique élevé (Z=53) permettant une absorption des rayons se traduisant par un fort contraste à l’image. En raison de leur toxicité, les PCI ne sont pas métabolisés par l’organisme et doivent donc être éliminés par filtration rénale, cela impose un débit de filtration glomérulaire (DFG) suffisant pour éviter une néphropathie au produit de contraste. Enfin, la gestion des protocoles, les paramètres d’injection du produit de contraste (volume et débit) et la visualisation des acquisitions sont possibles depuis le poste de commande informatisé qui assure la protection des utilisateurs pendant les examens (déporté).
2.1. Architecture du scanner
Le scanner peut être décliné en 2 catégories :
- Le scanner monotube est doté d’une seule source de RX et d'une matrice de détecteurs multi-barrettes (Multi-Detector CT) associée et présentée Figure 3. On désigne par barrette une rangée de cristaux scintillants (allant généralement de 800 à 2000 dans l’axe X) disposés en arc de cercle. C’est la juxtaposition de ces barrettes de détecteurs dans l’axe cranio-caudal du patient (ou axe Z) qui permet d’augmenter le nombre de coupes axiales acquises simultanément : généralement 16, 32, 64, 128, voire jusqu’à 320 coupes. Un scanner 128 barrettes avec des cristaux scintillants de 0.625 mm offre ainsi une couverture longitudinale totale de 80mm par rotation (acquisition simultanée de 128 coupes de 0.625 mm d'épaisseur). L’étendue transverse (plan X-Y) est quant à elle définie par le FOV (Field-Of-View) qui module la surface de cristaux scintillants couverte par le faisceau [16].
Figure 3. Représentation des géométries de détecteurs utilisés dans les TDM 64 coupes de 4 fabricants différents. Siemens utilise un système de détecteurs asymétriques avec un foyer flottant (Flying Focal Spot ou FFS) pour doubler le nombre de projections. [9]
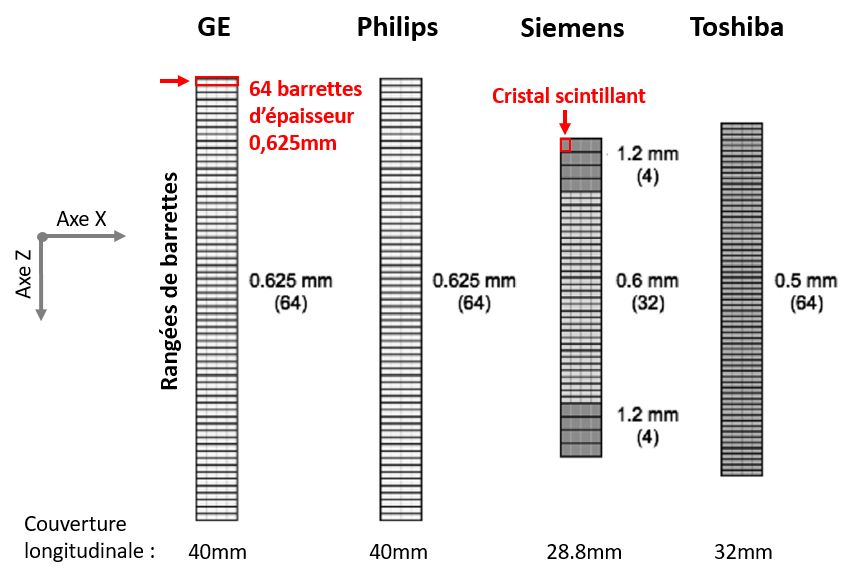
- Le scanner bitube utilise deux systèmes tube-détecteur formant un angle droit et qui tournent simultanément. En tomodensitométrie hélicoïdale, l’ensemble tube-détecteur effectue une rotation continue de 360° (spirale) autour du patient incluant un balayage angulaire de 180° pour l’acquisition des données et les 180° restant utilisés pour la reconstruction de l'image par interpolation et rétroprojection. Dans un système mono-tube, la vitesse de rotation doit être divisée par 2 pour obtenir la résolution temporelle (durée d’acquisition d’une image). L’architecture bi-tube permet de diviser à nouveau par 2 cette valeur et est donc particulièrement intéressante en imagerie cardiaque et pulmonaire pour réduire les artéfacts de mouvements. Cette architecture est très peu répandue du fait de sa complexité et de son coût élevé. Le scanner bitube offre deux modes de fonctionnement dont le “Dual Source Single Energy” (DSSE) qui exploite les deux tubes à une tension identique pour maximiser la résolution temporelle (indispensable en cardio-TDM) et la puissance du flux de photons (patient obèse), privilégiant la netteté des structures mobiles plutôt que l'analyse spectrale des matériaux. À l'inverse, le mode “Dual Source Dual Energy” (DSDE) permet une caractérisation précise des tissus par 2 acquisitions simultanées à des tensions différentes [17].
L’architecture du scanner est donc importante à prendre en compte en fonction des usages cliniques prévus. Avec des champs d’exploration plus avancés, le choix de la technologie de détection spectrale l’est tout autant.
2.2. Particularités techniques de l’imagerie spectrale
En intégrant l'énergie de l'ensemble des photons X reçus, les détecteurs des scanners conventionnels ne permettent pas leur différenciation native. Il reste néanmoins possible d’obtenir une imagerie spectrale par la réalisation d’acquisitions à différents niveaux d’énergie pour permettre la discrimination des tissus ayant des numéros atomiques différents mais des coefficients d’atténuation proches. En pratique, l’atténuation est mesurée à 2 énergies différentes pour chaque pixel de l’image : une tension basse à 80 kV et une haute à 140 kV. L’analyse de la dépendance énergétique de l’atténuation révèle alors les différentes signatures énergétiques. En plus des informations anatomiques fournies jusqu’alors, cette technologie renseigne également sur la composition chimique des éléments contenus dans la zone étudiée.
Grâce aux informations fournies par cette double acquisition, les logiciels de traitement permettent ensuite de générer des images monoénergétiques virtuelles (Virtual Monoenergetic Imaging ou VMI) par reconstruction à un niveau d’énergie différent de ceux auxquels ont été réalisées les acquisitions. Les reconstructions VMI à basse énergie améliorent le contraste des agents iodés et augmentent le rapport contraste sur bruit (CNR), contrairement au fenêtrage d’énergie, ce qui permet de réduire le volume d’agent de contraste nécessaire. À l’inverse, les reconstructions VMI à haute énergie sont utilisées pour réduire les artéfacts, notamment métalliques, optimisant ainsi la qualité de l’image. En quantifiant la composition de chaque matériau grâce à des modèles physiques ou des algorithmes de séparation spectrale, les images de décomposition matérielles permettent d’obtenir des cartes spécifiques, comme celles de la concentration en iode (cartographie de densité d’iode) qui est particulièrement utile en angiographie. Cette méthode de traitement de l’image permet également d'identifier et de soustraire les contributions de l’agent de contraste afin de simuler une image sans produit de contraste ou VNC (Virtual Non-Contrast Imaging). En remplaçant les acquisitions réalisées sans produit de contraste (non injectées ou True Non Contrast Imaging), ce mode peut limiter le nombre d'examens et donc l’exposition des patients aux rayonnements ionisants. Il est utilisé au cas par cas en fonction de la qualité d'image attendue car la qualité de reconstruction reste imprécise. Enfin, d’autres cartographies, telles que la carte de densité électronique, de suppression de Calcium ou de Z effectif sont également disponibles.
Les systèmes de scanner à double énergie (Dual-Enegy CT ou DECT) reposant sur ce principe se distinguent de la génération précédente par des variabilités au niveau de leur émetteur et/ou détecteur à RX, en fonction du dispositif on parle d’acquisition ou de détection bi-énergie, la Figure 4 permet de représenter les principales méthodes d'émission ou de détection spectrale utilisées :
Figure 4. Représentation schématique des différents systèmes à double énergie. On distingue la double émission (a, b, c) du système à double détection (d). [8]
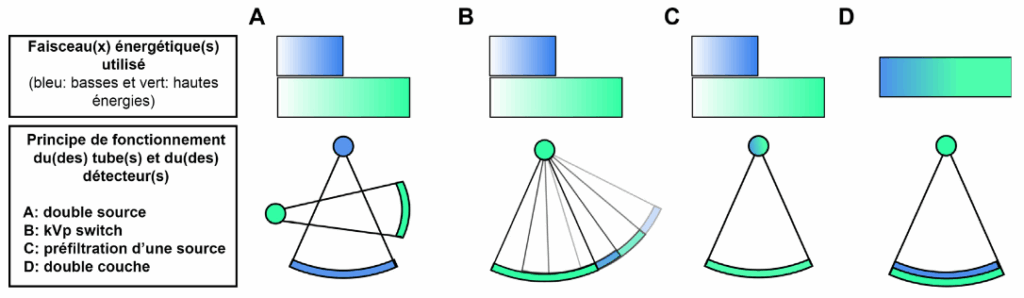
- A : Modèle DSDE simple
- B : Technologie kV Switching proposée par General Electric et Canon, visant à émettre des faisceaux de RX en alternant rapidement les deux niveaux d’énergie (80 kV et 140 kV) et de cette manière, obtenir deux atténuations quasi simultanées. Cette solution présente néanmoins l’inconvénient de décalage temporel et angulaire entre les deux mesures.
- C : Technologies Twin Beam proposée par Siemens, qui consiste à utiliser une seule source de RX et des filtres afin de diviser le faisceau en un spectre de RX de haute et basse énergie.
- D : Modèle à détection spectrale proposé par Philips (IQon Spectral CT), doté d’une double couche permettant la séparation des basses et des hautes énergies à la sortie du patient. Le tube va émettre un rayonnement à une seule énergie 100, 120 ou 140 kV et le détecteur sépare automatiquement l’énergie du faisceau grâce à ses deux couches de détection sensibles aux différentes niveaux d’énergie : les données spectrales sont toujours disponibles.
En somme, l’introduction de la TDM double énergie permet une exploitation spectrale des rayons X mais reste limitée par la sensibilité et la résolution des détecteurs à intégration d’énergie. L’échantillonnage actuel du spectre de rayons X en niveaux haut et bas d’énergie restreint les informations nécessaires à la décomposition matérielle et ne permet pas d’imagerie K-edge ou multi-contraste. Dans le cas des systèmes d’acquisition bi-énergie, l’exposition du patient à 2 faisceaux et le chevauchement des spectres ont des répercussions négatives sur la dose délivrée et la qualité des reconstructions. De même, des phénomènes de durcissement du faisceau (beam-hardening) liés à l’atténuation préférentielle des photons de faible énergie par les tissus de forte densité entraînent une dégradation de l’image (zones artificiellement claires ou sombres) et restent difficiles à corriger [8]. Cette technologie ouvre néanmoins la voie à une nouvelle génération d’appareils à comptage photonique ou Photon-Counting Detector Computed Tomography (PCD-CT), répondant à ces limitations en permettant une discrétisation spectrale encore plus précise grâce à leurs détecteurs photoniques innovants.
3. Principe et spécificités de la détection photonique
Depuis plus de deux décennies, les systèmes de tomodensitométrie à double énergie sont utilisés pour réaliser des images spectrales en distinguant les photons à faible énergie de ceux à haute énergie. Plus récemment, une nouvelle génération de détecteurs à résolution énergétique, appelés PCD (Photon Counting Detector), a fait son apparition pour remplacer les EID présents dans les systèmes de tomodensitométrie mono et double énergie conventionnels.
3.1. Choix du matériau semi-conducteur
Au contraire des détecteurs à intégration (EID), l’architecture des PCD comprend un composant semi-conducteur fonctionnant par conversion directe des photons X incidents en paires électron-trou. Les matériaux utilisés sont sélectionnés selon différents critères dont leur numéro atomique qui doit être suffisant pour assurer une bonne efficacité d’absorption des RX. Un numéro atomique Z élevé permet de privilégier des interactions photons/matière de type photoélectrique, ce qui est l’objectif recherché. On s’intéresse donc à l’épaisseur nécessaire pour stopper 90% des photons incidents en fonction de leur énergie en keV. Les travaux de recherches ont permis d’identifier plusieurs matériaux semi-conducteurs pouvant être utilisés pour le comptage photonique : le Tellure de Cadmium (CdTe) ou encore le Cadmium Zinc Telluride (CdZnTe ou CZT) sont les plus utilisés actuellement pour leur propriétés d’absorption aux niveaux d’énergies utilisés en clinique. Pour cette même raison, le Silicium (Si) pourrait constituer une alternative mais nécessite une épaisseur de couche largement supérieure à celle du CdTe pour un même pouvoir d’atténuation [18]. La Figure 5 permet de comparer différents matériaux semi-conducteur candidats :
Figure 5. Épaisseur de matériau (en mm) nécessaire pour stopper 90% des photons incidents en fonction de leur énergie (en keV) pour différentes applications : mammographie (jaune), radiographie (bleu) et scintigraphie (vert). [18]
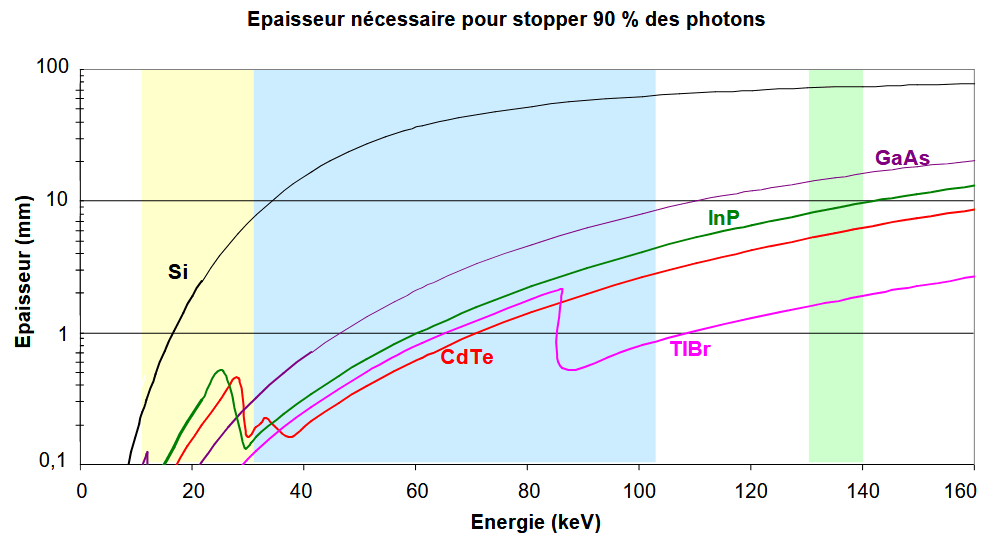
Cette notion est importante à prendre en considération car l’épaisseur du matériau entraîne certaines limites contraignantes [19] [10] :
- Il faut être capable de produire l’épaisseur nécessaire avec une bonne pureté cristalline (cristallogenèse) et la transformer (découpe, polissage, traitement de surface …)
- En fonction de l’architecture du détecteur et des propriétés de transport des charges du matériau, une trop grande épaisseur peut réduire les performances
- La bande interdite (ou Eg, énergie minimale nécessaire pour exciter un électron de la bande de valence vers la bande de conduction) doit être suffisamment élevée pour que le bruit thermique soit négligeable aux températures de fonctionnement
Le choix du matériau de détection est donc crucial avant d’aborder les phénomènes physiques associés.
3.2. De l'interaction dans le détecteur à la discrimination énergétique
Actuellement, les PCD sont généralement en structure planaire, avec les électrodes déposées sur la surface du matériau. Cette structure nécessite de faire un compromis entre l’efficacité d’absorption des photons incidents et l’efficacité de collecte des charges afin de ne pas saturer l’électronique d’acquisition [20]. L’interaction des photons X avec le matériau semi-conducteur repose sur les mêmes principes physiques que dans les détecteurs cristallins conventionnels. Le photon incident interagit par effet photoélectrique pour former une paire électron (éjecté) - trou (vacance de la couche électronique), ou par effet Compton pour former un nouveau photon diffusé et entraîner l'éjection d’un électron. La chaîne de réactions subséquente à l'interaction initiale d’un photon incident entraîne la formation d’un nuage de paires électron-trou. Les charges créées sont ensuite attirées vers les électrodes, selon une direction parallèle aux lignes du champ électrique appliqué, puis détectées sur un pixel de l’anode. L’architecture des PCD se distingue de celle des EID par l'absence de septa permise par le principe de détection directe. L’amélioration de l'efficacité géométrique de ces nouveaux détecteurs permet de réduire la quantité de rayonnement nécessaire pour recueillir un signal suffisant. La Figure 6 schématise l’ensemble de ces informations :
Figure 6. Schéma de fonctionnement d’un PCD en structure planaire. [20]
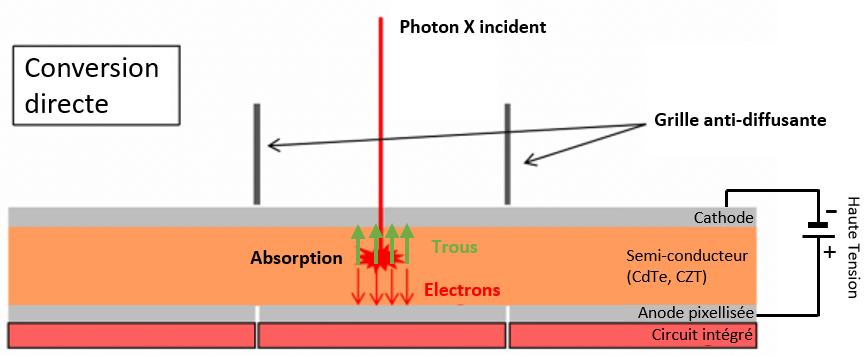
Le signal induit par l’arrivée des charges au niveau de l’anode pixellisée est mesuré et l’information spatiale conservée, contrairement aux cristaux scintillateurs où les photons de fluorescence sont émis de façon isotrope [18]. Chaque photon X engendre ainsi une impulsion ou pulse dont la hauteur dépend de son énergie. Ceci est permis par le circuit intégré (Application-Specific Integrated Circuit ou ASICs) qui est composé de canaux montés en parallèle qui vont successivement amplifier le signal, modéliser l'impulsion, comparer et classer les signaux dans les différentes fenêtres énergétiques (discrimination) comme représenté sur l’étape 4 de la Figure 7 : on parle alors de comptage photonique [21]. Le nombre de fenêtres disponibles varie selon les constructeurs et va permettre les reconstructions aux différents niveaux d'énergie.
Figure 7. 1. Production des rayons X, 2. Interactions dans le détecteur 3. Réception des signaux ou pulse et filtration selon un seuil minimum, 4. Classement des rayons X dans les différentes fenêtres énergétiques. [21], [22]
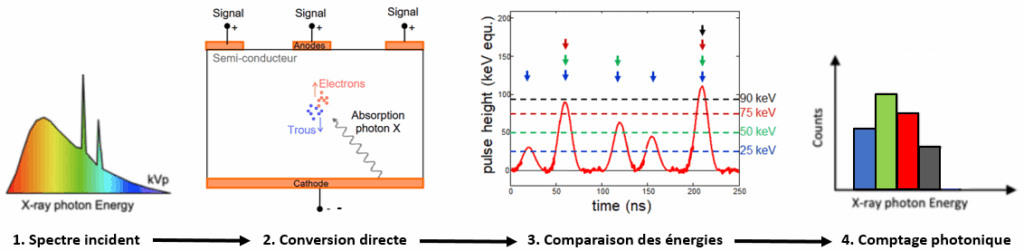
En filtrant les rayons X de faible énergie après leur détection (généralement inférieure à 20 keV), cette architecture permet une réduction significative du bruit électronique et donc un gain sur la qualité des acquisitions sans impact sur le taux de comptage. Cet avantage est particulièrement intéressant pour les études à bas keV ou sur les patients en surpoids pour lesquelles le bruit est amplifié. Le principe de fonctionnement des PCD offre donc des avantages techniques majeurs par rapport aux EID, les implications sont aussi importantes en usage clinique.
3.3. Avantages techniques du comptage photonique et conséquences cliniques attendues
En l’absence d’étape de scintillation, les détecteurs à semi-conducteur améliorent l’efficacité quantique (DQE) jusqu’ici atteignable avec ceux à intégration d’énergie, contribuant ainsi à réduire l’exposition du patient. En outre, les PCD offrent également une résolution spectrale ou énergétique intéressante aux niveaux d’énergies utilisés en scanographie, elle est d’environ 0.62 keV pour du CdTe à 100 keV [23]. Cette dernière, quantifiée par la largeur à mi‑hauteur (Full width at half maximum ou FWHM) de la réponse en énergie, reflète la capacité du détecteur à distinguer précisément l’énergie de chaque photon, ce qui permet une meilleure séparation spectrale des photons, une discrimination tissulaire accrue et une amélioration du contraste et de la quantification des matériaux par rapport aux détecteurs à intégration d’énergie. Ceci est permis par la faible énergie d’ionisation (bande interdite) des semi-conducteurs qui conditionne l’énergie moyenne nécessaire pour qu’une particule crée une paire électron-trou.
De même, la résolution spatiale est fortement améliorée par la conversion directe des photons X qui permet d’atteindre des dimensions de pixels à l’isocentre (qualité d’image optimale) variant entre 0,5 × 0,5 et 0,1 × 0,1 mm² en fonction des modèles. Les résolutions spatiales théoriques associées correspondent à 0.28 x 0.28 mm² et 70 x 70 µm respectivement. En pratique, les modèles PCD actuels atteignent une résolution planaire d’environ 0.3 mm en routine clinique avec une épaisseur de coupe de 0.4 mm (résolution standard) et jusqu'à 0.125 mm en Ultra-Haute-Résolution avec une épaisseur de coupe de 0.2 mm contre 0.5 mm de résolution planaire et d’épaisseur de coupe pour les meilleurs EID [24].
Le principe de décomposition spectrale permet également une imagerie multi-contraste ou K-edge, se définissant comme une imagerie spécifique et quantitative différenciant deux (bi-couleur) ou plusieurs agents (multicolore) de contraste au sein d'un même tissu et même voxel. L'interaction de K-électrons avec des photons X incidents par effet photoélectrique au sein des tissus entraîne une forte atténuation du spectre aux niveaux d’énergie K-edge. C’est cette forte discontinuité, détectable grâce à l’échantillonnage spectral des PCD, qui permet d’identifier un agent de contraste spécifique des autres composants participant à l'atténuation globale des RX. De la même façon, des pics d’atténuation correspondants aux couches L, M sont présents mais à des énergies beaucoup plus basses et qui ne permettent pas une discrimination optimale en imagerie clinique.
Ainsi des atomes à K-edge élevé, comme le Gadolinium, l'Or, l'Ytterbium, le Platinum pourront être étudiés en vue d’être utilisés comme agents de contraste. En effet, les nanoparticules d'Or (AuNP) s'avèrent particulièrement intéressantes en raison de leurs demi-vies plus longues que celles des agents de contraste iodés [10], offrant une meilleure imagerie du compartiment vasculaire et une biocompatibilité pour des applications in vivo. Son association à des molécules spécifiques d’un processus pathologique pourrait donc permettre de réaliser une imagerie moléculaire sans avoir recours aux radiotraceurs de la TEP (Tomographie par Émission de Positons). On note que l'iode présente une énergie K-edge trop basse (33.3 keV) pour être observable en usage clinique contrairement aux systèmes dédiés pour le petit animal ou pour la mammographie [25]. La Figure 8 ci-dessous permet de mettre en évidence l’imagerie spécifique multi-contraste ou K-edge permise par la technologie à comptage photonique et son intérêt pour une étude quantitative :
Figure 8. Reconstruction multi-contraste basée sur des algorithmes de décomposition matérielle à partir d’un fantôme spécifique. Le scanner à comptage photonique permet d’identifier plusieurs matériaux de contraste : Or (Gold), Iode (Iodine), Gadolinium, et organiques : Lipides (Lipid), Eau (Water), et Calcium, en s’appuyant sur leurs réponses d’atténuation distinctes dépendantes de l’énergie des photons X. [26]
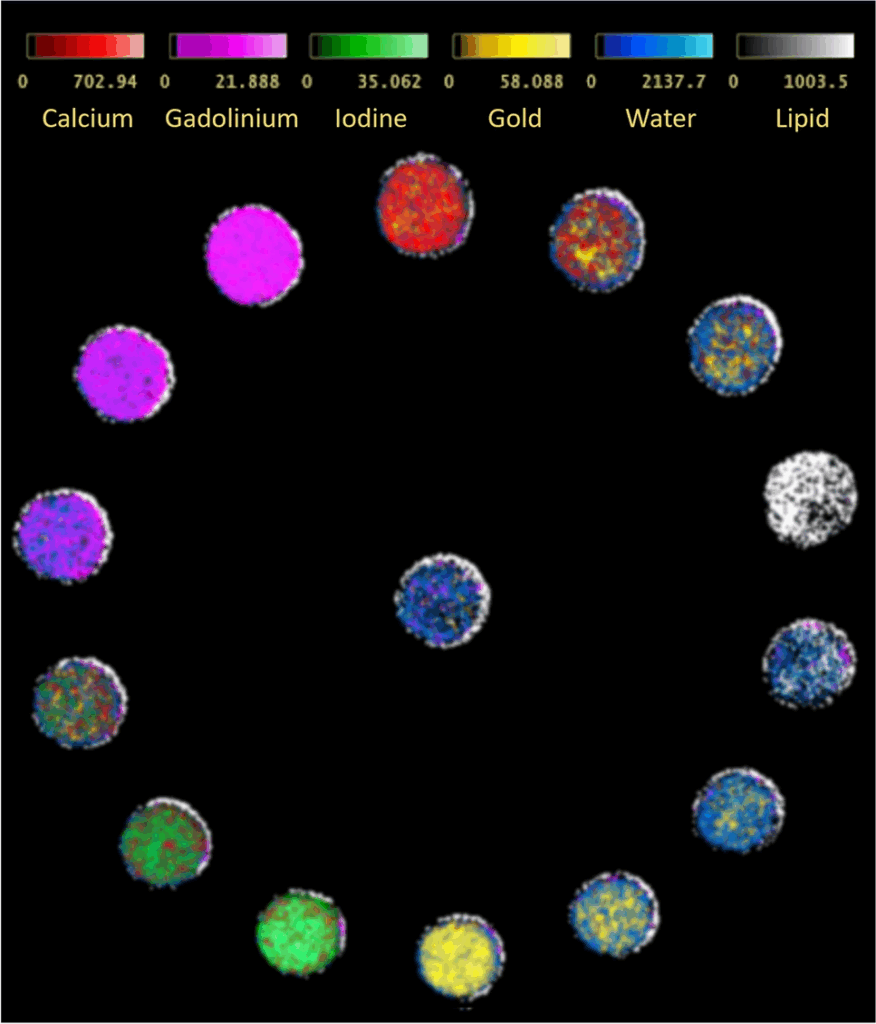
Grâce à leur sensibilité spectrale intrinsèque, les détecteurs à comptage photonique ne nécessitent pas d’architecture bi-tube ou d’acquisition/détection à 2 niveaux d'énergie différents pour étudier les variations d’atténuation. Ils permettent ainsi de produire des cartographies de distribution quantitative, particulièrement utiles pour les reconstructions VMI, en estimant plus précisément la concentration des composés dans chaque voxel. On parle d'images densitométriques représentant par exemple la quantité de milligrammes d'iode par millilitre de sang. La disponibilité de l’ensemble des informations spectrales pour chaque examen est également intéressante pour le suivi des patients. En scanographie, les acquisitions ne peuvent être comparées qu’à des niveaux d’énergie (keV) équivalents. La reconstruction sur l’ensemble du spectre permet de respecter cette condition et diminue le nombre d’examens complémentaires.
En améliorant la pondération des photons de basse énergie et en supprimant le bruit électronique, le PCD-CT se rapproche du niveau de contraste de l’IRM et améliore significativement plusieurs caractéristiques majeures des dispositifs conventionnels tout en permettant de nouvelles techniques d’imagerie. De même, l’optimisation des reconstructions, et particulièrement à bas keV qui sont intéressantes pour leur contraste, et la réduction subconséquente des volumes de produits de contraste injectés contribuent au renforcement de la position du scanner en Imagerie Médicale. Les apports techniques de cette innovation ouvrent donc la voie vers une amélioration des applications cliniques actuelles dans un premier temps, et la possibilité de leur extension par la suite.
II. Apports et applications cliniques du scanner à comptage photonique
Suite à l’étude des fonctionnalités attendues et des principes physiques sous-jacents, cette partie s’intéresse davantage aux apports cliniques des nouveaux scanners photoniques. Bien que l'IRM soit actuellement la modalité privilégiée pour l'évaluation des tissus mous et de la moelle osseuse, le scanner excelle dans l'imagerie des structures à contraste élevé, telles que les tissus minéralisés. En imagerie musculo-squelettique par exemple, le scanner est utilisé dans un large éventail d'indications, seul ou en association avec l'IRM. Les exemples cliniques proposés cherchent donc à déterminer si les apports de cette nouvelle technologie vont modifier les équilibres existants et imposer le scanner comme l’imagerie diagnostique de référence pour davantage d’indications.
1. Comparaison avec les autres modalités d’imagerie
En exploitant des détecteurs capables de compter individuellement chaque photon incident et d’en mesurer l’énergie, cette nouvelle génération se distingue des scanners conventionnels à intégration d’énergie utilisés en pratique clinique depuis plusieurs décennies. Il est possible d’analyser la place du scanner à comptage de photons dans le paysage des modalités d’imagerie médicale, en comparant ses performances en termes de résolution spatiale, temporelle et spectrale, de rapport signal sur bruit, de contraste, de dose délivrée et d’indications cliniques, avec celles des générations précédentes mais également avec l’autre principale modalité d’imagerie anatomique en coupe : l’IRM.
1.1. Une amélioration de la résolution spatiale
Le scanner à comptage photonique présente une résolution spatiale significativement supérieure à celle des générations précédentes. En effet, la réduction de la dimension des unités de détection (pixels de l’anode) augmente le niveau de détails observables à l’image qui passe d’environ 0.5mm pour les EID à 0.2mm pour les PCD en haute résolution. Les images de la Figure 9, qui ont été acquises avec ces deux niveaux de résolution permettent de se rendre compte du gain de précision.
Figure 9. Comparaison d’une acquisition avec un scanner à intégration d’énergie Somatom Force de 3ème génération EID-CT (Siemens Healthineers) et à comptage photonique Naeotom Alpha PCD-CT (Siemens Healthineers) pour l’angiographie des membres inférieurs avec un indice de dose volumique ou CTDIvol (Computed Tomography Dose Index volume) et un protocole de produit de contraste équivalents. Le CTDIvol est un indice dosimétrique utilisé en tomodensitométrie pour estimer la dose moyenne délivrée (mGy) dans le volume irradié lors d’un examen. Bv ou Body vascular : matrice de reconstruction (kernel) vasculaire. [27]
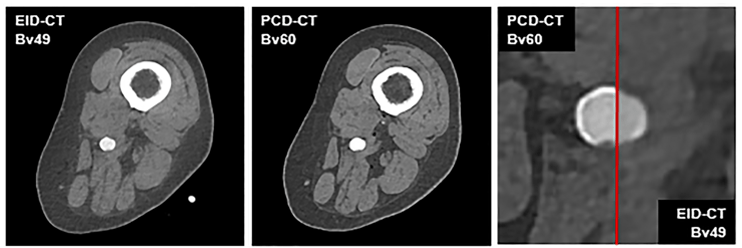
Grâce à la haute résolution du PCD-CT, il devient possible d’explorer des zones difficilement accessibles par d’autres modalités. C'est le cas par exemple pour l'exploration du rocher, une structure osseuse située dans l'oreille interne pour laquelle cette technologie apporte un gain significatif pour la visualisation des structures fines. En comparaison, l’IRM offre une résolution spatiale variable selon la séquence et le champ magnétique, généralement inférieure pour les structures denses ou osseuses [28]. L’échographie peut atteindre une très haute résolution spatiale pouvant aller jusqu'à 0.05 mm avec des sondes haute-fréquence (autour de 20 MHz), mais uniquement pour une exploration très superficielle [24]. La résolution spatiale en échographie reste fortement limitée par l’os et les milieux gazeux (poumons par exemple).
Du côté de la résolution temporelle, celle du scanner à comptage photonique bi-tube est de 66 ms ce qui est moins intéressant que celle de l'IRM cardiaque notamment : entre 30 et 50 ms en ciné IRM permettant d'annuler la prise de bêta bloquant [24], et largement supérieure à la résolution temporelle de l'échographe qui permet d'acquérir des images en temps réel. En scanographie, la résolution temporelle étant dépendante de la vitesse de rotation du système tube-détecteur qui est par définition limitée, le PCD-CT bénéficie des avancées réalisées sur la réduction des temps d’acquisitions sans permettre de les réduire davantage. Les problématiques liées aux explorations des structures anatomiques cardiaques ne sont donc pas résolues malgré l’existence de mécanismes de compensation tels que le prospectif ou gating respiratoire (acquisition synchronisée avec le mouvement respiratoire). Ainsi, même le mode d’acquisition ultra-rapide (Flash) ne permet pas d'annuler la prise de bêta-bloquant. Cependant, la durée des acquisitions, environ 3 à 4s pour un examen thoraco-abdomino-pelvien (TAP), reste largement inférieure à celle de l’IRM (plusieurs minutes).
1.2. Une meilleure caractérisation tissulaire
Le scanner à comptage photonique permet également d’améliorer le contraste et de réduire certains types de bruits notamment liés à la diffusion interne des scintillateurs. Cette amélioration, associée à une meilleure exploitation des photons de basse énergie, contribue à l’augmentation du rapport signal/bruit comme présenté Figure 10 :
Figure 10. Reconstructions coronales curvilignes en scanners conventionnels (à gauche), et à comptage photonique (à droite) montrant une réduction du bruit ainsi qu’une meilleure résolution en contraste pour la détection d’une tumeur endocrine pancréatique isthmique (têtes de flèche) et la meilleure visualisation du canal pancréatique principal (flèches). [25]
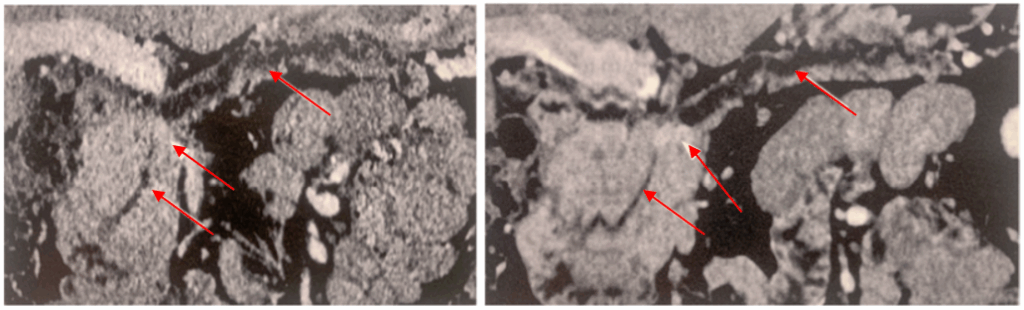
Aussi, l’intérêt majeur de cette nouvelle technologie réside dans sa capacité spectrale qui permet une distinction plus fine des matériaux, par exemple pour la séparation iode/calcium, la caractérisation des plaques athéroscléreuses, la discrimination des métaux ou les reconstructions virtuelles selon différents niveaux d'énergie. L’IRM conserve toutefois un avantage pour la caractérisation des tissus mous grâce à la diversité de ses contrastes. Le comptage photonique se positionne donc comme une modalité complémentaire, particulièrement prometteuse en imagerie cardiovasculaire et ostéo-articulaire. La réduction de la dose délivrée permise par le principe de détection ouvre la voie vers une extension des indications en 1er recours du scanner.
1.3. Une réduction significative des rayonnements ionisants
Enfin, l'un des grands apports des scanners à comptage photonique par rapport aux scanners conventionnels, c'est la réduction de la dose de rayons X délivrée aux patients, en maintenant, voire en améliorant, la qualité de l’image (Figure 11). Plusieurs études ont démontré la pertinence d'une diminution de dose pouvant aller jusqu’à 80% de rayonnements en moins sans réel compromis sur le rendu des images. Un radiologue pédiatrique de l'hôpital Necker-Enfants Malades a ainsi expliqué lors d'une conférence donnée dans le cadre des Journées Francophones de Radiologie 2025, que la diminution de la dose de rayonnements ionisants peut aller jusqu'à 80% pour certains organes explorés chez l'enfant lorsque l'acquisition est réalisée en mode "Flash", qui permet notamment une exploration TAP en 0.5 s avec un système bi-tube. Il convient toutefois de noter que certains protocoles peuvent maintenir une dose comparable à celle du scanner conventionnel.
Figure 11. Images acquises dans le cadre d’un suivi de séquelles de virose avec une diminution par quatre de la dose d’irradiation passant de 0,43 mGy (à gauche) à 0,09 mGy (à droite) sans compromis sur la qualité de l’image. [25]
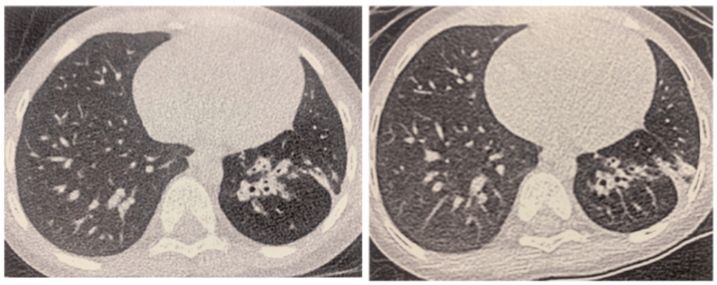
Avec le scanner à comptage photonique, les praticiens peuvent désormais décider de conserver une exposition du patient équivalente à celle des générations précédentes pour améliorer la qualité de l’image ou réduire la dose délivrée tout en conservant une qualité des acquisitions comparables au scanner conventionnel. Cet avantage est particulièrement intéressant pour améliorer la prise en charge de patients ayant une forte corpulence en réduisant significativement la dose nécessaire [20]. Enfin, les reconstructions tridimensionnelles, les VMI, les VNC, et les décompositions matérielles sont également améliorées et possibles en routine clinique grâce à l’énergie multi-spectrale.
1.4. Réduction du volume de produit de contraste
Le scanner à comptage de photons (PCD-CT) permet de reconstruire des images mono énergétiques à très bas keV (≈40–60 keV). À ces énergies, l’atténuation de l’iode est maximale, ce qui augmente le contraste iodé sans augmenter la dose de rayonnement ni le kV d’acquisition.
Chez les patients corpulents, l’acquisition doit en pratique se faire à 120 kV afin d’assurer la pénétration du faisceau. Cependant, la reconstruction à 60 keV permet d’obtenir un rehaussement équivalent à celui d’un scanner classique à 90 kV. Cette indépendance acquisition/reconstruction permet une réduction significative du volume de PDC injecté. De plus, depuis 2024, le Projet de Loi de Financement de la Sécurité Sociale (PLFSS) impose aux établissements ou cabinets d’imagerie de fournir et tracer la quantité de PDC administrée, tandis qu’auparavant c’était le patient qui se le procurait en pharmacie sur ordonnance. Un intérêt tout particulier est donc apporté à l’évaluation personnalisée de la quantité de produit de contraste à injecter. Un calculateur local a été mis en place au CHU de Bordeaux pour optimiser la quantité de produit de contraste idéale selon le gabarit du patient. Des diminutions pouvant atteindre 40% nous ont été rapportées sur certains protocoles, en particulier chez les patients corpulents. La Figure 12 issue d’une reconstruction volumique illustre ce gain :
Figure 12. Reconstructions tridimensionnelles d’un angioscanner des membres inférieurs avec détecteurs à intégration d'énergie (EID) et 145 ml de produit de contraste iodé en A, et à détection de photons avec seulement 55 ml du même produit de contraste iodé en B. En améliorant la détection du signal de l’iode, le PCD-CT réduit le volume nécessaire à injecter. [32]
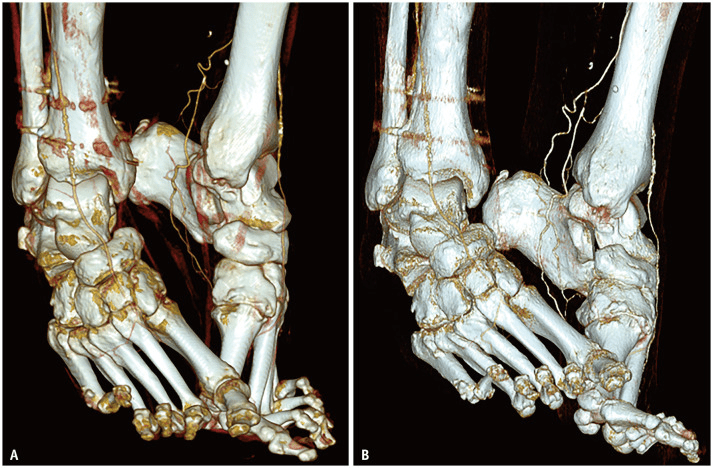
La limitation de l’utilisation du produit de contraste représente un intérêt pour chaque patient mais une attention sera toute particulière pour les patients ayant déjà perdu une partie de leur capacité rénale. Une thèse interne au CHU de Bordeaux est en cours et a montré que les volumes de PDC injectés avec le PCD-CT restaient suffisamment faibles pour préserver la fonction rénale résiduelle chez des patients insuffisants rénaux. Dans plusieurs cas, l’examen a pu être réalisé alors qu’il aurait été contre-indiqué avec un scanner conventionnel. En revanche, en mode haute résolution, utilisé pour visualiser de très petits vaisseaux ou structures fines, le besoin en signal augmente. Dans ces cas, la réduction de PDC peut être limitée, voire annulée, afin de maintenir un rehaussement vasculaire suffisant. Finalement, les apports cliniques du scanner à comptage photonique offrent de nouvelles perspectives puisque de nombreuses études démontrent que son utilisation pour l'évaluation de la stéatose hépatique métabolique, exclusivement réservée à l’IRM actuellement, pourrait être envisageable à l’avenir.
2. Applications cliniques actuelles et à venir
Les bénéfices du PCD-CT sont susceptibles de transformer l’approche diagnostique dans des contextes cliniques variés. En effet, l’ensemble des experts avec lesquels nous avons pu échanger dans le cadre de ce projet (radiologues, radiophysiciens et ingénieurs d’applications) s'accordent à dire que le scanner à comptage photonique surpasse le scanner conventionnel sur l’ensemble des applications cliniques et vient concurrencer d’autres modalités sur certaines indications.
2.1. Applications en radio-pédiatrie
La pédiatrie constitue l’un des secteurs où le scanner à comptage photonique présente le plus grand potentiel d’impact clinique. En radiopédiatrie, la question de la dose est centrale, car les rayons sont plus délétères pour les enfants que pour les adultes et induisent un risque supérieur de provoquer des cancers radio-induits. C'est pourquoi l'IRM ou l'échographie sont toujours privilégiés lorsque cela est possible. Mais dans certains cas, le scanner reste incontournable comme pour les jeunes patients atteints de tumeurs osseuses avec des métastases diagnostiquées ou à risque métastasique. C'est pourquoi l'Institut Gustave Roussy, centre de référence dans le traitement du cancer qui est équipé de deux scanners dont un à comptage photonique, utilise systématiquement ce dernier pour l'examen des enfants afin de profiter de la diminution des rayonnements ionisants qu'il permet. Les manipulateurs radio que nous avons rencontrés nous ont indiqué avoir observé des réductions de dose allant jusqu'à 70% sur certains examens sans que cette réduction ne se fasse au détriment de la qualité des images qui est même parfois meilleure. Cette diminution des doses est d'autant plus importante que certains cancers pédiatriques peuvent nécessiter entre 12 et 20 scanners thoraciques [25] durant les cinq premières années de la prise en charge.
Du côté de l'imagerie interventionnelle pédiatrique, l'échographe est majoritairement privilégié, mais pour certaines interventions le scanner est irremplaçable, notamment pour les poumons et les os qui ne sont pas accessibles en échographie. Dans ces cas, combiné aux systèmes de contrôle automatique de l'exposition (Automatic Exposure Control ou AEC) qui permettent, à l’aide du scout-view (radio de positionnement) de moduler le courant en temps réel en fonction de la zone anatomique et de l’indication (compromis dose/bruit), le scanner à comptage photonique présente un avantage indéniable pour les enfants qui sont ainsi moins exposés.
Outre la réduction des doses de rayons X, le comptage photonique ouvre de nouvelles perspectives grâce à sa grande précision. C'est le cas par exemple pour la détection du cholestéatome (accumulation anormale de cellules de peau derrière le tympan pouvant détruire progressivement les structures osseuses de l’oreille). Cette anomalie peut toucher aussi bien l’enfant que l’adulte, mais il est souvent plus agressif chez la population pédiatrique, ce qui explique l’attention particulière qu’il nécessite. Le stéatome étant très difficile à distinguer, l'examen est presque systématiquement réalisé en IRM, et très rarement en scanner. Mais d'après le témoignage du docteur Kahina Belhous de l'hôpital Necker-Enfant Malades [25], le scanner à comptage photonique pourrait être utilisé pour caractériser les propriétés spectrales de cette tumeur en utilisant une décomposition en 3 matériaux.
2.2. Un bénéfice indéniable dans la prise en charge en cancérologie digestive
L'intérêt du scanner à comptage photonique se manifeste de façon nette en oncologie digestive et particulièrement dans les cancers du pancréas et des voies biliaires, où toutes les décisions thérapeutiques reposent presque exclusivement sur l'analyse des données de l'imagerie. Cette technologie permettant une amélioration de la qualité d'image, la délimitation des lésions tumorales est plus fine, tout comme l'évaluation de leur expansion (Figure 13). Ainsi il devient plus facile de définir les rapports de la tumeur avec des structures vasculaires voisines et donc à orienter la stratégie de prise en charge.
Figure 13. Images mettant en évidence un adénocarcinome du pancréas, acquises avec un scanner conventionnel (à gauche) et un scanner à comptage photonique (à droite) mettant en valeur une meilleure délimitation de la tumeur (flèches) et un meilleur contraste entre la tumeur et les tissus sains.[29]
Étant donné que le scanner à comptage de photon n'est pas encore très implanté, il est important de sélectionner les indications en privilégiant les situations cliniques où la finesse diagnostique influence réellement la décision thérapeutique. Et le bilan dans les cancers du pancréas en est un bon exemple.
2.3. Applications cardiovasculaires
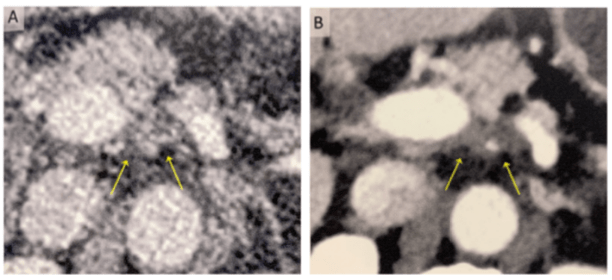
En cardiologie, le scanner à comptage photonique occupe une place grandissante pour l’analyse des artères coronaires dans les cardiopathies. Bien qu’il améliore nettement la qualité diagnostique par rapport aux scanners conventionnels, il ne va pas entièrement remplacer la coronarographie. Celle-ci reste l’examen de référence pour les phases aigües car elle permet de traiter les lésions simultanément. Cependant, dans les situations où seul un avis diagnostique est nécessaire, le scanner à comptage photonique constitue une véritable alternative. Sa résolution spatiale accrue et son rapport signal/bruit amélioré permettent de réduire significativement le recours à une coronarographie purement diagnostique, examen plus invasif et à risque pour le patient. Grâce à l’analyse spectrale et à la réduction des artéfacts, l’étude des calcifications complexes et des petits stents coronaires, jusque-là réservée à la coronarographie, est rendue possible. Le PCD-CT répond donc aux limitations des scanners précédents et permet d’étendre le recours à cette modalité pour l’évaluation des sténoses. En effet, l’accès simultané à plusieurs niveaux d’énergie facilite l’étude de la lumière coronaire et la caractérisation des plaques d’athérome en distinguant plus précisément les composants calciques, fibrineux ou lipidiques. Cela permet une estimation plus fiable du degré de sténose, notamment dans les segments où le calcium entraînait autrefois des artefacts qui limitent l’interprétation. Cette caractérisation permet de mieux discriminer les plaques vulnérables et à risque de se rompre, de celles qui ne sont pas dangereuses, réduisant ainsi le recours systématique à une intervention invasive lorsque celle-ci n’apporte pas d’avantage thérapeutique immédiat [33].
Plusieurs études démontrent que le score CAD-RADS (Coronary Artery Disease – Reporting and Data System) lié au degré de sténose des coronaires est souvent reclassifié à un niveau plus bas que celui établit avec un scanner conventionnel. La Figure 14 permet de mettre en évidence cette observation avec plusieurs comparaisons entre un scanner à comptage photonique et spectral à intégration d’énergie. La précision des acquisitions réduit le nombre de segments coronariens exclus et offre une meilleure caractérisation des dépôts athéromateux calcifiés. Ceci est permis par la réduction des artéfacts de blooming calciques, liés à la saturation du signal des détecteurs conventionnels, et à l’amélioration de la résolution spatiale. La décision thérapeutique associée au diagnostic pouvant fortement varier selon le score CAD-RADS, cette reclassification offre au patient un traitement plus adapté à sa pathologie tout en optimisant les dépenses de santé associées [34].
Figure 14. Exemples d’examens de sténoses coronariennes en reconstruction multiplanaire curviligne et en coupe transversale ayant conduit à une reclassification à la baisse du score CAD-RADS du patient. Les acquisitions EID-CT et PCD-CT ont été réalisées avec une dose et un protocole de produit de contraste équivalents. [35]
III. Aspects médico-économiques, réglementaires et d’intégration hospitalière
L’évaluation de la place du scanner à comptage photonique impose de prendre en considération les aspects médico-économiques associés. Compte tenu de la complexité technologique de cette innovation, des bénéfices apportés pour les praticiens au service des patients et du monopole actuel d’un constructeur en usage clinique, le montant d’achat est significativement plus élevé que pour un modèle conventionnel mono-énergie (3 à 5 fois plus élevé) ou spectral double-energie (2 à 3 fois plus élevé). En France, le forfait technique permet d’amortir le coût des équipements d’imagerie lourde (scanner, IRM) sur une durée réglementaire de 7 ans (puis dégressif par palier). Un tel investissement doit donc être justifié par une activité suffisante. Plusieurs études comparatives entre un scanner conventionnel et à comptage photonique concluent néanmoins d’un avantage de ce dernier sur l’impact économique global sur le système de santé par une réduction du nombre d'examens complémentaires grâce à sa précision diagnostique [24] [30]. L’évolution du financement des soins et des obligations réglementaires pourraient avoir un impact majeur sur le développement de cette technologie.
1. Cadre réglementaire actuel en radiologie
L’installation d’un scanner photonique, comme tout équipement de tomodensitométrie, est strictement encadrée par la réglementation radiologique française. Selon le Code de la Santé Publique et sous la supervision de l’Autorité de Sûreté Nucléaire (ASN), tout appareil utilisant des rayons X à des fins médicales doit être déclaré et faire l’objet d’une autorisation préalable. Cette réglementation impose également la réalisation de contrôles qualité avant mise en service, des vérifications périodiques par des physiciens médicaux, et la conformité aux doses maximales de rayonnement délivrées aux patients. Le personnel manipulateur et les radiologues doivent suivre des formations certifiées pour garantir la sécurité des patients et la maîtrise de l’appareil. En diminuant les niveaux de dose délivrés, le PCD-CT pourrait, à long terme, entraîner une révision des Niveaux de Référence Diagnostique (NRD) qui correspondent aux recommandations de doses en fonction des modalités d’imagerie, des indications cliniques et du patient. En effet, selon la décision de l’Autorité de sûreté nucléaire (ASN) n° 2019-DC-0667 du 18 avril 2019, les responsables des services de radiologie et de médecine nucléaire doivent procéder à des évaluations dosimétriques périodiques et transmettre les résultats à l'IRSN (L'Institut de Radioprotection et de Sûreté Nucléaire). Enfin, de prochains travaux du Comité Interdisciplinaire de Recherche et de Travail sur les Agents de Contraste en Imagerie (CIRTACI piloté par la Société française de radiologie ou SFR) devraient également permettre de confirmer les réductions de volume de produit de contraste sur plusieurs indications. [36].
En parallèle, le scanner photonique doit respecter les normes techniques et de sécurité des équipements médicaux. Tout appareil doit être marqué CE conformément au Règlement Européen sur les Dispositifs Médicaux (MDR 2017/745), garantissant la sécurité électrique, mécanique et radiologique. Les normes internationales IEC 60601-1 et IEC 60601-2-44 (scanner) définissent les exigences pour la conception, la performance et la protection contre les risques électriques et radiologiques. L’installation physique doit également respecter les critères de blindage des locaux, d’alimentation électrique, de climatisation et de ventilation, tandis que le traitement et le stockage des images doivent être conformes aux standards et aux règles de protection des données personnelles (RGPD) et de grade médical [37].
En France, la prise en charge des actes de tomodensitométrie repose sur la nomenclature CCAM (Classification Commune des Actes Médicaux) et les règles de remboursement de l’Assurance Maladie ; tant que l’acte prescrit est médicalement justifié et correctement codé, il est remboursé indépendamment de la gamme du modèle d’équipement ayant été utilisé. Cette logique axée exclusivement sur l’acte pose problème pour les technologies innovantes et coûteuses, dont fait partie le PCD-CT, car le tarif de remboursement du forfait technique de l’acte ne prend pas en compte le surcoût d’acquisition de cet équipement ni le gain diagnostique offert. Cela peut ainsi dissuader les établissements d’investir malgré les bénéfices potentiels pour les patients. Par ailleurs, l’évaluation réglementaire et technique de nouvelles modalités (contrôles qualité, mesures de dose, validation clinique) relève d’organismes comme l’ANSM (Agence nationale de sécurité du médicament et des produits de santé) ou l’ASN, et nécessite du temps et des ressources, retardant l’émergence d’un cadre spécifique de valorisation économique. Finalement, les mesures réglementaires et légales encadrant l’acquisition et l’exploitation d’une telle modalité doivent être compatibles avec la maîtrise des coûts en incluant notamment les aspects liés à la gestion des données de Santé produites.
2. Logistique d’installation et d’utilisation du PCD-CT
Bien que novateur, le scanner à comptage photonique présente plusieurs contraintes d’intégration liées à ses détecteurs. Une de leur particularité est leur sensibilité accrue aux variations de température. Ils nécessitent d’être refroidis de manière continue par une panoplie à eau glacée. Ainsi, l’installation d’un tel dispositif peut impliquer la mise en place d’une boucle dédiée, l’acquisition d’équipements de production d’eau glacée ou l’adaptation d’une infrastructure existante. Dans le cas de l’Institut Gustave Roussy, la salle destinée au scanner disposait d’un volume suffisant pour intégrer un échangeur d’eau glacée, ce qui a permis de limiter l’ampleur des travaux d’adaptation.
Ces derniers requièrent également une alimentation électrique stable et continue, y compris hors-fonctionnement. En cas de coupure de courant, même de très courte durée, un recalibrage complet de l’appareil est nécessaire avant toute nouvelle utilisation. La durée de cette procédure varie généralement selon celle de l’interruption et est susceptible d'entraîner une reprogrammation des examens. Cette contrainte, qu’on ne retrouve pas sur les générations précédentes, peut avoir des répercussions importantes sur l’organisation des soins. Elle pourrait être particulièrement problématique dans les établissements ne disposant que d’un seul scanner à comptage photonique où l’absence d’alternative rend difficile la prise en charge des patients urgents. Cette re-calibration en cas de coupure de courant pourrait aussi être une contrainte lorsque le scanner est mobilisé dans le cadre d’actes d’imagerie interventionnelle où la stabilité de l’équipement est essentielle.
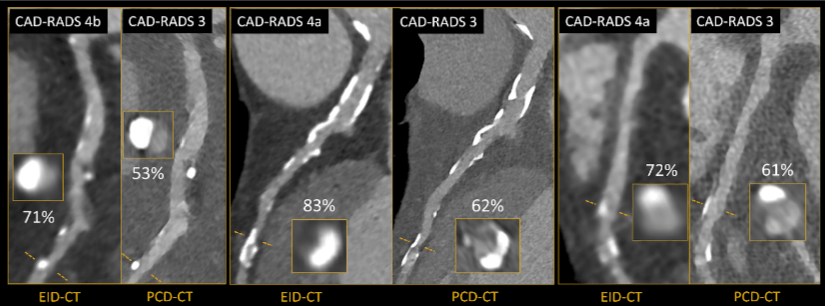
La mise en œuvre du scanner à comptage de photons modifie également la gestion de la donnée médicale au sein du flux de travail radiologique. Deux aspects majeurs sont à considérer : le volume des données générées et la complexité de leur reconstruction. Premièrement, la quantité de données produites par ce type de scanner est considérablement accrue. Sur un scanner conventionnel, une série DICOM (Digital imaging and communications in medicine) d’une centaines de coupes de 0,6 mm avec une matrice image de 512×512 représente environ 0,5 Mo. En comparaison, les modèles récents de scanner, incluant ceux à comptage de photons, génèrent des images avec une matrice de 1024×1024, multipliant par quatre le volume d’information. De plus, la finesse des coupes du PCD-CT (0,2 mm contre 0,6 mm pour EID-CT) triple encore le nombre d’images, portant la taille minimale d’une série à près de 600 Mo et jusqu’à 10 Go pour un examen TAP en UHR. À titre indicatif, les examens d’IRM sont également de l’ordre du Go. Cette hausse du volume de données améliore nettement la qualité d’image, mais impose des contraintes techniques, voire financières, notamment sur la capacité de stockage et la performance des stations de relecture. Elle pourrait contraindre les établissements à limiter l’usage de l’UHR et s’orienter vers la résolution standard en routine clinique. Bien que cela n'annulent pas l’accès à l’imagerie spectrale notamment, l’intérêt de se doter d’un tel équipement sans possibilité d’exploiter l’ensemble de ses fonctionnalités semble réduit. En fonction du modèle de facturation du stockage des données, par patient ou au volume d’images, l’impact financier pourrait être différent. Cette contrainte impose également une montée en puissance des stations de reconstruction, notamment par l’augmentation de la mémoire vive de 16 à 32 Go si l’on souhaite s’affranchir de certaines lenteurs à la visualisation des images.
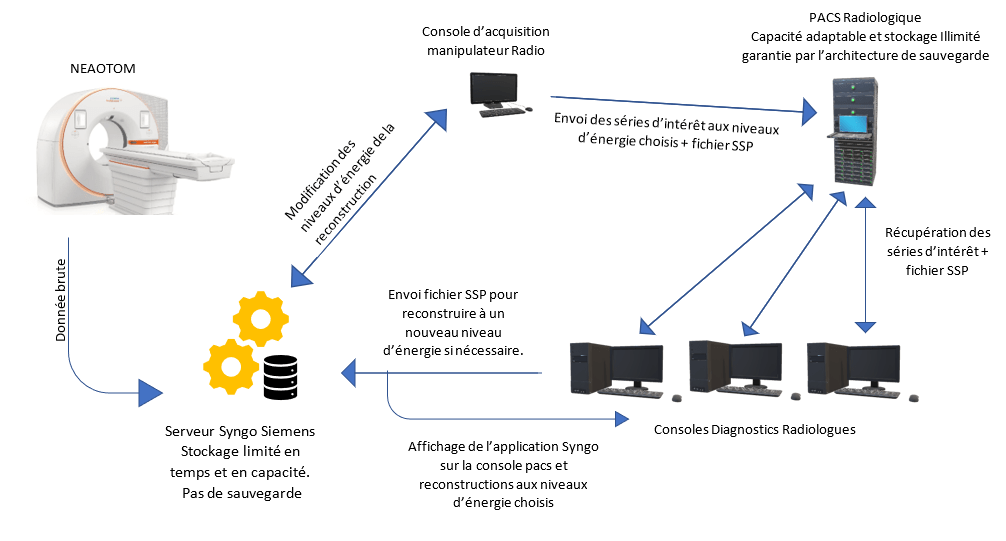
Deuxièmement, la reconstruction multi-énergie propre au scanner à comptage de photons engendre une complexité supplémentaire. Pour une même acquisition, il est possible de réaliser de nombreuses reconstructions simulant différents niveaux d’énergie (de 40 à 190 keV). Il est évidemment impossible de stocker l’ensemble de ces séries, de 600 Mo chacune, sur le PACS. Afin de préserver la souplesse diagnostique sans saturer le stockage, les établissements ont mis en place une solution hybride : seules quelques séries clés et un fichier SPP (Spectral Post Processing) contenant les informations d’énergie basse et haute sont archivés sur le PACS. Les reconstructions spécifiques peuvent ensuite être calculées de nouveau sur le serveur Syngo (Siemens), qui conserve temporairement les données complètes pendant une semaine. Cette approche garantit la disponibilité de l’information tout en maîtrisant le volume de stockage. Cependant, elle nécessite de se reconnecter depuis les consoles PACS au serveur Syngo pour effectuer ces reconstructions, entraînant une perte de temps. Des besoins supplémentaires en ressources humaines pour le paramétrage applicatif, la gestion réseau et la maintenance de l’infrastructure sont ainsi nécessaires. La synoptique de gestion des données est disponible en Figure 15 et peut varier en fonction des établissements :
Figure 15. Synoptique de transmission type de la donnée d’imagerie médicale dans le cas du Naeotom Alpha. Source : Auteur.e.s
Il est donc possible d’établir plusieurs défis liés au scanner photonique vis à vis du PACS :
- Volume de données largement supérieurs à ceux du scanner spectral conventionnel : double ou triple la quantité de données sur un même protocole
- Protocole propre PCD-CT peut générer jusqu’à +10000 images (UHR+SPP) en plus des données brutes (Raw Data) qui peuvent atteindre jusqu’à 30 Go (recherche scientifique)
- Les transferts d’images volumineuses et les tags DICOM récents imposent une infrastructure réseau et un PACS compatible pour les afficher [33].
La durée de conservation légale des clichés sur 20 ans pour les établissements de santé (hôpitaux et cliniques), incluant une disponibilité immédiate durant 3 ans, complique davantage cette situation liée au manque de capacité de stockage et d’infrastructure permettant le traitement et le transfert des données. Occupant parfois près de la moitié de la capacité de stockage disponible sur le PACS, les scanners sont particulièrement affectés par la massification des données d’acquisition du fait de la quantité d’images produites. Cette tendance s’opère en contrepartie de l’amélioration diagnostique de cette modalité. Le dimensionnement des infrastructures de transfert et de stockage des données doit donc être anticipé lors de l’acquisition de ces nouveaux équipements de pointe. En évitant le téléchargement des acquisitions sur les clients lourds pour leur visualisation, le zero footprint (streaming sur client léger) représente une alternative intéressante pour éviter les transferts de fichiers et l’upgrade onéreuse des stations de visualisations.
3. État des lieux du marché du photonique
Les détecteurs à comptage photonique représentant un tournant significatif en imagerie médicale, les principaux producteurs de scanner mènent des travaux de recherche pour développer cette technologie et profiter d’un avantage concurrentiel. De nombreux axes sont particulièrement explorés, tels que le choix du matériau semi-conducteur, l'expérimentation de nouveaux agents de contraste ou encore l’optimisation des algorithmes de reconstruction. Avec son modèle Photonova™ Spectra, Ge Healthcare se distingue particulièrement par l’utilisation d’un détecteur épais au Silicium qui bénéficie d’une meilleure résolution spectrale que les détecteurs au CZT grâce à son énergie moyenne de création de paire plus faible. De même, le Silicium génère moins d’effets K-escape et permet un fenêtrage énergétique (5-10 keV) plus fin que celui des détecteurs au Cadmium (20-25 keV) [10]. Cependant, sa complexité de production, la prédominance des effets Compton et les limites de résolution spatiale atteignable pourraient restreindre le développement des PCD au Silicium. Enfin, de nouvelles collaborations sont également rendues possibles en l’exemple de GE Healthcare avec Nvidia pour l’intégration de leurs GPU (Graphics Processing Units) qui devraient permettre de réduire les durées de reconstruction tout en améliorant la qualité des images.
D’autres dispositifs sont actuellement en phase d'expérimentation, dont celui de Philips et de Canon, ou limités à un usage clinique localisé, comme le scanner crânial de Samsung Healthcare. Enfin, dans un contexte économique défavorable à l’innovation, les politiques d’investissement sur le comptage photonique varient également puisque Siemens envisage de s’orienter exclusivement sur cette modalité à moyen terme tandis que Philips continue de miser principalement sur son scanner spectral à intégration d’énergie.
IV. Contraintes et limites du comptage photonique
En plus de nécessiter une infrastructure réseau hospitalière adaptée à son intégration, le scanner à comptage photonique est également impacté par le volume de données générées lors de l’étape de détection. En effet, la réalisation des acquisitions en Ultra-Haute-Résolution impose de réduire la surface de détection afin de ne pas saturer l'électronique d’acquisition. La durée des examens est alors rallongée ce qui limite l'utilisation de ce mode pour certaines indications. Dans le cas d’un protocole d’acquisition à basse énergie pour l’exploration de structures de faibles différences de densité, la qualité des reconstructions est altérée par l’indisponibilité des informations tomodensitométriques sur l’ensemble du spectre (40 à 190 keV). De même, les reconstructions VNC nécessitent des niveaux d’acquisitions élevés : 140 à 190 keV, contrairement aux cartographie d’iodes réalisables à 120-140 keV. L’utilisateur doit donc déterminer au préalable le type de reconstruction qu’il souhaite pouvoir réaliser pour fixer la fenêtre d’énergie nécessaire tout en limitant la dose délivrée. Enfin, on note que l’imagerie K-edge, fonctionnalité exclusive du PCD-CT, est aujourd'hui inexploitable en routine clinique en raison de l’absence de produits de contraste compatibles.
D’autres contraintes intrinsèques liées à l’architecture des PCD sont égalements présentes telles que le partage de charge, ou Charge Sharing, qui correspond à la répartition du nuage d’éléctrons, engendré par un photon X incident, entre plusieurs pixels adjacents ce qui entraîne une diminution de la résolution spatiale et des erreurs de discrimination spectrale. Les photons X à haute énergie sont ainsi comptés comme plusieurs événements de faibles énergies.
Lorsque le rayonnement de fluorescence, provoqué par l’interaction du photon incident avec un K-électron, entraîne à son tour l’éjection puis la détection d’un électron sur un pixel différent de celui qui se trouve en coïncidence du lieu d’interaction du photon incident, on parle de phénomène K-escape. L'énergie recueillie par le pixel primaire est alors déplétée de l'énergie de liaison de l'électron ayant entraîné le rayonnement de fluorescence (et le phénomène K-escape) et donc sous évaluée. À l’inverse, un pixel adjacent perçoit ce déficit d'énergie sans qu’il n’y ait eu d’interaction en correspondance. Lorsque le rayonnement fluorescent à l’origine d’un événement détecté sur un pixel différent de celui en coïncidence du lieu d’interaction du photon incident est issu d’une interaction Compton (photon diffusé), on parle de Compton scattering. On note que l’augmentation de la dimension des pixels de l’anode pourrait permettre de mitiger ce phénomène mais réduirait par la même occasion la résolution spatiale. Dans l’ensemble de ces cas, le spectre d’énergie est déformé et la résolution spatiale réduite. Les phénomènes de Charge sharing et de K-escape sont représentés sur la Figure 16. [36]
Figure 16. Schéma des effets de Charge sharing et K-escape. [36]
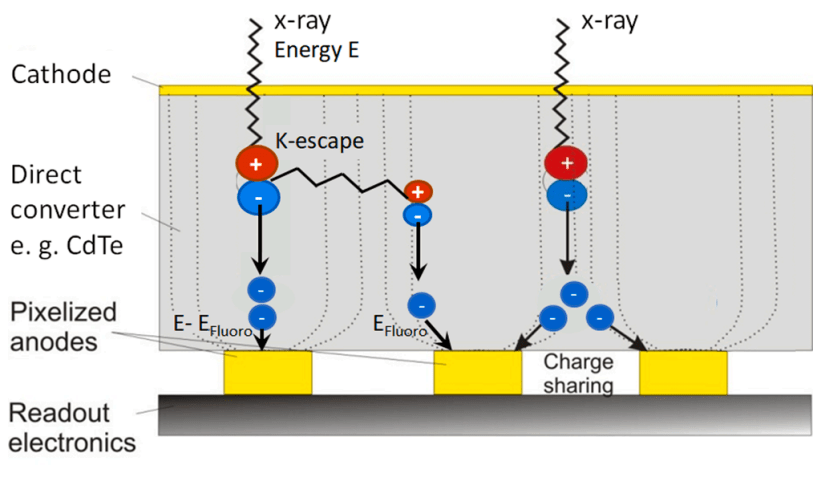
La structure planaire des détecteurs à comptage photonique présente également des compromis physiques importants. En effet, l’efficacité de collecte des paires électron-trou diminue avec l’épaisseur du semi-conducteur. Par ailleurs, la résistivité intrinsèque du semi-conducteur (liée à la pureté du matériau) impose de fortes limites à la tension de polarisation que l’on peut appliquer. Une résistivité trop faible entraîne un courant de fuite élevé ce qui dégrade le rapport signal/bruit. À l’inverse, une résistivité élevée réduit la zone déplétée et limite ainsi le parcours moyen des charges.
Enfin, le scanner à comptage photonique souffre également d’une limite que l’on retrouve sur les générations précédentes. Il s’agit du phénomène de Pile-Up, représenté Figure 17, se caractérisant par la superposition de plusieurs signaux (pulse) distincts, affectant ainsi la résolution énergétique par distorsion du spectre de détection. En effet, sous des flux de photons très élevés pouvant atteindre plusieurs centaines de millions d’interactions par mm² et par seconde, plusieurs charges peuvent arriver quasi simultanément au niveau des pixels de l’anode et être enregistrées comme un seul événement. Les algorithmes de décomposition des composants tissulaires basés sur ces informations, et qui constituent un des atouts majeurs de l’imagerie spectrale, sont alors altérés. On note que la mobilité des charges au sein des détecteurs à CZT ou CdZnTe est réduite par rapport au Si ce qui amplifie les effets de pile-up dans ces détecteurs [38].
Figure 17. Effet de superposition d'impulsions ou pile-up. [36]
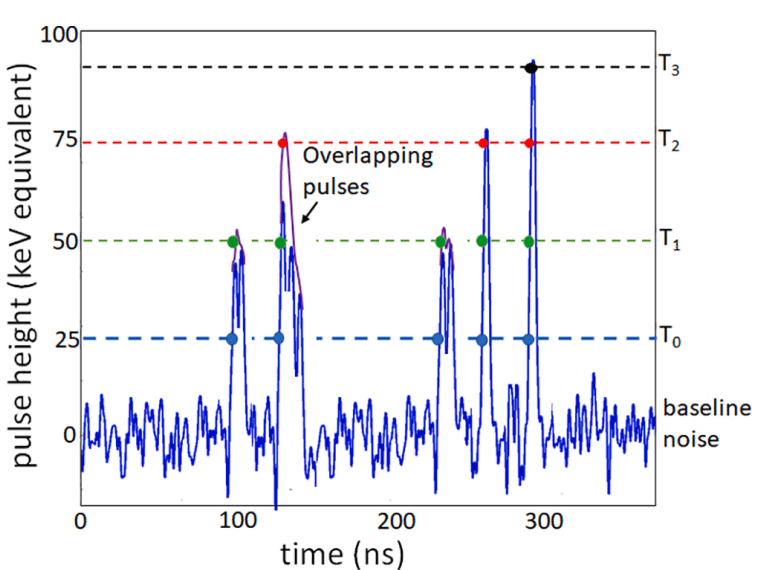
Avant de clôre cette dernière partie, le Tableau 1 rassemble les principaux avantages et inconvénients associés au scanner à comptage photonique :
Tableau 1 : Récapitulatif des avantages et inconvénients du scanner à comptage photonique. Sources : Auteur.e.s
| AVANTAGES | INCONVÉNIENTS |
| - Réduction potentielle du nombre d’examens complémentaires et/ou invasifs - Réduction significative de la dose et des volumes de produits de contraste sur plusieurs indications - Amélioration du niveau de détail et de la qualité des acquisitions (bruit, contraste, artéfacts) - Sensibilité spectrale intrinsèque simplifiant les reconstruction aux différents niveaux d'énergie - Introduction de l’imagerie multi-contraste | - Manque d’évaluations cliniques sur certaines applications et d’uniformisation des protocoles d’acquisitions - Augmentation significative de la quantité de données générées - Coûts d’acquisition significativement plus élevés que ceux des générations précédentes - L’usage clinique de l’UHR n’est pas toujours nécessaire ni bénéfique puisqu’il rallonge la durée des examens et ajoute du bruit à l’image |
Conclusion
L’imagerie tomodensitométrique conventionnelle offre la meilleure résolution spatiale tout en permettant une grande rapidité des acquisitions. Au cours des dernières années, le développement de cette modalité a permis de la positionner comme une référence incontournable pour la prise en charge d’un très grand nombre de pathologies. Cependant, elle est également associée à une exposition des patients aux rayonnements ionisants contrairement à d'autres modalités dont l’IRM. Bien qu’elles ne répondent pas aux mêmes indications cliniques et soient considérées comme complémentaires, le développement d’une nouvelle génération de scanner doit être justifié du fait de l’existence d’alternatives. Depuis l’introduction de l’imagerie spectrale, l’avènement récent des détecteurs à comptage photonique offre désormais une acquisition native sur plusieurs niveaux d’énergies. En répondant à plusieurs limites des anciens détecteurs à intégration d'énergie, ils contribuent à une imagerie diagnostique plus fine et devraient pouvoir offrir de nouveaux modes d’exploration tels que l’imagerie multi-contraste. L’usage du PCD-CT devrait progressivement se substituer à celui des EID-CT où la gestion de la dose, du produit de contraste et de la qualité image reste un problème, et pourrait même devenir la référence sur des indications aujourd’hui réservées à d’autres modalités, comme la coronarographie à visée diagnostic. Néanmoins, il souffre également de contraintes à prendre en considération même si plusieurs d'entre elles devraient être en partie mitigées avec la maturité des dispositifs.
À l’avenir, on peut espérer voir de nouvelles avancées concernant les agents de contraste à base de nanoparticules qui pourraient permettre l'accès à une imagerie morpho-fonctionnelle. Leur développement s’avère particulièrement intéressant pour une possible application en suivi oncologique notamment. Cependant, l’utilisation du Gadolinium nécessite actuellement un volume d’injection 10 fois supérieur à celui de l’IRM. D’autre part, l’Or ou le Bismuth sont aujourd’hui interdits en usage clinique chez l’Homme ce qui pourrait contrarier leur utilisation. La conception de fantômes spécifiques et l’élaboration de protocoles de contrôle qualité adaptés aux nouvelles techniques d’imagerie et de résolution doivent également accompagner cette technologie. L'évolution constante des capacités de traitement de l'électronique d'acquisition, qui constituent aujourd’hui un facteur limitant sur les acquisitions en Ultra-Haute-Résolution, pourrait permettre de diminuer les durées d’examens et les doses associées. Enfin, la constitution de bases de données et le développement d’outils de Deep Learning Reconstruction (DLR) représentent des axes d’investissements majeurs pour les fabricants qui misent sur ces solutions pour améliorer l’ensemble de leurs produits, des algorithmes de traitement des données à la simplification du workflow pour les utilisateurs.
Si l’innovation représente indéniablement un enjeu stratégique pour les constructeurs afin de maintenir leur compétitivité, elle répond avant tout à des besoins cliniques concrets et à des exigences croissantes en matière de qualité diagnostique et de radioprotection. De même, l’acquisition de ces équipements par les établissements de santé ne relève pas uniquement d’une démarche d’image ou de prestige, mais s’inscrit dans une volonté d’amélioration de la prise en charge des patients, en particulier pour les pathologies les plus sensibles ou nécessitant des examens répétés. Leur adoption repose notamment sur une formation adaptée des utilisateurs pour augmenter la confiance diagnostique en permettant l’interprétation des acquisitions pouvant révéler de nouveaux types de lésions. Malgré des contraintes médico-économiques et organisationnelles importantes, le scanner à comptage photonique s’impose ainsi comme une évolution pertinente, cohérente et majeure de l’Imagerie Médicale, renforçant la place de la scanographie au sein d’une approche multimodale moderne et complémentaire.