Guides des bonnes pratiques de l'ingénierie biomédicale en établissement de santé : revue de synthèse
L’accès rapide aux travaux ci-dessous visent à contribuer aux progrès et aux évolutions :
- De l’ingénierie biomédicale en établissement de santé,
- Des technologies et de la maîtrise des dispositifs médicaux.
Citez vos sources quand vous les utilisez et n’hésitez pas à les partager. Bonne lecture !

ID interne : 2021_01_idsoa
Auteur : Dr Ing Gilbert FARGES (HDR)
Contact : gilbert.farges@utc.fr
Citation à rappeler pour tout usage : Gilbert FARGES, « Guides des bonnes pratiques de l'ingénierie biomédicale en établissement de santé : revue de synthèse », Université de Technologie de Compiègne (France), Master Ingénierie de la Santé, Laboratoire Biomécanique et Bioingénierie (BMBI - UMR CNRS 7338, avril 2021, https://travaux.master.utc.fr/open-access/2021_01_idsoa
Dernière mise à jour : 16 octobre 2025
Raisons d'être
Cet article retrace la genèse et les retours d'expérience sur les "Guides des Bonnes Pratiques Biomédicales" développés en France depuis 2002. Il présente les éléments-clefs et les évolutions internationales francophones des bonnes pratiques biomédicales que les ingénieurs et techniciens biomédicaux peuvent mettre en œuvre dans leurs établissements de santé.
Les bonnes pratiques biomédicales en établissement de santé sont un ensemble d'activités d'achat, de maintenance, de contrôle qualité, de formation, de veille technologique, normative et règlementaire, de vigilance et de suivi des dispositifs médicaux. Elles concernent les ingénieurs ou techniciens biomédicaux exerçant dans les hôpitaux, cliniques ou autres structures exploitant des dispositifs médicaux, que ce soit à un niveau local individualisé ou à un niveau territorial dans un groupement d'établissements.
Les Bonnes Pratiques Biomédicales visent à aider les acteurs biomédicaux à contribuer à la qualité et à la sécurité des dispositifs médicaux mis à disposition des soignants afin que les patients bénéficient des meilleurs soins possibles via les technologies de santé accessibles.
Pour cela, le meilleur de l'état de l'art est identifié par des pairs volontaires ayant une expérience professionnelle approfondie des métiers de l'ingénierie biomédicale en établissement de santé. Après concertation et validation collectives, cet état de l'art est publié dans un Guide des Bonnes Pratiques Biomédicales et diffusé le plus largement possible.
Les démarches et travaux collectifs ont été souvent orchestrés par l'auteur, enseignant-chercheur à l'Université de Technologie de Compiègne, dans le cadre de recherches pré-normatives et d'enseignements en ingénierie biomédicale et en management de la qualité.
Guide biomédical (2002)

Le 1er Guide des bonnes pratiques biomédicales en établissement de santé est édité en novembre 2002 dans la revue ITBM-RBM News de l'éditeur Elsevier [1].
Trois associations professionnelles d'ingénieurs et de techniciens biomédicaux français ont validé ce guide avec la contribution de 45 co-auteurs :
Ce guide a été conçu après avoir dressé le constat, à partir des années 2000, des difficultés pour les services biomédicaux français de développer et maintenir des certifications ISO 9001 "Management de la Qualité" depuis les premières obtenues en 1997 (voir [3] dans les références) :
- Par exemple, la difficulté de décrypter les exigences normatives souvent absconses pour les transformer en actions et résultats compréhensibles par les ingénieurs et techniciens biomédicaux néophytes en culture et langage de la qualité.
- Egalement, la difficulté à consacrer le temps nécessaire pour rédiger des manuels, procédures, enregistrements associés à la "Certification Qualité". Ce temps peut-être estimé "improductif" et au détriment des actions techniques, toujours prioritaires, de maintenance et de contrôle qualité des dispositifs médicaux dont le service biomédical a la charge.
- Enfin, le peu d'appui en ressources et en reconnaissance de la part des hiérarchies, Directions ou Tutelles des établissements de santé, auxquelles sont rattachés les services biomédicaux.
Face à ce constat, les initiateurs du projet ont visé de rédiger collectivement un ensemble de bonnes pratiques "par" et "pour" les acteurs biomédicaux en établissement de santé :
- Aucune subvention publique ou aide financière privée n'a été sollicitée afin de garder la "neutralité" nécessaire à la future légitimité professionnelle souhaitée pour les Guides Biomédicaux.
- Les mots utilisés sont directement ceux de la profession afin de rendre les bonnes pratiques directement applicables. Pour cela ce sont les acteurs biomédicaux eux-mêmes qui proposent les contenus des bonnes pratiques via des interactions numériques et une orchestration unique de la part de l'UTC.
- L'amélioration continue, qui est la base de toute démarche qualité, est intégrée dans la structure même des guides des bonnes pratiques biomédicales afin de faciliter le cheminement vers des certifications ultérieures de type ISO 9001. En cela, les compétences de l'auteur en management de la qualité ont été exploitées avec l'aide des nombreux étudiants qui ont participé à l'évolution continue des pratiques biomédicales en établissement de santé.
Structure
Le Guide biomédical 2002 présente les bonnes pratiques selon 2 catégories s'adressant :
- soit aux ingénieurs et responsables des services biomédicaux avec les Bonnes Pratiques Fonctionnelles (BPF),
- soit aux techniciens biomédicaux avec les Bonnes Pratiques Opérationnelles (BPO).
BONNES PRATIQUES FONCTIONNELLES (BPF)
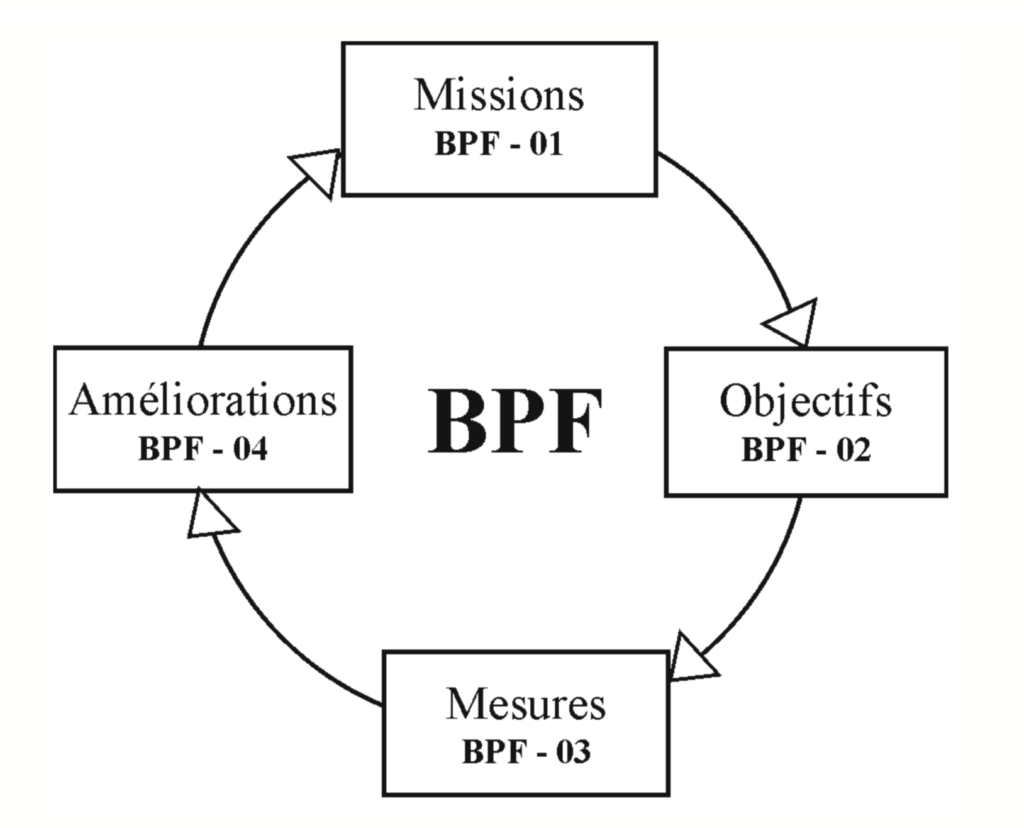
Les BPF sont structurées selon un cycle d'amélioration continue garantissant un progrès permanent des activités selon les retours d'expérience et les évolutions du métier.
- BPF-01 : missions
- BPF-02 : objectifs
- BPF-03 : mesures
- BPF-04 : améliorations
BONNES PRATIQUES OPÉRATIONNELLES (BPO)
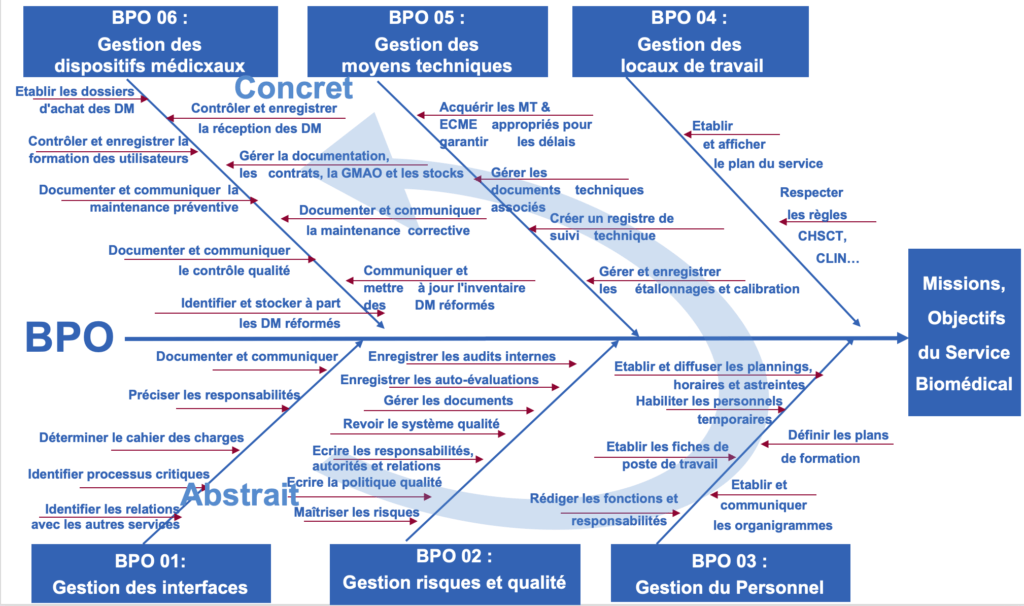
Les BPO explicitent comment atteindre les objectifs des BPF en allant du plus "abstrait" (BPO-01) au plus "concret" (BPO-06)
- BPO-01 : processus de gestion des interfaces avec les services
- BPO-02 : processus de gestion des risques et de la qualité
- BPO-03 : processus de gestion du personnel
- BPO-04 : processus de gestion des locaux
- BPO-05 : processus de gestion et de suivi des matériels techniques et équipements de contrôle, de mesure et d’essai
- BPO-06 : processus de gestion et de suivi des dispositifs médicaux
Auto-évaluation
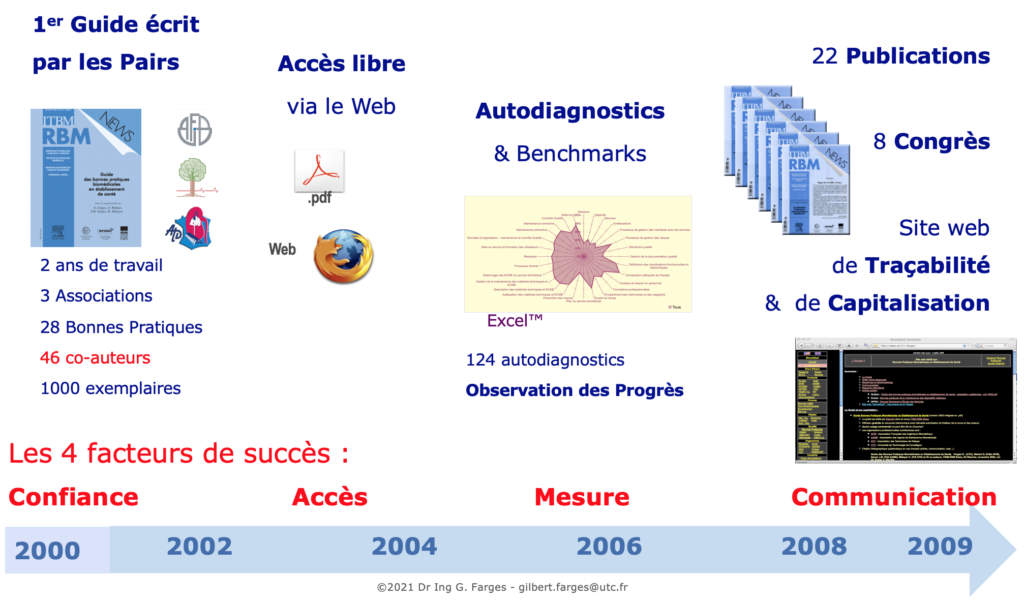
Un outil de diagnostic libre d'usage a été publié en 2004 suite à des travaux d'étudiants en DESS Technologies Biomédicales Hospitalières de l'UTC [2].
Cet outil est basé sur un tableur Excel® préformaté pour les 28 bonnes pratiques déclinées en 117 processus.
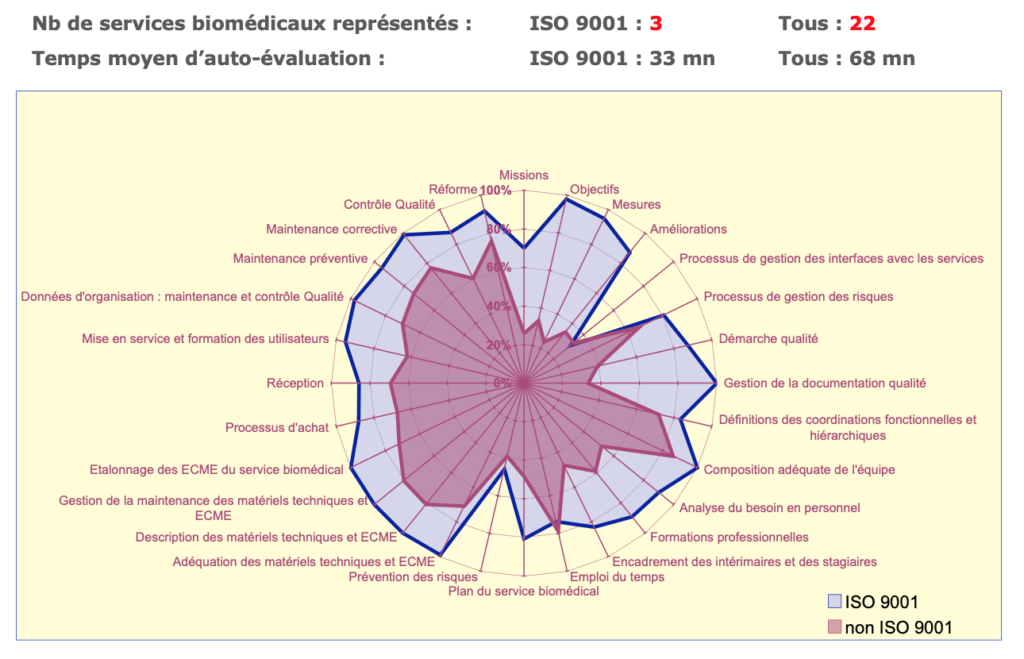
Il permet une évaluation rapide et l'obtention immédiate du résultat sous forme d'un graphe radar présentant en un coup d'œil les scores des 28 bonnes pratiques.


Avec cet outil de diagnostic de nombreux services biomédicaux français ont pu évaluer leurs pratiques de 2004 à 2007. En garantissant la confidentialité des réponses, des moyennes ont pu être calculées et communiquées périodiquement auprès des professionnels lors des journées techniques biomédicales organisées annuellement par l'AFIB ou l'AAMB.
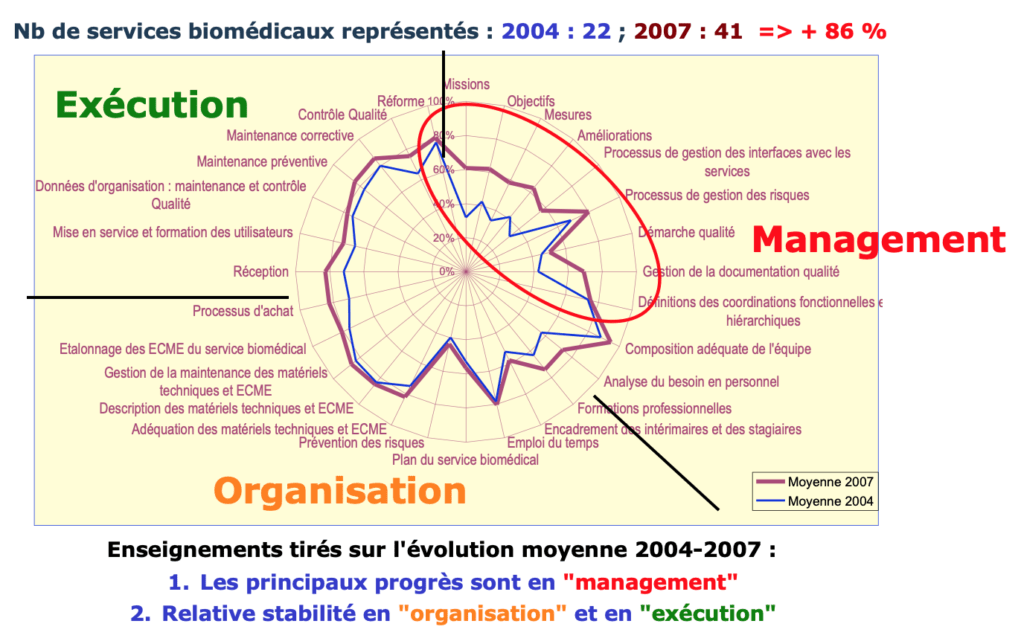
Ces comparaisons ("benchmarks") ont montré que les démarches qualité aboutissant à une certification ISO 9001 favorisaient grandement le respect des bonnes pratiques biomédicales et que des progrès significatifs dans le management ont été accomplis entre 2004 et 2007.
Adaptation Québécoise (2005)
Grâce à l'autorisation donnée en 2004 de diffusion libre du Guide biomédical 2002 par l'éditeur Elsevier et les associations co-autrices (AFIB, AAMB et ATD), les ingénieurs biomédicaux québécois ont pu le découvrir sur le web accompagné de son outil de diagnostic.
L'Association des Physiciens et Ingénieurs Biomédicaux Québecois (APIBQ) s'est alors montrée très intéressée à entreprendre une démarche similaire afin de démontrer les compétences maîtrisées de ses adhérents et d'augmenter leur reconnaissance auprès des directions et tutelles de leurs établissements de santé.
Les contacts initiaux réalisés à Montréal en juillet 2004 à l'invitation de l'APIBQ ont permis de cerner les avantages structurels du Guide 2002 et la méthode pour l'adapter rapidement au contexte québécois.


Ainsi, en juin 2005, l'adaptation québécoise du Guide des Bonnes Pratiques Biomédicales est éditée et diffusée par l'APIBQ avec son outil de diagnostic en fichier Excel® :
- Adaptation québécoise du Guide des Bonnes Pratiques Biomédicales - Juillet 2005 - APIBQ (.pdf)
- Adaptation québécoise de l'outil de diagnostic pour le Guide biomédical québécois - APIBQ (.xls)
La dynamique professionnelle a été maintenue grâce à des retours périodiques faits à la communauté biomédicale soit par des communications lors de leurs Journées Techniques annuelles, soit par des publications dans la revue IRBM News, dédiée à l'ingénierie biomédicale et lue tout autant par les techniciens que par les ingénieurs biomédicaux.
Entre 2002 et 2009, les retours d'expérience ont montré les progrès accomplis et les évolutions nécessaires pour une mise à jour du Guide 2002.

Publications associées
De nombreux travaux ont ensuite été publiés sur les retours d'expérience de ce premier guide biomédical de 2002. Ceux-ci sont accessibles librement et gratuitement ci-dessous dans leurs versions "pre-print" en conformité avec les règles des éditeurs.
- Naissance du guide des bonnes pratiques biomédicales en établissement de santé [3]
- Premiers retours d'expérience du « Guide des bonnes pratiques biomédicales en établissement de santé [4]
- Contribution à la démarche de validation en « bonnes pratiques biomédicales : la grille d'évaluation [5]
- Validation d'un service en « bonnes pratiques biomédicales : les voies possibles [6]
- Proposition de « Bonne Pratique : contrôle qualité interne en mammographie analogique de dépistage systématique [7]
- Analyse de pratiques biomédicales à l'étranger : les prémices d'un réseau biomédical hospitalier international ? [8]
- Contribution méthodologique aux bonnes pratiques en contrôle qualité des ventilateurs artificiels en usage hospitalier [9]
- Guide des bonnes pratiques biomédicales en établissement de santé : Un outil qui atteint son objectif ? [10]
- Guide des bonnes pratiques biomédicales en établissement de santé : retours d'expérience 2004 [11]
- Proposition d'une « bonne pratique opérationnelle : prévention des risques pour le personnel au service biomédical [12]
- Proposition d'une bonne pratique en coopération internationale biomédicale [13]
- Proposition d’une nouvelle bonne pratique relative à l’encadrement et l’accueil d’un stagiaire [14]
- « Guichet unique » sur le Guide des bonnes pratiques biomédicales : un projet inter-associatif [15]
- Guide des bonnes pratiques biomédicales : évolutions 2004-2007 et perspectives d’une version 2 [16]
- Comment améliorer la confiance dans l’auto-diagnostic associé au Guide des bonnes pratiques biomédicales ? [17]
- Réflexions sur une nouvelle structure du Guide des bonnes pratiques biomédicales en établissement de santé [18]
- Enseignements 2003-2008 et projet v2010 du Guide des bonnes pratiques biomédicales en établissement de santé [19]
- Proposition d’une nouvelle structure pour le guide des bonnes pratiques biomédicales version 2010 [20]
- Guide des bonnes pratiques biomédicales version 2 : compatibilité, progressivité et simplicité [21]
Guide biomédical (2011)

Le second Guide des bonnes pratiques de l'ingénierie biomédicale en établissement de santé est édité en 2011 en ouvrage indépendant aux éditions Lexitis [22].
L'autorisation de diffusion publique a été donnée par l'éditeur en novembre 2017 afin de contribuer à sa large diffusion auprès des professionnels biomédicaux.
Il est le résultat de 2 ans de travaux collectifs menés de 2009 à 2011 et intègre les retours d'expérience du 1er guide dont il reprend environ 80% des anciens contenus en les améliorant et en les approfondissant.
Il utilise le mot "ingénierie biomédicale" dans son titre afin de faciliter auprès de tout public néophyte une compréhension directe du secteur d'application des bonnes pratiques : il n'est ni "biologique", ni "médical" mais en lien avec les aspects technologiques des dispositifs médicaux exploités en établissement de santé.
Après le succès du 1er guide biomédical et de son adaptation québécoise, huit associations professionnelles d'ingénieurs et de techniciens biomédicaux francophones ont participé à la rédaction et validé ce 2ème guide biomédical 2011 avec la contribution de 90 co-auteurs :
- Association Française des Ingénieurs Biomédicaux (AFIB)
- Association des Agents de Maintenance Biomédicale (AAMB)
- Association des Techniciens de Dialyse (ATD)
- Association nationale des cadres et experts techniques hospitaliers (H360)
- Association des Physiciens et Ingénieurs Biomédicaux du Québec (APIBQ)
- Association des Technologues en Génie BioMédical (ATGBM)
- Association Francophone Inter hospitalière Techniciens Biomédicaux de Belgique (AFITEB)
- Association Francophone des Professionnels des Technologies de Santé (AFPTS)
Structure
Le guide 2011 simplifie le nombre de bonnes pratiques à 9 et le nombre de processus à 48, tout en permettant un usage adapté à l'international et un accès aux activités connexes mais hétérogènes qui peuvent incomber aux services biomédicaux.
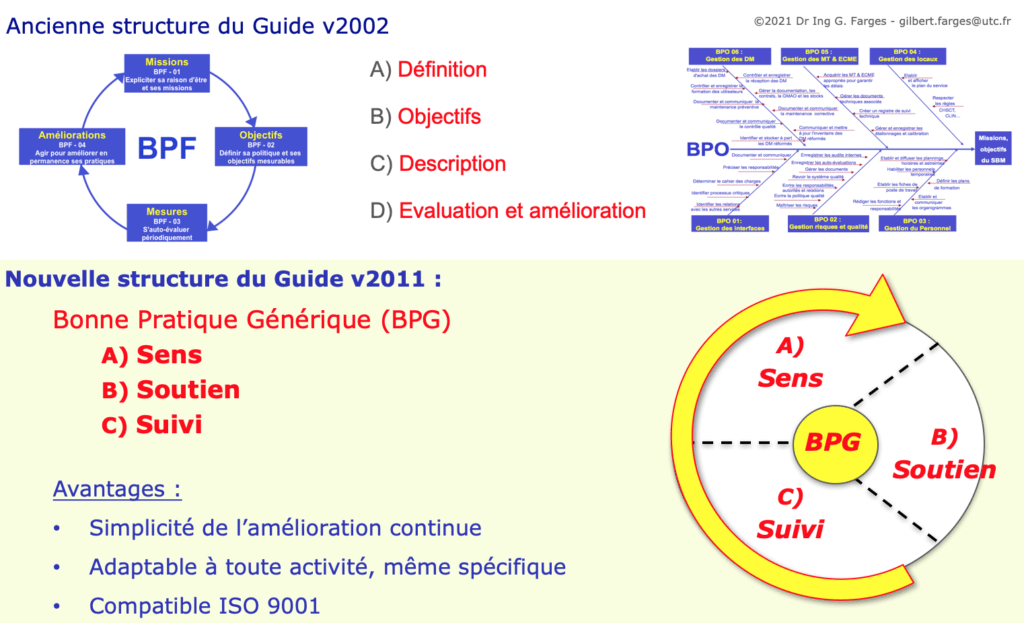
Il exploite pour cela le concept d'une Bonne Pratique Générique (BPG) structurée en 3 phases simples à mémoriser et directement associées à un cycle d'amélioration continue, les "3 S" de :
- SENS : afin de définir et d'expliciter les raisons d'être des activités biomédicales
- SOUTIEN : afin d'identifier les ressources matérielles et immatérielles nécessaires au succès des activités
- SUIVI : afin de préciser les processus et activités à réaliser et comment mesurer leur performance sur les 3 dimensions Efficacité, Efficience et Qualité perçue
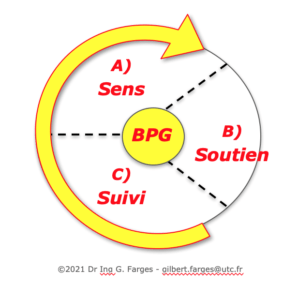
La structure du Guide biomédical 2011 est déclinée en toute cohérence selon les "3 S" pour ses 9 bonnes pratiques :
SENS - Bonnes Pratiques de Management (BPM)
- BPM 1 : Manager le service et la communication
- BPM 2 : Manager la mesure du succès
- BPM 3 : Manager l’innovation et le progrès
SOUTIEN - Bonnes Pratiques d’Organisation (BPO)
- BPO 1 : Organiser les interfaces
- BPO 2 : Organiser la qualité attendue
- BPO 3 : Organiser les ressources
SUIVI - Bonnes Pratiques de Réalisation (BPR)
- BPR 1 : Réaliser les activités support
- BPR 2 : Réaliser la gestion des dispositifs médicaux
- BPR 3 : Réaliser les activités connexes en ingénierie biomédicale
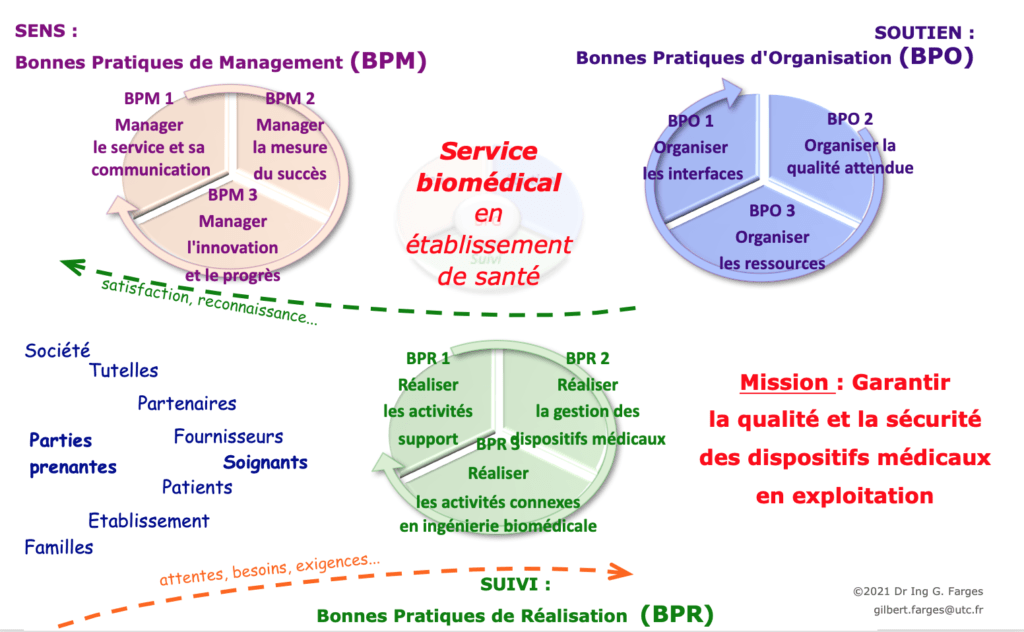
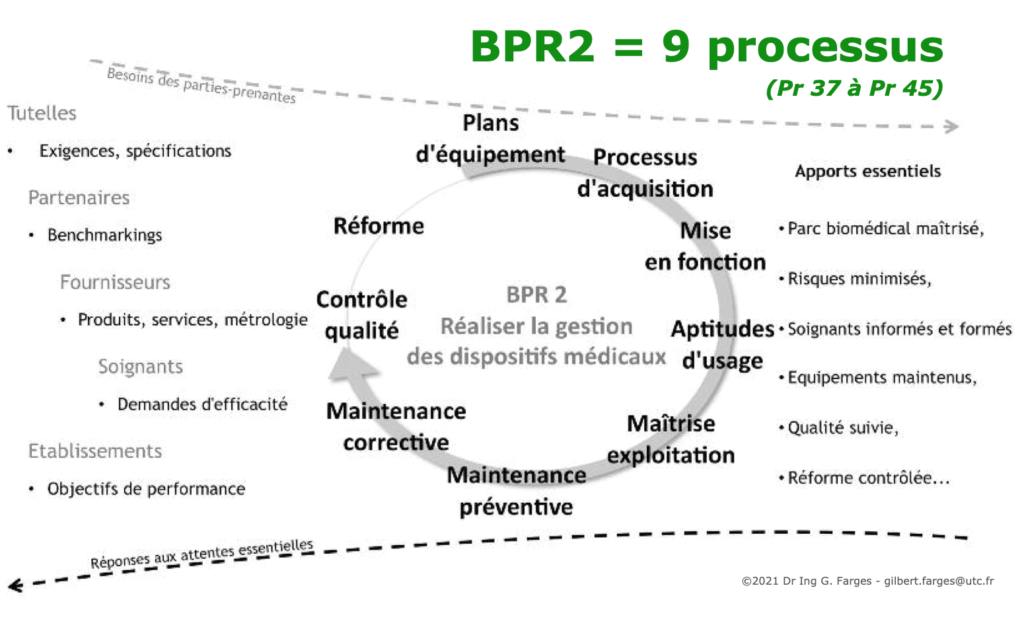
Chacune des 9 bonnes pratiques est elle-même déclinée et détaillée selon les "3 S" :
- SENS : Définition, Enjeux, Objectifs, Innovation et progrès associés à la bonne pratique,
- SOUTIEN : Parties-prenantes, ressources génériques internes et externes à l'établissement, ressources spécifiques selon les pays,
- SUIVI : Cartographie et explicitation des processus, indicateurs de performance en "efficacité", "efficience" et "qualité perçue".
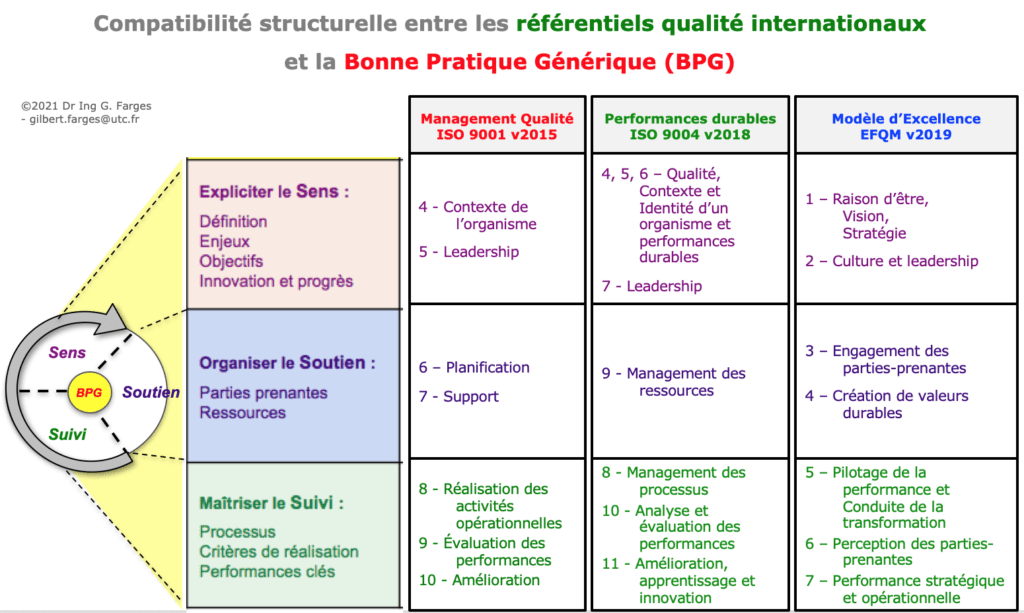
Par rapport à celle du Guide 2002, la nouvelle structure originale des "3 S" pour le Guide 2011 permet des correspondances directes avec les meilleurs référentiels qualité internationaux cités et illustrés ci-dessous :
- ISO 9001 "Systèmes de management de la qualité - Exigences",
- ISO 9004 "Management de la qualité - Qualité d'un organisme - Lignes directrices pour obtenir des performances durables",
- Modèle d'Excellence de l'European Foundation for Quality Management (EFQM).
Ceci peut induire et faciliter des dynamiques de progrès valorisées par des certifications ou des reconnaissances internationales pour les services biomédicaux ayant une maturité suffisante sur les bonnes pratiques biomédicales.
Activités Connexes à l'Ingénierie Biomédicale
Les activités connexes en ingénierie biomédicale intègrent toute bonne pratique qui pourrait être mise en œuvre par un service biomédical particulier en cohérence avec son contexte, mais qui n'est pas nécessairement applicable, utile ou pertinente pour d'autres services biomédicaux.
C'est un moyen simple et innovant pour rendre "agile" un référentiel métier qui peut ainsi s'adapter aux multiples contextes biomédicaux différents, aux pratiques spécifiques à certains et pertinentes à valoriser et aux évolutions du métier de l'ingénierie biomédicale.
Le guide biomédical 2011 intègre directement 3 Bonnes Pratiques d'Activités Connexes (BPAC), dont les contenus ont été publiés antérieurement. Leurs contenus extraits du Guide 2011 sont disponibles librement ci-dessous :
- BPAC 1 : Bonne pratique en coopération internationale biomédicale
- cette BPAC fait suite à la publication suivante : Proposition d'une bonne pratique en coopération internationale biomédicale [13]
- BPAC 2 : Bonne pratique de gestion de l’accueil et de l’encadrement de stagiaires
- cette BPAC fait suite à la publication suivante : Proposition d’une nouvelle bonne pratique relative à l’encadrement et l’accueil d’un stagiaire [14]
- BPAC 3 : Bonne Pratique du contrôle qualité interne en mammographie à rayons X analogique de dépistage systématique du cancer du sein pour respecter la réglementation française
- cette BPAC fait suite à la publication suivante : Proposition de « Bonne Pratique : contrôle qualité interne en mammographie analogique de dépistage systématique [7]
Auto-évaluation
Pour évaluer le niveau de respect des bonnes pratiques, un outil de diagnostic est disponible en accès libre. Il est conçu à partir d'un tableur Excel® préformaté et semi-automatisé dont chaque onglet peut servir d'enregistrement qualité et de preuve pour des audits internes ou externes.
Les échelles d'évaluation sont nuancées et utilisent à la fois la "véracité" pour évaluer le niveau de réalisation des actions et la "maturité" pour évaluer le niveau de maîtrise des processus, ce dernier point étant recommandé par la majorité des référentiels qualité internationaux.
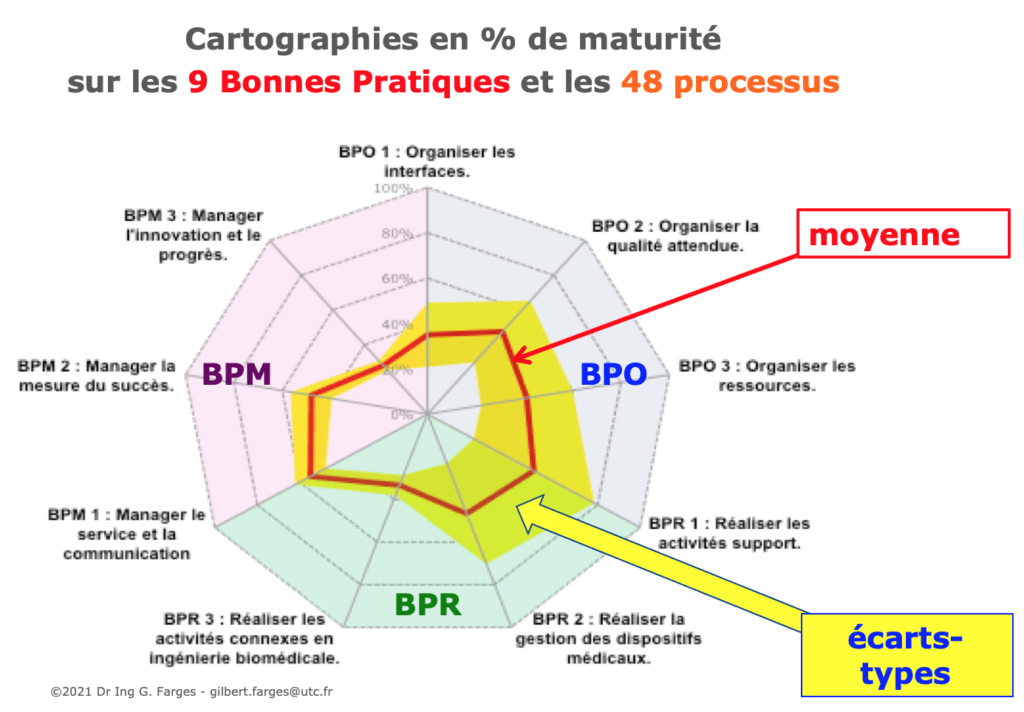
L'outil de diagnostic permet une évaluation rapide et l'obtention immédiate du résultat sous forme d'un graphe radar présentant en un coup d'œil les scores des 9 bonnes pratiques et 48 processus.
Pour minimiser les effets de la subjectivité humaine, l'évaluation peut se faire individuellement ou collectivement jusqu'à 5 personnes ou groupes différents. Les résultats présentent à la fois la moyenne des évaluations indépendantes réalisées et les écarts-types dont l'analyse, en cas de divergence importante entre les évaluateur, peut être riche de sources de progrès internes.

Si les résultats sont probants, il est possible d'éditer une déclaration de conformité préformétée selon la norme internationale ISO 17050 "Évaluation de la conformité - Déclaration de conformité du fournisseur - Partie 1 : exigences générales" conduisant rapidement et gratuitement une reconnaissance dite "1ère partie" :
Il est proposé en téléchargement sur le site de l'éditeur [23] avec un mode d'emploi détaillé et illustré dans l'Addenda 2013 [24] du guide de 2011.

Publications associées
L'ADDENDA 2013 du Guide 2011 des bonnes pratiques de l’ingénierie biomédicale en établissement de santé [24] détaille le mode d'emploi de l'outil de diagnostic ainsi que 2 nouvelles bonnes pratiques d'activités connexes (BPAC 4 et 5), disponibles librement ci-dessous après extraction de l'ADDENDA 2013 :

BPAC 6 - Biomédical et GHT en France
En 2019, une 6ème BPAC a été publiée afin de prendre en compte l'évolution du système de santé français en Groupements Hospitaliers de Territoires (GHT). Les publications afférentes sont disponibles en pre-print :
- BPAC 6 : les raisons d'être de l'ingénierie biomédicale au sein d’un groupement hospitalier de territoire en France [25]

L'outil de diagnostic afférent à la BPAC 6 est proposé gratuitement en téléchargement sur le site web de capitalisation des travaux du Master Ingénierie de la Santé de l'UTC :
En plus d'un fichier Excel® préformaté et semi-automatisé, une découverte rapide de la BPAC 6 est disponible sous forme d'une cartographie interactive.

Autres travaux publiés en lien avec le guide biomédical 2011 :
- Retour d’expérience sur la mise en place du Guide des bonnes pratiques en ingénierie biomédicale pour les établissements de santé "version 2011" » [30]
- Bilan de l’usage des Bonnes Pratiques en Ingénierie Biomédicale, G. Pénisson, F.Z. Meskini, G. Farges, IRBM News, 2014, Vol. 35, n° 5-6, pp 153-156, https://doi.org/10.1016/j.irbmnw.2014.10.004 ; https://travaux.master.utc.fr/articles-publies/2014_05_ttsap/ [31]
Outil de Management Guide 2011
En 2022, un nouvel outil est proposé pour le Guide des Bonnes Pratiques de l'ingénierie Biomédicale en Établissement de Santé édition 2011. Basé sur les constats d'une certaine complexité de l'outil développé en 2013, ce nouvel outil est un véritable Outil de Management, simple et rapide d'emploi, grâce à l’ajout d’une cartographie des processus à déployer et d’un planning de suivi des plans d'amélioration décidés collectivement.
L'outil de management afférent au Guide biomédical v2011 est proposé gratuitement en téléchargement sur le site web de capitalisation des travaux du Master Ingénierie de la Santé de l'UTC :
En plus d'un fichier Excel® préformaté et semi-automatisé, une découverte rapide de l'outil de management est disponible sous forme d'une vidéo.

Autres travaux publiés en lien avec l'Outil de Management pour le guide biomédical 2011 :
- Bonnes Pratiques en Ingénierie Biomédicale : de l'autodiagnostic au management. L. Blanpain, M. Bourjac, B. Dejenne, M. Saksik, D. Mamoud, G. Farges, IRBM News, juin 2022, Vol. 43, n°3, 5 pages, https://doi.org/10.1016/j.irbmnw.2022.100402 ; https://travaux.master.utc.fr/articles-publies/2022_02_idsap/ [32]
Références bibliographiques
[1] Gilbert Farges, Geneviève Wahart, Jean-Marc Denax, Hubert Métayer, « Guide des bonnes pratiques biomédicales en établissement de santé », ITBM RBM News, Elsevier, vol. 23, no Suppl 2, novembre 2002, p. 32 (https://doi.org/10.1016/S1297-9570(02)80019-X ; https://doi.org/10.1016/S1297-9570(02)80015-2 ; https://doi.org/10.1016/S1297-9570(02)80018-8)
[2] Anne Guyard,Contribution à la démarche de validation en "bonnes pratiques biomédicales" : la grille d'évaluation, Anne Guyard, Laurent Tamames, Gilbert Farges, IRBM News, vol. 25, n° 2, p. 3-6, avril 2004, https://doi.org/10.1016/S1297-9570(04)80018-9 ; https://travaux.master.utc.fr/articles-publies/2004_02_tbhap/
[32] Bonnes Pratiques en Ingénierie Biomédicale : de l'autodiagnostic au management. L. Blanpain, M. Bourjac, B. Dejenne, M. Saksik, D. Mamoud, G. Farges, IRBM News, juin 2022, Vol. 43, n°3, 5 pages, https://doi.org/10.1016/j.irbmnw.2022.100402 ; https://travaux.master.utc.fr/articles-publies/2022_02_idsap/